Геллан негізінде гидрофильді композициялық материалдарды құру және олардың физика-химиялық қасиеттерін зерттеу


Қазақстан Республикасының білім және ғылым министрлігі
әл-Фараби атындағы Қазақ Ұлттық университеті
Мұхамедияр Ж.
ГЕЛЛАН НЕГІЗІНДЕ ГИДРОФИЛЬДІ КОМПОЗИЦИЯЛЫҚ МАТЕРИАЛДАРДЫ ҚҰРУ
ДИПЛОМДЫҚ ЖҰМЫС
«050721 - Органикалық заттардың химиялық технологиясы» мамандығы
Алматы 2013
Қазақстан Республикасының білім және ғылым министрлігі
әл-Фараби атындағы Қазақ Ұлттық университеті
Химия және химиялық технология мамандығы
Органикалық заттар, табиғи қосылыстар және полимерлер химиясы мен технологиясы кафедрасы
Кафедра меңгерушісінің
рұқсатымен қорғауға жіберілді
Ж. Ә. Әбілов
«» 2013 ж.
ДИПЛОМДЫҚ ЖҰМЫС
ГЕЛЛАН НЕГІЗІНДЕ ГИДРОФИЛЬДІ КОМПОЗИЦИЯЛЫҚ МАТЕРИАЛДАРДЫ ҚҰРУ
«050721 - Органикалық заттардың химиялық технологиясы» мамандығы
Орындаған Ж. Мұхамедияр
Ғылыми жетекші:
химия ғылымдарының кандидаты,
доцент Р. А. Маңғазбаева
Нормобақылаушы
к. х. н., аға оқытушы Г. Ж. Қайралапова
Алматы 2013
МАЗМҰНЫ
ҚЫСҚАРТУЛАР, БЕЛГІЛЕР ЖӘНЕ БЕЛГІЛЕНУЛЕРДІҢ ТІЗІМІ
ПАҚ - полиакрил қышқылы
TDPG - тимин-5-дифосфат глюкоза
UDPG - уридин-5-дифосфат глюкоза
- ӘДЕБИ ШОЛУ
1. 1 Геллан шайырының алынуы және олардың физика-химиялық қасиеттері
Полисахаридтер, гликандар - молекуласында гликозидті байланысқан он мыңнан артық моносахарид қалдықтары бар көмірсулар. Полисахаридтердің молекулалық массасы бірнеше мыңнан (ламинарин, инсулин) бірнеше миллионға дейін (гиалурон қышқылы, гликоген) жетеді. Полисахаридтерге моносахаридтердің бір ғана түрінен немесе әр түрінен құралатын целлюлоза, крахмал, геллан, хитин, пектиндік заттар, гликопротеиндер, гепарин, т. б. жатады. Полисахаридтер сілтіге төзімді, қышқылда диполимерленеді, суда жақсы ериді [1] .
Полисахаридтер табиғи жоғары молекулалы қосылыстар. Полисахаридтердің жалпы формуласы (С 6 Н 10 О 5 ) n , көптеген моносахарид молекуласының қалдықтарынан тұрады. Макромолекуладағы моносахаридтер қалдықтары полисахаридтерде де оттек "көпіршесі" арқылы жалғасқан:
. . . Р - О - Р - О - Р . . .
Өсімдіктер мен жануарлар организмінде ферменттердің әсерінен фотосинтез нәтижесінде түзілген моносахарид молекулалары поликонденсацияланып, полисахаридтер түзіледі:
6СО 2 + 6Н 2 О → С 6 Н 12 О 6 + 6О 2
н С 6 Н 12 О 6 → (С 6 Н 10 О 5 ) н + н H 2 О
Ондаған жылдардан бері микробиологиялық экзополсахаридтер тамақ өнеркәсібінде, сондай-ақ фармацевтика мен басқада химиялық технологияның бағалы шикізаты ретінде қолданыс табуда. Микробиологиялық полисахаридтерге жататын геллан өзінің жылуға сезімталдық ерекше қасиеті болуымен қолдану маңыздылығы артып келеді [2] .
Геллан Pseudomonas elodea [3] мен тетрасахаридтің қайталануымен түзілген α-L-рамноза, бір β-D-глюкурон қышқылы және екі β-D-глюкоза қалдығының ферменттену барысында түзілген [4, 5], аниондық, жоғары молекулалы, деацетилденген сыртқы жасушалық полисахаридті шайыр. Түзілген ағза болса ауру тудырмайтын қасиетке ие аэробтық, грамтерістік бактерия (gram-negative bacterium) [6] . Бұл организимдер пайдалы қасиеттері бар табиғи түзілетін гидроколлоидтарды іздеу барысында табылған.
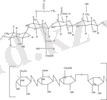
Полисахаридттердің химиялық құрылымы қосарланған тетрасахарид тізбегінен құралған екі глюкоза қалдығы, бір глюкон қышқылы қалдығы, бір рамноза қалдығынан тұрады [7, 8] . Бұлар бірлесіп тетрасахарид тізбегін құрайды (сурет 1) . Табиғи полисахарид L-глицерин мен сірке қышқылымен жартылай эфирленген [9], бірақ сатымдылық өнім Gelrite R негізбен өңдеу арқылы эфирсізденген [10, 11] . Геллан шайырының нақты формуласы глюкон қышқылдарын әр түрлі тұздармен бейтараптауға байланысты басқа полисахаридтерден өзгешелеу.
 n
n
[→3] -β-D-Glcp-(1→4) - β-D-GlcpA-(1→4) -β-D-Glcp-(1→4) -α-L-Rhap-(1→]
Сурет 1 - Диацетиденген геллан шайырының құрылымы
Геллан Pseudomonas elodea бактериясы жағынан түзілетін сыртқы жасушалық полисахаридтердің жалпы атауы. Канеко және Каң бұл полимерді АҚШ-тың Калифорния штатының Келько Мерк лабораториясында 1978 жылы ашқан болатын [6] . Ол бастапқыда S-60 немесе PS-60 деген аттармен белгілі болған. Геллан түзетін микроорганизим Элодия өсімдігінің ұлпаларынан бөлініп алынады. Зерттеу нәтижелері ол бактерияның Pseudomonas тәріздес екенін анықтап, кейін келе Pseudomonas elodea деп атайтын болды [12] . 1994 жылы геллан түзетін бактерияның Sphingomonas paucimobilis екені анықталып, Proteobacteria класына жатқызылды [7] . Гелланның токсикалық қасиеттері 1988 Жапония да зерттеліп, оны тағам ретінде қолнануға болатындығы ұсынылды. АҚШ-та гелланды тағам өнімдері ретінде қолдануға 1992 жылдан бастап рұқсат етілген [8] .
Әр түрлі типтегі геллан шайырларының құрамы. Геллан полисахариді β-D-глюкоза ( D -Glc), L -рамноза ( L -Rha) және D-глюкон қыщқылынан ( D-GlcA) құралады. Қоспа шамамен 60% глюкоза, 20% рамноза және 20% глюкон қышқылынан тұрады. Одан бөлек, көп мөлшердегі полисахарид емес заттар да геллан құрамынан табылады. Оларды филтрация немесе центрифугация әдістері арқылы бөліп алуға болады [13, 14] .
Геллан шайырының биосинтетикалық жолы. Көптеген ғалымдар тетрасахаридтердің қосарланған тізбектерін Sphingomonas paucimobilis арқылы синтезделу жолымен зерттеді [15, 16] . Вертак геллан шайырының екі түрін Sphingomonas paucimobilis биосинтезін және polyhydroxybutyrate (PHB) жабайы түрін зерттеді. Sphingomonas paucimobilis глюкозасы Embden-Meyerhof жолы арқылы немесе пентоза фосфат жолы арқылы жүреді. Embden-Meyerhof жолы глюкоза дегидратациясында айтарлықтай роль атқармады, себебі ол фосфофруктоза активтілігінің есебінен болады, ол глюколиздегі негізгі фермент [16] болып табылады.
Глюкозаның дегидратацияланудан бұрын жасушаға кіруі мүмкін болатын жол деп қарастырылған. Ол төмендегі жолдардың бірімен жүзеге асуы мүмкін:
glucose out → glucose in → gluconate →
→ gluconate-6-phosphate
немесе
glucose out → gluconate-6- phosphate in →
→ gluconate-6-phosphate
Мартинз бен Са-Корреиа гелланның қайталанған полисахаридті тізбектерінің синтезделуінің мүмкін болатын жолдарын анықтады, олар геллан синтезі қайталанған тізбектер түзілуден бұрын соған ұқсас белсенді топтар, экзополисахаридтердің микроағзалардың клеткасында синтезделгені сияқты болуы керек деп топтастырды [15] .
Геллан ізбасарлары ферменттерді анализдеу арқылы анықталып нуклеотид фосфат қанттары, яғни UDP -глюкоза, TDP-рамноза және UDP-глюкон қышқылдары екені анықталды. Мүмкін болатын синтезделу жолы 2- суретте көрсетілген.
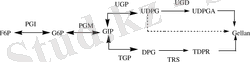
Сурет 2 - Геллан биосинтезіне қатысатын нуклеотид қанттары ізбасарларының түзілуінің жобаланған жолы
Глюкоза-6-фосфаты бұл екі жолдың басталуында шешуші рөль атқарады. Оның бірі уридин-5-дифосфат глюкоза (UDPG) болса, екіншісі тимин-5-дифосфат глюкозаның (TDPG) түзілуіне әкеледі. Сәйкесінше, UDPG D-глюкоза мен D-глюкоза қышқылы және TDPG синтезіне қатысып, прамнозаның синтезделуіне әкеледі. Бұл үш қосылыстың қоспасы геллан синтезделуінің нәтижесінде жүзеге асады [17] . Бірақ бұл үш мономердің қосарлануы толықтай зерттелмеген.
Табиғи геллан шайыры қосарласқан b-1, 3- D-глюкоза, b-1, 4- D-глюкон қышқылы, а-1, 4- L-рамноза, екі акрил группасы, ацетат және глицерат тізбектері глюкон қышқыл қалдығымен тізбектелген [14] . Табиғи геллан шайырындағы ацетил группалары сілтілермен өңдеу арқылы табиғи геллан шайырынан бөлініп, деацетилденген геллан шайырын түзеді. Ацил орынбасарлары табиғи гелланның реологиялық және деацилдену қасиеттеріне көп әсер етіп табиғи гелланның жұмсақ, эластик және жылуда ыдырайтын қасиеттері қатты, морт және жылуға төзімді қасиеттерге қарай өзгереді [18] . Табиғи гелланды деацилдеу барысы төмендегідей жүреді [18, 19] . Алдымен ерітінді қайнап жатқан суға 15 мин бойы шыланып, сосын қайта суытылып 1. 0 M NaOH мен pH 10. 0-ға арыттырылады. Сосын ерітінді 80 °C та 10 мин қалдырып 1. 0 M HCl мен pH 7. 0-ге түсіріледі. Масса центрифугада 8000 prm 4°C 30 мин айналдырып сүзіледі. Сүзіндіге үш есе көлемде суық спирт құйылып, деацилденген гелланда тұнбаға түсіреді. Тұндырылған геллан пеште 80°C-та 12 сағат бойы кептіріледі [20] .
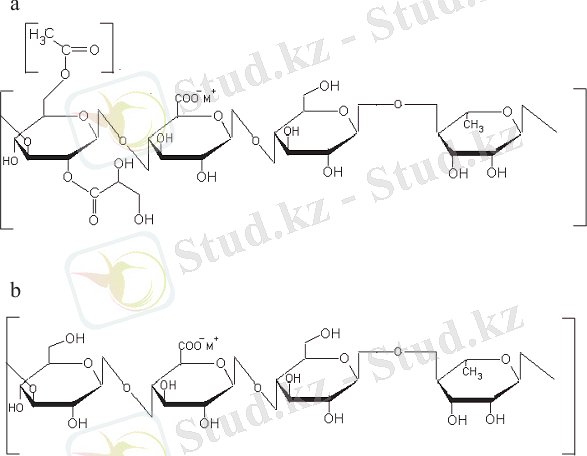
Сурет 3 - Қосарланған тізбекті табиғи (a) және деацилденген (b) гелланның химиялық құрылымы

Kg-a- кетоглутамат; Glc-DH- глюкоза дигидрогеназа; Glc-K- глюкоза кинеза; Gln-K- глюконат киназа; IC-DH- изоцитрит дигдрогенеза; G6PD- глюкоза-6-фосфатдигидрогеназа, TCA- трикарбоксил қышқылы циклы; KDPG- 2-кето-3-деокси-6-фосфоглюконат; Pg- фосфоглюконат; Pgm- фосфоглюкомутаза; G3P-DH- глцеральдегид-3-фосфат дегидрогеназа;
Сурет 4 - Глюкозаның S. Paucimobilis бактериясы арқылы ыдырауының мүмкін болатын жолы
Гелланың гель түзілуі кезінде параллель қатарлардан тұратын реттелген аймақтар (блоктар) пайда болады [21-22] .
а б
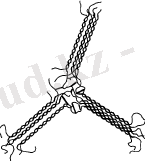

Сурет 5 - Өздігінен тігілген геллан: а-агрегаттағы қос тізбектің байланысы, б - гидрогельдің молекулалық моделі (блоктың сипаттамасы: ұзындығы 12, 48 нм; ені 4, 05 нм; биіктігі 8, 46 нм) .
Геланның гель түзілу механизимі туралы көптеген әдебиеттерде жазылған. Алайда, жоғары температура әсерінен термоқайтымды конформациялық бір құрылымнан екіншіге ауысу жүреді деген ұқсас пікірлер де бар [23] .
Суыту
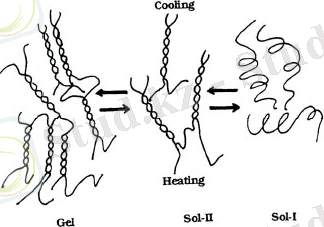

Қыздыру
Гель Зол-II Золь-I
Сурет 6 - Бір валентті катионның қатысымен және қатысынсыз геланның золь-гельге ауысу сызба-нұсқасы
Жоғарғы температурада гелланның макромолекулалары бос шумақталған күйде болады (золь-I) . Салқындатқан кезде геллан тізбектері қосарланған спираль және реттелген құрылым түзумен сипатталады. Алайда, мұндай реттелген құрылым тор түзілуге алып келмейді ( золь-II) . Гель түзілу тек катион қатысында ғана жүреді. Бұл золь-гель фазалық ауысу температурасының спираль-шумақ конформациясының температурасынан төмен болатындығына байланысты. Бірақ екі түрлі ауысу тудыратын ( золь-I, золь-II және гель) геллан үшін суыту және қыздыру кезінде болатын термиялық гистерезис құбылысы тән емес. Қосылған тұздың концентрациясын көбейткен сайын спираль-шумақ және золь-гель ауысу арасындағы температуралық айырмашылық азайып отырады. Гелланның сулы ерітіндісі 30-35 0 C температурада гельге ауысады, ал 90 0 C температурада балқиды.
Ацильдік топтардың болуына байланысты геллан екіге бөлінеді: төмен ацильді және жоғары ацильді. Жоғары ацильді формадан иілгіш және сынғыш емес, ал төмен ацильдіден қатты, сынғыш және иілмейтін гель алынады [24] . Жоғарыда айтып өткендей катион қатысында геллан гельге айналады [25-26] . Мысалы, натрий катионы қатысындағы гель түзілу гелланның молекулалық массасын анықтау үшін қолданылады. Натрий катиондары қажет емес агрегацияны болдырмауға және микрогельтүзілуге қатысады да молекулалық массаны анықтауға кедергі келтірмейді. Екі валентті катион қос спиральдің пайда болуына себепші болады [27] . Геллан шайырының ерітіндісіне хелаттаушы агенттерді қосу гель түзілудің температурасын жоғарылатады, бірақ алынған гельдің реологиялық қасиеттерін арттырады.
Геллан қазіргі кезде Жапония және АҚШ-тың Kelco компониясымен өндіріледі. Өнім төрт түрлі және мынадай атаулармен шығарылады: Келкогель (геллан шайыры), Гельрит (К + иондарымен), Фитогель және Гель Гро [28] . Келкогель тамақ өнеркәсібінде қоюландырғыш, эмульгатор және тұрақтандырғыш ретінде қолданылады. Қоспалардың номенклатурасында оның номері E418. Қалган үш түрі микробиологияда агар агардың алтернативасы ретінде қолданылады.
- Реологиялық анализ және молекулалық қасиеттері
Реология (грек тілінен rheos - ағын) - заттың деформациясы мен ағуы туралы ғылым. Реологияның зерттеу пәні - кернеуге тәуелді деформацияның түрлері болып табылады. Реология әр түрлі тұтқыр және пластикалық массалардың ағуымен, қайтымсыз қалдықты деформациямен байланысты үрдістерді, сонымен қатар кернеу релаксациясы құбылыстарын және т. б. қарастырады.
Әдетте реологияны материалдың деформациясы мен аққыш күйдегі қасиеттерін зерттейтін ғылым ретінде анықтайды. Полимерлерді өңдеудің теориясы олардың реологиялық қасиеттеріне негізделген, себебі полимерлердің табиғаты мен молекулалық массасына байланысты әртүрлі температура мен деформациялану режимінде алынған мәліметтер олардың қасиеттері, құрылысы және құрылымы жөнінде маңызды ақпарат береді. Мұндай реологиялық зерттеулер сан алуан өндірістік процестердің технологиясында, және әр түрлі жобалау және конструкциялық жұмыстарда пайдаланылады. Реологияның негізіне сүйеніп жоғары сапалы бұйымдар алуды қамтамасыз етуге болады. Реологияның жаңа әдістері сұйықтықтан қатты денеге ауытқитын шегі бар консистенциялы заттардың құрылымын зерттеуде қолдануға болады [29-30] .
Полимерлердің реологиялық қасиеттері негізінен оның тұтқырлығына байланысты. Тұтқырлық жүйеге түсірілген ығысу кернеуі мен одан туатын ығысу жылдамдығының арасындағы байланысты сипаттайды. Деформациялану жылдамдығына тәуелсіз тұрақты температура мен қысымда кернеудің ығысу жылдамдығына қатынасы динамикалық тұтқырлыққа тең болып, Ньютон заңына бағынатын кез келген жүйелер Ньютондық жүйелер деп аталады. Оған көбінесе төмен молекулалы сұйықтар жатады. Жылулық қозғалыстың салдарынан мұндай сұйықтың құрылымы үздіксіз тез бұзылып және қайтадан қалыптасып үлгіріп тұрады да, іс жүзінде сыртқы әсерлер бұл үрдіске айтарлықтай әсер етпейді. Сондықтан қалыпты кернеу мен ығысу жылдамдығында сұйықтықтар құрылымының өзгерісі байқалмайды. Реологияның жаңа әдістерін сұйықтықтан қатты денеге ауытқитын шегі бар материалдардың құрылымын зерттеуде қолдануға болады. Сұйықтыққа қосымша күш салу оның ағуына алып келеді. Егер бұл күшті жойса, онда сұйықтық өзінің бастапқы қалпына келмейді - ол тұрақты деформацияға ұшырайды. Қатты дененің сыртқы күшке жауап беру реакциясы оның эластикалық немесе пластикалық болуына байланысты [29] .
Барлық аққыш заттардың тұтқырлықтарының қозғалыс кернеуіне тәуелділігі немесе тәуелсіздігінің белгісіне қарап, ньютонды және ньютонды емес деп бөледі. Ньютонды деп тұтқырлық қозғалыс кернеуіне тәуелсіз, яғни Ньютон заңына тұрақты коэффицент болатын материалдарды айтамыз. Ньютонды емес деп тұтқырлық қозғалыс кернеуіне тәуелді, яғни деформация ығысу жылдамдығының функциясы болып табылатын материалдарды айтамыз.
Геллан өндіру кезіндегі ферменттелген сұйықтық, тіпті 0. 1% болған кезде де (көлемдік масса бойынша) псевдопластикалық реологиялық қасиеттер көрсетеді. Бастапқыда ерітінді тұтқырлығы Ньютондық сұйықтықтардай болып тұтқырлығы суға жақын болады, бірақ ерітінді тұтқырлығы кенет артып Ньютондық емес сұйықтықтардай болып сұйықтану қасиеттері болады. Бұл псевдопластикалық қасиеттері экзополисахаридтер фазасының жиналуы кезінде микробиологиялық полимерлердің түзілуіне ортақ қасиет болып табылады. Ол мынадай теңдеумен бейнеленеді:
Мұнда: -ерітінді тұтқырлығы, -қабат реті, Бұл модельде екі тәуелсіз параметр бар: қабаттың азаю индексі (Ньютондық сұйықтықтар үшін 1 және қабаттың жұқару дәрежесінің артуына байланысты 0-ге дейін төмендейді) және тұрақтану индексі k. Древетон және т. б. [31] индекс n-ның бастапқы 9 сағатта 1 ден 0, 30 айналасында тез төмендейтіндігін, сосын тұрақтанатынын байқаған. Ал k шамасы полимер концентрациясы өскен сайын артып отырады. Геллан катион қатысында қыздырғанда не суытқанда дереу гель түзеді. Бұндай ерітінді-гель өзгерісі, фаза алмасу өзгерісі негізінде қарауға болады. Гелланның гельдену барысы полимер концентрациясына, температураға және ерітіндідегі моновалент пен диваленттік катиондардың шамасына байланысты [32] . Төмен температурада ол ретті екі айқасқан спираль түрінде болады, ал жоғары температурада бір айқасқан полисахарид түзеді, яғни ерітінді тұтқырлығын айтарлықтай төмендетеді. Фаза алмасу температурасы шамамен 35°C, бірақ 30-50°C аралығында деп айтылады, себебі осы аралықта фазааралық алмасу байқала бастайды. Күй алмасу температурасынан төмен температурада қатты құрылым алынады, нәтижеде гель түзеді.
Гель түзу барысының үрдісін гелланның екі айқасқан орамдары агрегаттанып, екі айқасқан сегмент түзіп, катион және сумен сутектік байланыс түзу салдарынан үш-өлшемді торлар түзуімен түсіндіруге болады [33] . Гель түзу барысында моновалент немесе дивалентті катиондар қосу тізбектер байланысқан аумақта көптеген тұз көпіршелерін түзіп гельдену барысын арттырады. Әр түрлі факторлардың гельдің беріктігіне әсерін зерттеу үшін бірнеше зерттеулер жүргізілді. Кейбір гельденуге әсер ететін маңызды факторлар төменде баяндалады.
Ацетил гельденуге әсер ететін ең негізгі фактор болып табылады. Гелланның әр түрлі ацетил құрамдарының қасиеті әр түрлі болып келеді. Табиғи геллан шайыры жұмсақ, созылғыш және өте әлсіз болып табылады, себебі ацетил және глицерил топтары геллан полимер тізбектерінің жақын ассоциялануына кедергі болып, тығыз айқасқан екі спираль түзуін қиындатады. Деацилденген геллан ацетил және глицерил топтары болмағандықтан берік, морт, жылуға қайтымды болып келеді [34] .
Кесте 1 - Жоғары және төмен ацилді гелланның физикалық қасиеттерін салыстыру
Тек суыту
(катиондар керек емес)
Иондардың гельдің беріктігіне және морттылығына әсері үлкен. Геллан ионсызданған суда гель түзбейді, бірақ кальций, калий, натрий және магний тұздарының қосылуы бұл екі қасиетін өзгертеді [20] . Екі валентті катиондарда гельдену процесі оңай байқалады; тіпті геллан гелі өте төмен концентрацияда (0, 2% массасы бойынша әр көлемде), өте жоғары беріктік 0. 004% (массасы бойынша әр көлемде) кальций және 0. 005% (массасы бойынша әр көлемде) магний болғанда байқалады, сондай-ақ 0. 16% натрий немесе 0. 12% калий (массасы бойынша әр көлемде) болғанда да жоғарыдағыға ұқсас беріктік байқалады [35] . Геллан гелі KCl немесе NaCl тіпті жоғары концентрациясында (1% массасы бойынша әр көлемде) да төмен беріктік түзіледі [18] . Гелланның 0. 1-0. 2% концентрациясы көптеген тағамдық жүйелер үшін ыңғайлы.
Сандерсон және Кларк [36] гель беріктігін pH-3, 5 және 8 арасында ең жақсы деп көрсетті, ол табиғи тағамдардың pH аумағына сәйкес келеді. pH-тың өзгеруі гельдің шөгу нүктесін өзгертпейді, бірақ кейде балқу темперетурасына әсер етеді. Мысалы, гель моноваленті ионның төмен концентрациясында дайындалып pH бейтарап ортада балқу температурасы 70°C болады, бірақ pH=3, 5 болғанда балқу температурасы аздап артады. Бұл жағдай дивалентті иондарда байқалмайды.
Сахароза сияқты гидрофильді қоспалар (10% массасы бойынша әр көлемде) геллан гелінің беріктігіне қажетті ион коцентрациясын төмендетеді [37] . Касапис және т. б. [38] электрон тасымалдағыш микроскоппен полисахарид топшаларының табиғатының өзгерісін қанттың өсуімен байланыстыра зерттеді. Деацилденген геллан (<1%) қоспасының төмен (0-20%) және жоғары (80-85%) қант мөлшерінде дайындалып зерттелген. Жоғары қант/геллан гелінің микрографтары оның суу барысында алмасатын пластикалық күйден шыны тәріздес күйге алмасуын көрсететін полисахарид торларының айқасуының азайғандығын көрсетеді. Тангет және т. б. [39] фруктоза мен сахарозаның гельдену температурасына, мөлдірлігіне, натрий және кальций тігілген гелланның құрылымына әсерін зерттеген. Олар геллан ерітіндісінің гельдену температурасының сахароза қосылуынан артатындығын, ал фруктозаның қосылуы 35% (массасы бойынша әр көлемде) ешқандай өзгеріске ұшыратпайтындығын баяндайды. Фруктоза мен сахарозаның бірдей қосылуы гель мөлдірлігін жоғарылатады. Сахарозаның гель беріктігіне әсері катион концентрациясына тәуелді екені анықталған. Катионның төмен концентрациясында сахароза гельді беріктендіреді, ал жоғары катион консентрациясында сахароза гельді әлсірететіндігі байқалған.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz