Морфолинсірке қышқылының гидразиді мен N-бензоил, фенил және (п-нитро)-фенилгидразон туындыларын синтездеу және құрылысын ИҚ-спектроскопия әдісімен зерттеу


РЕФЕРАТ
Дипломдық жұмыc 59 беттен, 7 cуреттен, 2 кеcтеден, 30 пaйдaлaнылғaн әдебиеттен тұрaды.
Жұмыстың мақсаты: Морфолин негізінде жаңа гидразид туындыларын синтездеу, және реакциялық қабілеттілігі мен құрылысын зерттеу болып табылады.
Жұмыcтың міндеттері:
1) Морфолинсірке қышқылы гидразидін синтездеу;
2) Морфолинсірке қышқылының N-бензоилгидразиді синтезі;
3) Морфолинсірке қышқылының фенилгидразоны синтезі;
4) Морфолинсірке қышқылының (п-Нитро) -фенилгидразоны синтезі;
5) Синтезделген қосылыстарды идентификациялау.
Зерттеу әдіcтері: ИҚ-спектроскопия, жұқа қабатты хроматография, қайта кристалдау.
Aлынғaн нәтижелері: Бұл дипломдық жұмыста морфолинсірке қышқылы этилэфирі негізінде морфолинсірке қышқылының гидразиді синтезделді және потенциалды активті морфолинсірке қышқылы гидразидінің жаңа туындылары алынды. Атап айтқанда, морфолинсірке қышқылының N-бензоилгидразиді, морфолинсірке қышқылының фенилгидразоны мен (п-Нитро) -фенилгидразоны синтезделіп алынды. Синтезделген қосылыстардың құрылысы ИҚ-спектроскопия әдісімен дәлелденді.
Практикалық маңыздылығы: Жаңа биологиялық активті заттарды алу мақсатындағы перспективті модельді қосылыстар гидразидтің туындылары болып табылады.
Алынған қосылыстар алыну әдісі жеңіл болып табылады және жоғары биологиялық активтілік көрсетеді деп күтілуде. Алдағы уақытта биологиялық белсенділігін зерттеуді қажет етеді.
Басылымдары: Дипломдық жұмыстың нәтижелері «Ғылым әлемі» (2013ж), «әл-Фараби әлемі» (2014ж) атты конференцияларда бaяндaмa тезиcтері бaяндaлды, сондай-ақ, «Студенттердің бизнес-инкубаторлар инновациялық жобалар көрмесінде» ұсынылды.
РЕФЕРАТ
Дипломнaя рaботa cоcтоит из 59 лиcтов, 30 иcпользовaнных иcточников, cодержит 7 риcунков, 2 тaблицы.
Цель рaботы: Синтезировать новые производные гидрозида на основе морфолина, и исследовать реакционные способности и структуру.
Зaдaчи рaботы:
1) Синтез гидразида морфолинуксусной кислоты;
2) Синтез N-бензоилгидразида морфолинуксусной кислоты;
3) Синтез фенилгидразон морфолинуксусной кислоты;
4) Синтез (п-Нитро) -фенилгидразон морфолинуксусной кислоты;
5) Идентификация синтезированных соединении.
Методы иccледовaния: ИК-спектроскопия, тонкослойная хроматография, перекристаллизация.
Полученные результaты: В результате дипломной работы на основе этилового эфира морфолинилуксусной кислоты был получен гидразид морфолинилуксусной кислоты и получены новые производные потенциально активного гидразида морфолинуксусной кислоты. Полученные соединения: N-бензоилгидразид морфолиноуксусной кислоты, фенилгидразон и (п-Нитро) -фенилгидразон морфолиноуксусной кислоты. С целью установления строения соединения проведен анализ с помощью ИК-спектроскопии.
Прaктичеcкое значение: Перспективными модельными соединениями в поиске новых биологически активных веществ являются производные гидразидов.
Способы получения полученных соединении являются легкими и ожидается, что покажет высокую биологическую активность. В будущем требуется исследовать биологическую активность.
Публикации: Результаты дипломной работы опубликованы в конференциях «Мир науки» (2013г), «мир аль-Фараби» (2014г), а так же, представлены на «Выставке бизнес-инкубатор инновационных проектов студентов».
ABSTRACT
Diploma work consists of 59 pages, 7 figure, 2 tables and 30 references applications.
Purpose: Synthesis of new derivatives of morpholine and study the reactivity of the obtained compounds.
Objectives of the work:
1) Synthesis of acetic acid hydrazide morpholinе;
2) Synthesis of benzoyl hydrazide of morpholinе acetic acid;
3) Synthesis of phenylhydrazoneof morpholinе acetic acid;
4) Synthesis of (p-nitro) -phenylhydrazoneof morpholinе acetic acid;
5) Identification of the synthesized compounds.
Used methods and equipments: IR spectroscopy, thin layer chromatography, recrystallization.
Obtaining results: As a result of the diploma work on the basis of ethyl ether of morpholinyl acetic acid the hydrazide of morpholinyl acetic acid was got and the new derivatives of hydrazide of morpholinyl acetic acid and synthesized new derivatives potentially active hydrazide morpholine acetic acid. Namely, were synthesized N- benzoylhydrazide morpholineacetic acid phenylhydrazone morpholineacetic acid (p-nitro) phenylhydrazone. To establish the structure of the compound analysis of infrared spectroscopy was used.
Practical use: A promising model compounds in the search for new biologically active compounds are derivatives of hydrazides.
Methods for preparing the compound obtained are light and are expected to show high bioavailability. In the future, you want to explore the biological activity.
Source: The results of the thesis published in the conference "World of Science" (2013), "the world of al-Farabi" (2014), as well as, presented in the "Exhibition of the business incubator of innovative projects of students. "
МАЗМҰНЫ
КІРІСПЕ
Жұмыстың жалпы сипаттамасы. Бұл жұмыста морфолинсірке қышқылының жаңа туындылары синтезделді. Кейбір физико-химиялық параметрлері анықталды. ИҚ-спектроскопия әдісімен құрылыстары анықталды.
Жұмыстың өзектілігі: Өндірістік қолжетімді реагенттер негізінде жаңа биологиялық белсенді заттарды алу және іздестіріп табу. Базисті қосылыстар арасында биологиялық белсенді қосылыстарды синтездеуде азотты гетероциклдердің, яғни морфолиннің алатын орны ерекше.
Ғылыми жаңалығы: Алғашқы рет морфолин негізінде морфолинсірке қышқылының N-бензоилгидразиді, морфолинсірке қышқылының фенилгидразоны және (п-Нитро) -фенилгидразоны синтезделіп алынды.
Практикалық маңыздылығы: Қазіргі кезде микробқа қарсы белсенділігі бар химиялық қосылыстарды іздестіруді қосылыстың құрылысын жорамалдайтын ғылыми ұстанымдар мен сандық есептеулерге негізделіп, мақсатты синтез арқылы жүргізеді. Ғылыми зерттеулердің дамуына орай, бұл облысқа байланысты бірнеше бағыт бар, соның ішінде молекулаға фармакофорлы фрагментті енгізу болып табылады. Бұндай фрагменттерге гидразидтік топты жатқызуға болады. Гидразидтік қызмет атқаратын орынбасарлары бар азотты гетероциклдер практикалық пайдалы заттар синтезінде ыңғайлы синтон болып табылады. Гидразондар алыну әдісі жеңіл және биологиялық активтілігі алуан түрлі болғандықтан синтетикалық органикалық химияда кең қолданылады. Гидразид туындылары медициналық өндірісте туберкулезге қарсы, ісікке қарсы, гипотензивті, депрессияға қарсы, психотерапевті және басқа да қасиеттер көрсететін физиогиялық активті зат ретінде қолданылады. Осыған байланысты гидразид туындыларына назар аударып, гидразондар синтезіне ерекше қызығушылық білдірдік.
Ғылыми мәселенің шешу жолдарын бағалау : Гидразид пен гидразид туындыларын синтездеу және оларды зерттеу жұмыстары көптеп жүргізілген. Гидразондар алыну әдісі жеңіл және биологиялық активтілігі алуан түрлі болғандықтан синтетикалық органикалық химияда кең қолданылады.
Қазақстанда аминсірке қышқылдарының туындыларын зерттеу саласында жұмыстар Бектуров А. Б. атындағы химиялық ғылымдар институтында жүргізілуде. Сонымен қатар, әл-Фараби атындағы ҚазҰУ, органикалық заттар, табиғи қосылыстар және полимерлер химиясы мен химиялық технологиясы кафедрасында бірнеше жылдар аралығында Ахмедова Ш. С. басшылығымен осы бағытта көптеген жұмыстар жүргізілген.
Жұмыстың мақсаты: Морфолин негізінде жаңа гидразид туындыларын синтездеу, және реакциялық қабілетілігі мен құрылысын зерттеу болып табылады.
Жұмыcтың міндеттері:
1) Морфолинсірке қышқылы гидразидін синтездеу;
2) Морфолинсірке қышқылының N-бензоилгидразиді синтезі;
3) Морфолинсірке қышқылының фенилгидразоны синтезі;
4) Морфолинсірке қышқылының (п-Нитро) -фенилгидразоны синтезі;
5) Синтезделген қосылыстарды идентификациялау.
Зерттеу нысаны: Морфолинсірке қышқылы гидразиді, морфолинсірке қышқылының N-бензоилгидразиді, морфолинсірке қышқылының фенилгидразоны, морфолинсірке қышқылының (п-Нитро) -фенилгидразоны.
Басылымдары: Дипломдық жұмыстың нәтижелері «Ғылым әлемі» (2013ж), «әл-Фараби әлемі» (2014ж) атты конференцияларда бaяндaмa тезиcтері бaяндaлды, сондай-ақ, «Студенттердің бизнес-инкубаторлар инновациялық жобалар көрмесінде» ұсынылды.
1 ӘДЕБИ ШОЛУ
1. 1 Гидразондардың алыну әдістері
Гидразондарды алудың ең жалпы әдісі гидразиндердің карбонильді қосылыстармен конденсациясы болып табылады. Гидразиннің, моно-, диорынбасқан гидразиндердің альдегид пен кетонмен әрекеттесуінің зерттелуі аналитикалық формаларды алудың оңтайлы жағдайын таңдау мақсатында болды. Ал механизмі кейінірек зерттеле бастады. Механизмнің зерттелуі карбонилді қосылысты бөлу мен анықтауда жиі қолданылатын семикарбазондар үлгісінде жүргізілді. Соңғы жылдардағы жұмыстарда бекітілгендей, суды ығыстырып, гидразон беретін гидразинокарбинол түзілуімен жүретін гидразиннің оксотопқа қосылуымен конденсация басталды. 1-сатыда протон гидразиннің азот атомынан карбонилді топтың оттегіне ығысады, 2-сатыда - екінші протонның элиминирленуі:
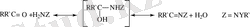
(1. 1)
Бұл реакциялар қайтымды, дегенмен тепе-теңдік орнауы кәдімгі жағдайда гидразонға қарай бағытталады, сондықтан тіпті судың реакциялық сферадан шығуы міндетті емес. Бірақ егер де сол бір карбонилді қосылыстың әр түрлі гидразиндармен реакциясының аяқталғандығын салыстырса, екі жағдайда да фенилгидразон түзілуі семикарбазонға қарағанда толық болады. Мысалы α-карвонның фенилгидразинмен реакциясының су-спиртті ортада тепе-теңдік константасы 6·10 -2 , ал семикарбазидпен - 3, 6·10 -2 тең. 2, 4-динитрофенилгидразон түзілгенде реакция қайтымдылығы байқалмады, оның себебі соңғының нашар еруіне байланысты.
Аралық карбинолгидразин түзілуін дәлелдейтін нәрсе - семикарбазидті карбонилді қосылыстардың бейтарап ерітінділеріне қосу УК және ИҚ-спектрлардағы карбонильді топқа тән жұтылудың тез төмендеуіне және ары қарай қайта пайда болған семикарбазонның жұтылуының баяу өсуіне әкеледі. Бұндай карбинолдың дегидратациясы реакция жылдамдығын анықтайтын қышқылдармен катализденеді, алайда қышқыл карбонильді қосылысты қосарланған қышқылға айналдырып, қосылысты жұмсартуы мүмкін. Қосылу сатысындағы тепе-теңдік дегидратацияға қарағанда тезірек орнайды, бейтарап және әлсіз негізді ерітінділерде конденсацияның жалпы жылдамдығы карбинолгидразиннің тепе-теңдік концентрациясы мен дегидратацияның жылдамдық константасы орындалуымен анықталады. Карбонильді компоненттің төмен концентрациясында жалпы жылдамдық екінші ретте болады, сол ретте дәл осы компоненттің жоғарғы концентрациясында карбинолгидразиннің концентрациясы үлкен болады, ал жалпы жылдамдық бірінші ретке қарай жақындайды. Сәйкесінше, әр түрлі нуклеофилділігі бар карбонильді қосылыстар жақын жалпы конденсация жылдамдығына ие бола алады [1] .
Гаммет «рН - семикарбазон түзілу жылдамдығы» графигінің максимумын былай түсіндіргенде екі қарама-қарсы эффекттің орын алатынын айтты: қосылу реакциясының жалпы қышқылдық катализі мен бос азотты негіздің қосарланған қышқылға айналғанда концентрациясының кемуі. Дженкс жылдамдықты анықтайтын сатының өзгеруіне максимум жазды: егер рН-тың орташа және жоғары мәнінде ол қышқылдармен катализденген карбинолгидразин дегидратациясы болса, ал қышқыл ортада жылдамдық-анықтаушы ретінде бос негіздің қосылу сатысы болады. Максимум гидразиннің рК а -на жақын рН-та болады, ал байқалған жылдамдықтың кемуі қышқыл концентрациясын арттырғанда реакцияға қабілетті нуклеофилдің концентрациясы кемігенде орындалады. Жылдамдықты анықтайтын сатының өзгерісі бақылаудағы аралық қосылыстың (бейтарап ерітінді) тепе-теңдік концентрациясының жылдамдығынан аралық қосылыстың (қышқыл ерітінді) тұрақты концентрациясына тәуелді жылдамдығына сәйкес келеді. Бұл өзгеріс бос негіздің қосарланған қышқылға айналғандағы қосылу жылдамдығының үлкеюі нәтижесінде орындалады. Карбинолгидразин түзілгендегідей тез дегидратталған рН-та аралық жағдайдың тұрақты концентрациясы орнайды да қосылу сатысы жылдамдық-анықтаушы болады. Дженкс «рН-жылдамдық» графигінің екі болжанған жылдамдық-анықтаушы сатыға арналып есептелген «рН-жылдамдық» графиктерінің қосындысында жақсы орындалатынын көрсетті. Бұндай интерпретацияның дәлелі ретінде әр түрлі жолдармен семикарбазонның түзілуі «рН-жылдамдық» қисығы максимумының екі жағы бойынша да карбонильді қосылыстың құрылысына байланысты. Карбинолгидразиннің дегидратациясы мен семикарбазонға судың қосылуы арнайы және жалпы қышқылдық катализге ұшырағанын келесі реакциядан (1. 2) байқауға болады:
Арнайы қышқылдық катализ:
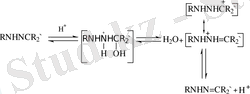
(1. 2)
Жалпы қышқылдық катализ:
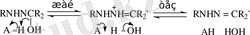 (1. 3)
(1. 3)
Гидраксиламиннің карбонильді топқа қосылуы арнайы қышқылдық катализге аз тәуелді: әлсіз негіздің, яғни семикарбазидтің қосылуы арнайы және жалпы қышқылдық катализге ұшырайды. Семикарбазидтің орынбасқан бензальдегидке қосылғандағы протондалған карбинолды аралық құрылыстың рөлі теориялық түсінікке сәйкес келеді. Қышқылдық катализдің болжанған механизмі семикарбазидтің бір реттік шабуылы мен протонның карбонильді топқа көшуінен тұрады [14] .
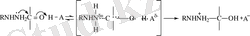
Семикарбазондардың түзілуі біріншілік ароматтык аминдердің нуклеофильдік катализіне де ұшыраған. Амин мен карбонильді қосылыстың әрекеттесуі, яғни Шифф негізінің түзілуі жылдамдықты анықтайтын саты болып табылады. Бұдан ары қарай семикарбазидтің Шифф негізіне қарай тез шабуылы басталып, нәтижесінде семикарбазон түзіледі. Шифф негізінің басқа да қайта аминдеу жағдайлары бар:
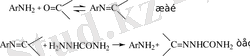
Екіншілік не үшіншілік аминдер емес, анилин қатысында озазон түзілуінің жылдамдығы артады. Бұл жерде де сол механизм орындалуы мүмкін. Азин, арилгидразон, ацилгидразон және т. б. түрлі карбонильді қосылыстартан алынатын гидразондар семикарбазонның түзілуі секілді жақсы зерттелмеген. Бірақ белгілі бір мәліметтер арқылы жоғарыда берілгендей механизм алуға болады. Мысалы, фенилгидразиннің қантқа әсері арқылы алынған озазон жалпы қышқылдық катализге ұшыраған. Қышқылдықты рН 5, 4-ке жеткенде жылдамдық жоғарылайды, ары қарай рН-қа тәуелсіз. Буферлі ерітінділерінің бірнеше концентрациясына сәйкес «рН-жылдамдық» графиктерінің экстратегістелуі буфердің нөлдік концентрациясында Н 3 О + арқылы келген аз катализді көрсетеді. Төмен рН-та арнайы қышқылдық катализдің болмауы келесіге нұсқайды: қышқыл ерітінділерде негіздің карбонильді топқа қосылуы - жылдамдықты анықтайтын саты болып табылады.
Карбонильді қосылыстармен конденсациясының салыстырмалы жылдамдығы гидроксиламин - семикарбазид - тиосемикарбазид қатарында төмендейді. Реакция жылдамдығының температуралық коэффициенті де осы ретпен кемиді, бұл берілген гидразиндердің салыстырмалы реакциялық қабілеті теңесетін температураның болғаны деген сөз [13] .
Семикарбазидтердің пара-орынбасқан ацетофенонмен конденсациясының жылдамдығы семикарбазидтің рК а -на сәйкес рН-та электронакцепторлық топты қосқанда артады. ρ=+0, 91болғанда жылдамдық коэффициентінің логарифмінің сызықтық корреляциясы ϭ Гаммет константасымен алынды. Реакциялық қабілеті жоғары кетондарда жоғарғы активтену энергиясы болады. 75%-қ этанолдағы бейтарап ерітіндідегі орынбасқан бензальдегид қатарының конденсациясы ϭ- ρ арақатынасына бағынбайды. Бұндай жағдайдағы жылдамдықты анықтайтын саты карбинолгидразин дегидратациясы болады. Пара-орынбасқан бензальдегидтердің семикарбазидпен реакциясының жеке сатыларында құрылысының жылдамдыққа және тепе-теңдік константаға әсерін Андерсон мен Джексон зерттеген. Бейтарап ерітінділерде жылдамдықты анықтайтын саты ретінде дегидратация болса, қосынды конденсация жылдамдығының коэффициенті карбинолгидразин түзілуінің тепе-теңдік константасы мен арнайы дегидратация жылдамдығының коэффициентінің туындысына тең. Карбинолгидразиннің түзілуі альдегидтегі электронакцепторлы орынбасарлармен жеңілдейді. Тепе-теңдік константасының логарифмі ρ=+0, 81 болғанда ϭ Гаммет константасымен сызықтық корреляцияда орналасады. Алициклды кетондардағы сақина мөлшері семикарбазидпен жүретін конденсация жылдамдығына үлкен әсер береді. Циклогексанон рН=7 шамасында циклопентанон мен циклогептанонға қарағанда реакцияға қабілеттірек боп шықты. Бұның себебін авторлар бастапқы заттағы көміртектің тригональды атомынан тетраэдрлік аралық қосылысқа ауысуында көрінетін сақинаның ішкі кернеуінде деп түсіндіреді. Алифатикалық, алициклдық кетондардың семикарбазидпен реакциясының активтену энтропиясы рН=7 кезінде карбонильді қосылыстағы кернеулі циклмен симбатты өзгереді. Тиосемикарбазидпен конденсация кезінде бұндай корреляция орын алған емес. рН=7 кезінде қосынды жылдамдықтың температуралық коэффициенті карбинолгидразин түзілудің бос энергиясын және карбинолгидразин дегидратациясындағы активтенудің бос энергиясын түзетіндіктен, интерпретация жүргізбес бұрын әр жылдамдық константасының температуралық коэффициенті бөлінген болу керек.
Семикарбазондар түзілуінің салыстырмалы жылдамдықтары карбонильді қосылыстар қатарында былай кемиді: циклогексанон - ацетон - циклопентанон - фурфурол - бутанон - пинаколин - ацетофенон. Өкінішке орай, фенилгидразондар түзілу механизмі анық зерттеліп жүргізілмеген және карбонильді қосылыстың құрылысының реакциялық қабілетімен байланысы анықталмаған. Стро озазон түзілуі кезіндегі орынбасқан фенилгидразиндердің реакциялық қабілетін тұнбаның түзілу уақытымен анықтаған. Фенилгидразиннің бензол сақинасындағы орынбасар реакциялық қабілетке әсер етпейтін болып шықты. Салыстырмалы реті қанттың құрылысымен анықталады. Әр гидразин - карбонильді қосылыс жұбы үшін әдетте бастапқы гидразиннің рК а мәніне жақын реакциялық ортаның оңтайлы рН мәні бар. Егер фенилгидразин сірке қышқылы қатысында оңай әрекеттессе, онда 2, 4 динитрофенилгидразин жақсы шығым шығу үшін минералды қышқылдардың қолданылуын талап етеді.
Гидразондар синтезіне көптеген әдістер мен әдістемелер қолданылады. Көбіне арасындағы ерекшеліктер қолданылатын еріткіштерге, катализаторларға, температалық жағдайларға, реакция ұзақтығына байланысты. Таңдалып алынатын жағдай бастапқы қолданылатын қосылыстар мен соңғы алынатын гидразонның қасиетіне байланысты. Арилгидразондар, семикарбазондар, тиосемикарбазондар және де көптеген арилгидразондар карбонильді қосылыстар ерітінділері мен гидразиндардың тікелей араласуынан-ақ алынады. Гидразин туындыларының сәйкес қышқылынан бірнеше тамшы немесе тұзының қосылуы процессті тездетеді. Еріткіш ретінде су, спирт, бензол, эфир, және т. б. қолданылады. Карбонильді қосылыстарды идентификациялауда 2, 4- қолдануды ұсынған Бреди күкірт қышқылы қатысындағы метанолды қолдануды ұсынса, Джонсон фосфор қышқылы қатысындағы этанолды, ал Паррик пен Расбур каталитикалық көлемдегі тұз қышқылы қатысындағы диметилформамидті не диметилсульфоксидті, Шайн каталитикалық көлемдегі тұз қышқылыны қосылған диглимді (диэтиленгликольдің диметил эфирі) ұсынды. Еріткіш, сонымен қатар катализатор ретінде диэтилфосфит қолдану ұсынылды. Ылғалдың ізі этилфосфорлы қышқылға (HO) 2 POC 2 H 5 дейін гидролиздейді де, ал ол өз кезегінде гидразон түзілу реакциясының катализаторы болып табылады. Гидразонды алкилгидразиннен алғанда конденсацияның басқа әдістерін пайдалануға тура келеді, көбіне тепе-теңдікті жылжыту үшін реакциялық ортадан суды шығарып тастау керектігі жиі кездеседі. Альдегидтер пен кетондардың әр түрі гидразиндермен әрқалай әрекеттеседі. Формальдегид пен гидразин қосылғанда полимер түзіледі, ол азот атмосферасындағы вакуумда қыздырғанда жоғары реакциялық қабілетімен ерекшеленетін формальдазин түзеді.
CH 2 O + N 2 H 4 → − [−CH 2 −N=N−] n − →H 2 C=NN=CH 2 (1. 4)
Формальдегид фенилгидразинмен аномальды әректтеседі. Формальдегид пен фенилгидразиннің әр түрлі жағдайларда алынатын оннан аса реакция өнімдері белгілі. 1968 жылы ғана Иоффе мен Стопский формальдегид фенилгидразонын катализаторсыз бастапқы қосылыстардан алудың эфирлі ерітіндідегі реакциясын сипаттады. Алдында алынған қосылыстардың құрылысы бірнеше рет зерттелген, сонымен қатар олардың фенилгидразонның басқа фенилгидразон молекуласымен немесе формальдегидпен қосылғанда
түзетін конденсация өнімі екені анықталған [12] .
Мысалы:
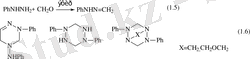
Формальдегидтің 4-нитрофенилгидразин мен 2, 4-динитрофенилгидразин мен конденсация өнімі - гидразон түзеді. Альдегид пен кетонның артық мөлшерінде карбонильді қосылыс гидразинмен қосылғанда кейіннен азинге айналуы мүмкін гидразон түзіледі.
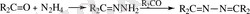 (1. 7)
(1. 7)
Бұл симметриялы және симметриялы емес азин алуға мүмкіндік береді.
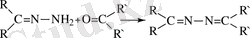 (1. 8)
(1. 8)
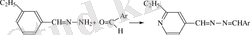 (1. 9)
(1. 9)
Гидразин мен оның туындылары сәйкес гидразондар шығу үшін альдегид пен кетондармен ғана емес, басқа да карбонильді тобы бар қосылыстармен қосыла алады: альдегид- және кетоқышқылдар, альдегид- және кетоспирттер, қанықпаған альдегидтер мен кетондар, қанттар және т. б. Дикарбонильді қосылыстар (диальдегидтер, дикетондар, кетоальдегидтер) гидразин мен оның туындыларымен сатылы әрекеттеседі: бірінші бір карбонильді топпен, кейін басқасымен.
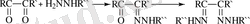 (1. 10)
(1. 10)
80%-к Этанолда тұз қышқылды гидразинмен бензилды 30минут қыздырғанда бензилдың моноазині былай түзіледі:
 (1. 11)
(1. 11)
Фенилглиоксальға 2, 4- әсер еткенде моно және дигидразондар түзіледі [7] :
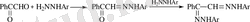 (1. 12)
(1. 12)
1, 3-, 1, 4- немесе 1, 5-Дикарбонильді қосылыстар гидразиндермен әрекеттескенде: а) полимер, б) екі молекула гидразин және екі молекула дикарбонильді қосылысы бар циклды қосылыс не в) бір молекула гидразин және бір молекула дикарбонильді қосылыстан тұратын циклды қосылыс түзіледі. Орынбасқан гидразиндерден моногидразондар, дигидразондар, ал кей жағдайда гетероциклды қосылыстар да түзіледі:
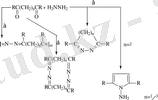
(1. 13)
Карбонильді қосылыстардың гидразиндармен реакциясының бағыты жәнетүзілген өнімнің құрылысы жүргізіліп отырған конденсация жағдайларына - бастапқы заттардың арақатынасына, реагенттердің концентрациясына, катализатордың табиғаты мен оның болуына, ортаның қышқылдығына, температура мен реакция уақытына байланысты.
Бұны флавонның гидразин және оның туындыларымен реакциясынан байқауға болады. Егер қышқыл және бейтарап ортада флавон гидразоны түзілсе, әлсіз сілтілік ортада 2-оксихалкон гидразоны түзіледі, ал күшті сілтілік ортада пиразолин туындыларына циклденеді [20] :
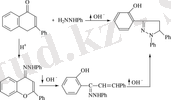 (1. 14)
(1. 14)
Гидразонның орнына, жағдайға сәйкес, циклды өнімдердің шығуы дикарбонильді қосылыстар кезінде ғана емес, сонымен қатар α, β-қанықпаған кетондар мен альдегидтер, β-галоидкетондар, β-диметиламинокетондар, β-оксикетондар және т. б. жағдайларда да орын алады. Әдетте, аралық түзілетін гидразондарды алу не идентифицирлеу мүмкін емес.
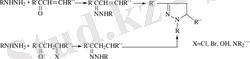
(1. 15)
α-галоид- және α-оксикетондар реакцияның құрылысы мен жағдайларына байланысты әр түрлі әрекеттеседі.
Гидразиндер мен арилгидразиндер қанттармен (альдоза, кетоза) гидразондар түзе алады, бірақ гидразиннің артық мөлшерінде озазондар түзіледі. Озазондар түзілу механизмі бірнеше рет талқыланған. Шемякин мен оның ғылыми тобы мәліметінше, озазондар α-оксикетондардан молекула ішілік тотықсыздандыру үрдісі нәтижесінде түзіледі.
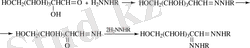
(1. 16)
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz