Уранды динамикалық ұңғымалық шаймалау кезінде орын алатын физико-химиялық үрдістерді зерттеу


КІРІСПЕ3
1 ӘДЕБИ ШОЛУ5
1. 1 Уран5
1. 1. 1 Уран туралы тарихи мағлұмат8
1. 1. 2 Уранның физика-химиялық қасиеттері9
1. 1. 3 Уранның спецификалық қасиеттері11
1. 2 Уранның физико-химиялық қасиеттері және қосылыстары12
1. 3 Уранның гипергенез қабатындағы күйі14
1. 4 Уранның комлекс түзу қабілеттері16
1. 5 Уранның химиялық технологиясы19
1. 6 Уранды өндірудің жер асты шаймалау әдісі20
1. 7 Жер асты сілтісіздендіру жүйелері21
1. 8 Жер асты шаймалаудің физико-химиялық ерешелігі22
1. 9 Уранды кен жыныстарын шаймалау25
1. 10 Қышқылды шаймалаудың артықшылықтары және кемшіліктері27
1. 11 Уранды шаймалау технологиясында тотығу-тотықсыздану құбылыстары27
1. 12 Қызылқұм кен орнының геолого-гидрогеологиялық ерекшелітері28
2 ТӘЖІРИБЕЛІК БӨЛІМ31
2. 1 Элементтік анализ31
2. 2 Статикалық жағдайда шаймалау31
2. 3 Шаймалау бойынша зертханалық тәжірибелерді орындау әдістемесі32
2. 4 Зерттелінетін кен үлгісінің гранулометриялық (түйіршікті) құрамын елеуіштік әдіспен анықтау33
2. 5 Өнімдік ерітінділерден ауыр металдар мөлшерін анықтау33
2. 6 Көміртек қостотығының, органикалық көміртектің, жалпы күкірттің, темір сульфаттары, сульфидтері мен қағынның мөлшерін анықтау33
3 НӘТИЖЕЛЕР МЕН ТАЛДАУЛАР35
3. 1 Элементтік анализ35
3. 2 Зерттелінген сынаманың сипаттамасы35
3. 3 Зерттелінген кен үлгісінің гранулометриялық құрамы36
3. 4 Кеннің минералдық құрамы. 36
3. 5 Сканерлеуші электронды микроскопия және жартылайсандық элементтік анализ38
3. 6 Зерттеу улгісін статикалық шаймалау47
3. 6. 1 Күкірт қышқылды шаймалау47
3. 6. 2 Карбонаттық шаймалау47
3. 7 Фильтрациялық колонналарда уранды шаймалау49
3. 7. 1 Сумен шаю сатысы50
3. 7. 2 Күкірт қышқылды шаймалау сатысы51
ҚОРЫТЫНДЫ56
ПАЙДАЛАНЫЛҒАН ӘДЕБИЕТТЕР ТІЗІМІ:58
КІРІСПЕГидрометаллургияда экономикалық және экологиялық тұрғыдан бүгінгі таңда ең тиімді уран өндіру әдісі болып табылатын жер асты ұңғымалық шаймалау мемлекетімізді атомдық энергетиканың негізігі отынын өндіруден дүние жүзінде бірінші орынға шығарды. 1954-ші жылдарда негізі қаланып, аз уақыт арасында дүние жүзінде кең қолданыс тапқан бұл әдіс, негізгі бөлігі аридтік зонада орналасқан Қазақ даласында, мемлекетіміздің гидрометаллургия өндірісі үшін таптырмас құралға айналды. Уранды жер асты ұңғымалық шаймалау әдісімен өндірудің өзіндік құны таулық әдісті қолдануға қарағанда 20-25%-ға төмен [1] . Бұл әдістің тағы бір айта кететін артықшылығы, таулық әдісті қолдану тиімсіз болып табылатын уран мөлшері 0, 01-0, 03%-ды құрайтын кендерді өңдеуге мүмкіндік беретіндігінде. Сонымен қатар, уран өндірудің қоршаған ортаға тигізетін кері әсері әлдеқайда азаяды. Жер асты ұңғымалық шаймалау әдісін қолданған аймақтарда жердің шөгуі және қопарылуы, бос жыныстардан және балланстан шыққан кендерден тұратын үйінділер болмайды. Уран қос тотығынның 100 кг өндіру кезінде 1 кг қатты қалдықтар түзіледі, ал таулық әдісте уран қос тотығының дәл сол мөлшерін алу үшін 100 000 кг қатты қалдықтар түзіледі. Оған қоса технологиялық үрдістен шаң-тозаң бөліну көздері жойылған, соның нәтижесінде атмосфераға бөлінетін радиоактивті заттардың көлемі біршама азайтылды. Жұмысшылар мен қызметкерлерге α-, β- және γ- сәулеленушілер әсері минималданған, өйткені уран радиоактивті отбасының жалпы γ-сәулеленуінің 98%-ы қышқылдық шаймалау кезінде жер астында қалатын радий және оның ыдырау өнімдеріне тиісті. Әдістің экологиялық, эконимикалық артықшылығы және технологиялылық кемшілігінің бірі негізгі кен түзуші жыныстардың жер астында шоғырланғандығында. Тек шаймалаушы агентпен әрекеттесетін кен жыныстарын көп жағдайда толық өңдеу мүмкін емес болып жатады. Сонымен қатар, жер асты ұңғымалық шаймалау әдісін қолдану барысында кен түзуші горизонттарының өткізгіштігі, шаймалаушы агентті таңдау, тотықтырғыштың тиімділігінің төмендігі не оның бағасының қымбаттығы сияқты үнемі туындап жататын мәселелер жеткілікті. Сондықтан жер асты ұңғымалық шаймалау әдісін зерттеу өзектілігін жоғалтпай, бүгінгі күнге дейін АҚШ, Франция, Ресей, Канада сияқты уран өндіруші алпауыттар осы салада үлкен зерттеу жұмыстарын жүргізуде.
Барланған уран кеніштерінің жер асты ұңғымалық шаймалау әдісімен өндіру мүмкіндігін анықтау мақсатында зертханаларда шаймалау үрдісін модельдеу сынақтары жүзеге асырылады. Технологиялық тұрғыдан бұл сынақтарға өте үлкен көңіл бөлінеді. Өйткені бұл сынақтар нәтижесі бойынша барланған кеніштен уран өндірудің максималды мөлшерлері, шаймалаушы агент сияқты технологиялық үрдісті жүзеге асыруға қажетті негізгі параметрлер толыққанды анықталады және осы үрдісті сипаттайтын математикалық модельдерді құрастыруға мүмкіндік береді.
Жоғарыда айтылғанның барлығын тұжырымдай келе, берілген жұмыстың мақсаты уранды динамикалық шаймалау кезінде орын алатын физико-химиялық үрдістерді зерттеу болып табылды.
Белгіленген мақсатқа жету барысында келесідей міндеттер қойылды:
- Тақырып бойынша басылымдық материалдармен танысу;
- Зерттеу объектісі болып табылатын уран кені үлгісінің негізгі геотехнологиялық сипаттамаларын анықтау;
- Уран кені үлгілерінен уранды статикалық жағдайда күкірт қышқылды және карбонаттық шаймалау;
- Уранды динамикалық шаймалау кезінде орын алатын негізгі физико-химиялық үрдістерді анықтау мақсатында сүзгіштік коллонкаларында шаймалау тәжірибесін жүргізу.
Зерттеу жұмыстары барысында алынған нәтижелер Ақбастау, Инкай, Қызылқұм уран кеніштерінде жүзеге асырылып жатқан технологиялық үрдісті жетілдіруде ұсыныстар дайындау кезінде үлкен үлесін тигізуі мүмкін.
Берілген зерттеу жұмысы Дүние жүзілік банктің «Практическое применение изотопных соотношений природных радионуклидов в гидрометаллургии урана и радиоэкологии» халықаралық ғылыми жобасы шебінде жасалған.
1 ӘДЕБИ ШОЛУ 1. 1 Уран
Уран табиғатта үш изотоптың 238 U, 235 U және 234 U қоспасы ретінде таралған. Табиғи радионуклидтердің табиғатта таралуы жайлы мәліметтер бірнеше жұмыстарда келтірілген. Солардың ішіндегі сенімдісі келесі кестеде көрсетілген Холденнің мәліметтері болып табылады [46] .
Кесте 1 - Уранның табиғи изотоптарының таралуы және ядролық қасиеті [46]
Жартылай ыдырау периоды,
Лет
2, 45·10 5
2·10 16
Α
СД
4, 777 (72 %)
4, 723 (28 %)
7, 037·10 8
3, 5·10 17
Α
СД
4, 397 (57 %)
4, 367 (18 %)
4, 468·10 9
8, 19·10 15
Α
СД
4, 196 (77 %)
4, 149 (23 %)
Бірақ, айта кететін жағдай, табиғи қосылыстардағы уран изотоптарының қатынасы өзгеруі мүмкін (абсолютті шамадан ±0, 1 % арасында) . 234 U изотобы 238 U изотобының радиоактивті ыдырауы кезінде пайда болатындықтан бұл екі изотоп бір-бірімен тығыз байланысты.
Уран табиғатта екі түрлі тотығу дәрежесінде кездеседі: +4 ([Rn] f 2 ) және +6 ([Rn] f 0 ) . Зертханалық жағдайда тұрақтылығы әлсіз U(III) және U(V) валентті қосылыстары алынған.
Уран (IV) өзінің қосылыстарында иттрийлі ауыр лантаноидтар тобы мен Th (IV), Y (III) химиялық қасиетіне жақын U 4+ ионы формасында болады. Химиялық тұрғыдан қарағанда U 4+ ионы әлсіз негіз болып табылады. Ол тек күшті қышқылды ерітінділерде кездеседі және ерітіндінің қышқылдығы төмендеген кезде U(OH) 4 түзе отырып гидролизденеді. U(OH) 4 гидроксиді суда аз ериді, бірақ қышқылдарда күшті ериді. UO 2 диоксиді іс-жүзінде 300 0 С-қа дейін сумен әрекеттеспейді, Тұз қышқылында (HCl) ерімейді, бірақ азот қышқылында (HNO 3 ) және қышқылдар қоспасында жақсы ериді. U(IV) қосылыстарының ішінде UCl 4 пен U(SO 4 ) 2 басқалардан қарағанда суда жақсы ериді. Осының себебінен U(IV) күштіқышқылды сульфатты, хлоридті және нитратты ерітінділерге тұрақты болады. U(IV) силикаттары күштіқышқылды ортада ерігіш болады.
U(IV) 8 координациялық санымен комплексті қосылыстар түзуге бейім келеді. U 4+ -тің карбонатты, сульфитті, оксалатты және де басқа комплекстері бар. Уранның комплексті қосылыстары қатарының тұрақтылық константалары келесі кестеде көрсетілген.
Уран буының атом спектрін зерттеуде оның негізгі жағдайының электронды құрылысы 5f 3 6d7s 2 екені анықталынды. Бұл мәлімет оның ауыр актиноидты элементтер тобына жатанын растайды. Уранның химиялық қаситеінің қиындығы оның энергетикалық деңгейлерінің (5а және 6d деңгейшелерінің) тым жақындығында.
Кесте 2 - Уранның комплексті қосылыстарының тұрақтылық константала- ры [46]
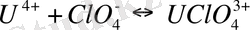

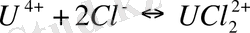


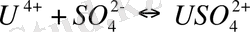
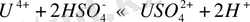

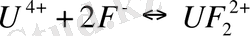
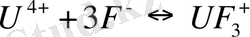
Уран (VI) - ауаның еркін қатысында ең тұрақты тотығу дәрежесіне ие болатын уран. U 6+ секілді ірі катион үшін оның алты валенттігі жоғары болып табылады. Ол энергетикалық тұрақсыз және сулы ерітіндіде көзді ашып-жұмғанша гидролизденіп, уранил UO 2 2+ екі валентті катионын түзеді. Уранилді топ UO 2 2+ - орталық атомнан тұратын және оған диаметральді қарама-қарсы екі оттегі атомынан құралған компактті сызықты қосылыс болып табылады. Мұндай қосылыстың максималды ұзындығы 6, 84 Å, ал минималды ұзындығы - 6, 04 Å, қалыңдығы - 2, 64 Å. UO 2 2+ -нің орташа иондық радиусы жуық шамамен 3, 22 Å -ге тең және табиғатта тараған көптеген катиондардың біразының радиустарынан едәуір жоғары. Осыған байланысты UO 2 2+ химиялық қосылыстарда изоморфты түрде басқа катиондарды өзіне қосып алып табиғатта өзінің жеке минералдарын түзеді (уранитит, настуран және т. б. ) .
U(VI) қосылыстары салыстырмалы түрде сулы ерітінділерде ерігіш және тұрақты болып келеді. Ең ерігіштерінің бірі уранил нитраты болып табылады. Суда жақсы ерігіштері уранил сульфаты мен оксигалогениді болып табылады. UF 6 мен UCl 6 ұшқыш болып келеді, бірақ су буының қатысында оңай гидролизденіп, оксигалогенидке айналады.
Органикалық қышқылдарда уранның көптеген тұздары ерігіш болып келеді. U(VI) - ның маңызды қиын еритін қосылыстары фосфаттар, арсенаттар және ванадаттар болып табылады.
U(VI) геохимияда маңызды рөл ойнайтын комплексті қосылыстар түзуге бейім келеді. Комплекстүзгіштік қабілеті мен түзілген комплекстің беріктігі туралы мәліметтерді төмендегі кестеден көруге болады.
Кесте 3 - [UO 2 ] 2+ уранил-ионының бейорганикалық лигандтты комлекс -терінің тұрақтылық константалары (25 0 С) [32]
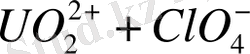
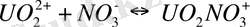
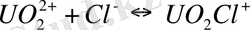
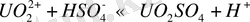
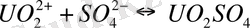
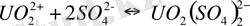
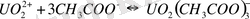
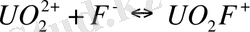
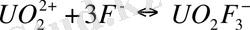
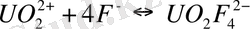
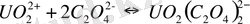

Табиғи жағдайларда карбонатты, сульфатты, фторидті, фосфатты және гидроксокомплексті комплексті қосылыстар маңызды мағынаға ие. Уранил ионымен комплекстүзу күшіне байланысты аниондар келесі кезекпен орналасқан:
бірзарядты: F - > NO 3 - > Cl - > ClO 4 - ;
екізарядты: CO 3 2- > C 2 O 4 2- > SO 4 2- .
Уранил аквагидрокомплекстері акватоптардың уранил акваионына [UO 2 (H 2 O) 6 ] 2+ сатылы түрде енуі нәтижесінде қалыптасады және [UO 2 (OH) n (H 2 O) 6n ] 2-n күйіндегі формада болады. Мұндағы n-нің мәні 0-ден 6-ға дейін өзгереді.
Карбонатты комплекстердің ішінде сулы ерітіндіде тек [UO 2 (CO 3 ) 3 ] 4- және [UO 2 (CO 3 ) 2 (H 2 O) 2 ] 2- комплекстері ғана тұрақты болады. Біріншісі ерітіндіде CO 3 2- иондары артық мөлшерде болғанда кездеседі, ерітіндіні сұйылтқан кезде екінші түріне өтеді.
Келесі саты суда әлсіз еритін уранил карбонатының UO 2 CO 3 түзілу сатысы болып табылады (3-сурет) .
Уранилдің фторидті комплекстері тек фтордың жоғары концентрациялары шоғырланған орталарда түзіледі. Уранилдің сульфатты комплексті қосылыстары құрылысы бойынша карбонаттыға ұқсас болып келеді, бірақ беріктігі бойынша тек қана карбонаттыдан ғана емес, сонымен қоса фторидті комплекстерден де кейін қалады.
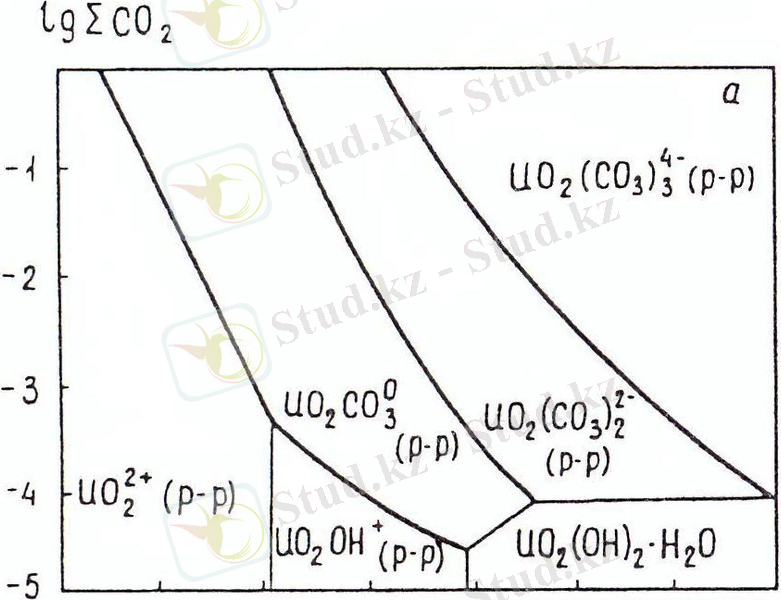
Сурет 1 - 25 0 С кезіндегі lg ∑CO 2 координатындағы әртүрлі уранил иондарының аудандарының қатынасы
1. 1. 1 Уран туралы тарихи мағлұмат1789 жылы Клапрот “смола кені” деген атпен белгілі ауыр қара кеннен жаңа элементті - уранды ашты, уран деген ат сол кезде жаңадан ашылған уран планетасының құрметіне қойылған.
Клапроттан кейін уранмен басқа да зерттеушілер айналысқан, бірақ ешкім таза металдық уран ала алмады. Тек 1891 жылы Пелиго уран хлоридін металдық натрий немесе калиймен тотықсыздандыру арқылы металдық уран алған.
ХІХ ғасырдың алғашқы жартысында уранның қасиеттері толығымен зерттелді, уранның тұздары шыны, фарфор және эмаль бояуларында өте жақсы сары түсті бояғыш екені анықталды.
1896 жылы Беккерель смолалық кенде радиоактивтілікті ашты. Осы уақыттан бастап уранның минералдарына назар көп бөлінді.
Содан соң Мария Склодовская-Кюри және Пьер Кюри смола кенінен радийды ашты. Уран тұздарын өндіруде өзгеріс болды: бұрын зауыт жұмысының басты мақсаты уран тұздарын өндіру болса, ендігі мақсат радийды өндіру болды, ал уран қосымша өнім ретінде алына бастады.
Радий әрқашан тек уранмен ғана кездеседі, кейде тек табиғи сулар құрамында радий жоғары концентрацияда урансыз кездеседі.
1 г радий өндіру үшін жуық шамамен 4 т таза уран смола кенін өңдеу керек. 1896 жылдан бастап уранның өзіне көңіл бөлінбей, радийға көңіл аударыла бастады.
1939 жылы уран ядросы ыдырау кезінде көп мөлшерде энергия бөлінетіні анықталды. Осыдан бастап атом энергиясының көзі ретінде уранға деген назар арта бастады.
1. 1. 2 Уранның физика-химиялық қасиеттеріУранның кейбір қасиеттері басқа металдармен салыстырғанда, уранның ІІІ топ элементтерімен ұқсас екені анықталды.
12 - кестеде ІІІ топтың ұқсас металдары ретінде молибден, вольфрам, уран және алюминийдің кейбір қасиеттері келтірілген. Ең алдымен вольфрам уранға қарай ауысқанда, тығыздығы мен балқу температурасының төмендеуіне көңіл аударылды, онда әдеттегідей төменгі аналогтан жоғарыға бұл қасиеттері өседі.
Кесте 4 - Молибден, вольфрам, уран және алюминийдің қасиеттері
Әрекеттес-
Пейді
Әрекеттес-
Пейді
Қара, ыдырамай-
Ды
Сулфоқышқыл-
дар түзуі
Молибдат-
Тар
Вольфрамат-
Тар
1947 жылдан бастап шығатын барлық химиялық анықтамаларда және периодтық жүйенің кестелерінде уран VІ топ элементі ретінде, яғни хром, молибден және вольфрам аналогы ретінде қаралды.
12 - кестедегіден басқа қасиеттерінде біріншіден молибден мен вольфрамның арасында, екіншіден уран мен алюминий арасында толық ұқсастық байқалады. Басқа жағынан вольфрам мен уран қасиеттерінде ұқсастық жоқ. Бұл жағдай уранның VІ топқа емес, ІІІ топқа жататынын дәлелдейді.
Уран, плутоний, нептуний америцийге жоғары валенттілік - алты тән. Уранның реттік нөмірі 92, атомдық салмағы - 238, 07, табиғи уран үш изотоптан тұрады: 99, 28 % U 238 ; 0, 7 % U 235 ; 0, 006 % U 234 . Уранның изотопы U 235 бөліну қасиетіне ие, сондықтан атомдық техникада маңызы зор. Уранның табиғи изотоптары - α -шағылдырушылар жартылай ыдырау периодымен өте жоғары шамалармен өлшенеді: 4, 5 ∙ 10 9 жыл U 238 , 7, 13 ∙ 10 8 жыл U 235 және 2, 48 ∙ 10 5 жыл U 234 үшін. Жасанды түрде массалық салмағы 227-ден 240-қа дейін изотоптар алынған, өмір сүру мерзімдері әр түрлі, жартылай ыдырау периоды - 1, 3 мин. тең.
Уранның тығыздығы 18, 7 г/см 3 -қа тең. Балқу және қайнау температурасы: t б = 1105-1850 о С-ға дейін ауытқиды. Бірақ 1150 о С температураны жоғарыланған деп есептеп, 1133 о С -дағы температураны дұрыс деп алады. Қайнау температурасы 3500 о С; жаңа берілген мәліметтер бойынша - 3927 о С. С. Сиборг және Кац бірнеше төмен шамаларды келтіреді - 3818 о С.
Электрөткізгіштігі 2-4 ∙ 10 4 см-ге тең.
Уран - жұмсақ ақ-сұр металл, механикалық өңдеуге жақсы беріледі. Уранның үш кристалдық модификациясы белгілі: α -модификация ромбалы торлы, бөлме температурасында және 668 о С-қа дейінгі температурада өмір сүреді, β -модификация тетрагональды торлы, 668-774 о С аралығында болады және γ -модификация көлемді центрлі торлы, 774 о С-тан жоғарыда металл балқығанша өмір сүреді. Пластикалық қасиетке α және γ -модификациясы ұшырайды.
Таза уранның қаттылығы мен беріктігі жоғары емес, сондықтан оның механикалық қасиетін жақсарту үшін басқа металдармен құйма түзуге көп жұмыстар жүргізілген.
Уран металл күйінде өте реакцияға түскіш. Компактты металл ауада оңай тотығады да, алдымен алтын түстес қабықпен, сосын қара түспен қапталады, ал ұнтақ уран немесе оның ұсақ жұқа таяқшасы ауада, әсіресе, механикалық әсер еткенде оңай тотықсызданады.
Уран тікелей сутекпен, көміртекпен, азотпен, фосформен, күкіртпен, галогендермен және азот оксидтерімен әрекеттеседі.
Компактты уран суықта ақырын, ал қыздырғанда суды тез ыдыратады, мына реакция жүреді:
U + 2H 2 O → UO 2 + 2H 2 (1)
Түзілген сутек реакцияға әлі түспеген уранмен әрекеттесіп, оны серпімді гидридке айналдырады, содан металл өте тез бұзылады.
Сулы бу уранмен дәл солай әрекеттеседі, ал 150-250 о С температурада әсіресе жылдам, уран оксиді және гидриді түзіледі:
7U + 6H 2 O газ → 3UO 2 + 4UH 3 (2)
Сиборг және Кац бұл реакцияны уранның оттегіде жануынан жылдамырақ өтеді деп көрсеткен.
Уран қышқылдарға қатысты қызықты және практикалық маңызы зор. Тұз қышқылы уранды тез ерітеді, сұйытылған тұз қышқылында 100 о С-да салмағы 10 г уран үлесі 1 сағатта ериді. Күкірт қышқылы уранмен мүлде әрекеттеспейді. Азот қышқылы уранды толық ерітеді.
1. 1. 3 Уранның спецификалық қасиеттеріУранның ерекше қасиетінің бірі, оның өте үлкен энергия мөлшерін бөлетін ядроларды бөлуге бейімділігі, бұл қасиеті тек нейтрондар ашылғаннан кейінгі, яғни 1930-1932 жылдарда белгілі болды. Нейтрон салмағы бойынша протон салмағына тең, бірақ заряды жоқ бөлшек. Сондықтан нейтрондар бөлшекке бөлінбейді, заряд таситын бөлшектерге бөлінбейді және ядро атомына ене алады, сондықтан “снарядтың” өте күшті түрі ядролық реакцияларда қолданылатын, яғни, атомдағы ядролар өзгеруімен байланысты реакциялар.
Ядролық реакция сипаты нейтрон жылдамдығына тәуелді: нейтрондармен реакциының осы немесе басқа түрімен барлық элемент (гелийден басқа, гелийдің ядросы өте тұрақты) ядролары әрекеттеседі. 1933 жылы нейтрондар ядромен қапталатыны анықталды. Мұнда ядро өзгеруі келесі сызбанұсқа бойынша өзгеріске ұшырайды:
(1) сызбанұсқа бойынша бастапқы элемент изотопының түзілуі өтеді. Осы изотоптың ядро салмағы бастапқы ядро салмағынан бір шамаға үлкен. Егер ядроның осы күйі тұрақсыз болса, онда β-ыдырау өтеді, нәтижесінде нейтрон келесі сызбанұсқалық ауысуға ұшырайды:
Бұл жағдайда электрон бөлінеді (немесе β-бөлшек) және заряд түзілген протон нәтижесінде жоғарылайды. (2) сызбанұсқада көрсетілген процесс өтуі және жаңа элемент түзілуіне әкеліп соқтырады. Нейтрондардың “тартып алуын” ашылу заряды 92-ден жоғары, яғни “трансуран” немесе “зауран” элементтерін алуға мүмкіншілік береді. Уранды нейтрондармен “бомбалауда” жаңа элементтер емес, периодтық жүйенің ортасындағы жақсы белгілі элементтер - барий, стронций, лантан және т. б. сонымен қатар инертті газдар табылды.
1938 жылы уран шынында да бөлініп, периодтық жүйенің ортаңғы бөлігіндегі элементтерін беретіні диагональдық ұқсастықпен дәлелденді. Бұл бөлшектердін салмағы уранның салмағынан аз және реакция өте көп энергия мөлшері бөлінуімен жүреді. Есептеулер бойынша, 1 гр көмір атомы жануымен салыстырғанда 1 гр уран атомы бөлінгенде 50 млн. есе көп энергия бөлінеді.
1941 жылы алғаш рет төменде жазылған элементтердің микромөлшері алынды. Уранды атқылау арқылы жаңа элемент түзілуі тек уранның көбірек таралған, қарапайым изотобы мен атом салмағы 238 болған нейтронмен жоғарыдағы (2) сызбанұсқа бойынша анықталады.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz