Атомның электрондық құрылысы және термодинамика негіздері


Атомның құрылуы. Радиоактивтілігі.
- Атомдардың электронды құрылысы. Элементтер қасиеттерінің олардың атомдарының құрылысынан тәуелділігі.
Атомның электронды құрылысы туралы сұрақтарды шешкенде, ең алдымен атомдағы элетронның кез келген тұрақты күйі n, l, m және s кванттық сандардың оның мәндері мен сипаталады. Атомдағы n, l, және m сандардың анық мәндеріне жауап беретін электрон күйі атомдық электрондық Орбиталь деп аталады.
Әр атомдық орбиталь (АО)
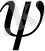 толық функциясының кеңістікте анықталған үлестірімен сипаталады, бұл функцияның квадраты кеңістіктің сәйкес бөлігінде электронды табу ықтималдылығын анықтайды. L мәні 0, 1, 2 және 3 - ке тең, жауап беретін атомдық орбитальдар сәйкесінше S-P-d- және f -орбитальдар деп аталады.
толық функциясының кеңістікте анықталған үлестірімен сипаталады, бұл функцияның квадраты кеңістіктің сәйкес бөлігінде электронды табу ықтималдылығын анықтайды. L мәні 0, 1, 2 және 3 - ке тең, жауап беретін атомдық орбитальдар сәйкесінше S-P-d- және f -орбитальдар деп аталады.
Атомдардың электронды құрылуын жазба схемаларда
- Белгісімен әр орбитальды белгілейміз
Паули принципіне сәйкес, атомда бірдей кванттық сандар жинағы бар екі электрондардың болуы мүмкін емес. Сол себепті, әр атомдық орбитальда екі электроннан артық электрондар болуы мүмкін емес және де олардың арқалық кванттық сандар әр түрлі болуы қажет, белгі түрінде былай көрсетіледі.
Көпэлектрондық атомның тұрақты (қозусыз) күйіне атом энергиясы ең кіші болатын АО бойынша электрондардың үлестіру жауап береді. Сондықтан АО өз энергияларының тізбектеме өсу ретімен толтырылады. (Бәрақ Паули принципіне қайшы келмеуі қажет!) АО-ды элекрондармен толтыру реті Клечковский ережесімен анықталады, ол ережеде орбиталь энергиясының басты (n) және орбитальды (l) кванттық сандар мәнінен тәуелділігін ескереді. Бұл ережелерге сәйкес, АО-ға n+l қосындысының тізбектеме өсу ретімен (Клечкоскийдің 1-ші ережесі), ал бірдей кванттық санның тізбектеме өсу ретімен (Клечковскийдің 2-ші ережесі) электрондарды толықтырамыз.
1 Мысал. А томның 4р ішдеңгейі электронмен толтырылғаннан кейін қай ішдеңгей толтырылады?
Шецшімі 4р ішдеңгейге n+l қосындысы жауап береді, ал ол 4+1=5. Дәл осылай n+l қосындысымен 3d(3+2=5) және 5s (5+0=5) ішдеңгейлері сипатталады. Бірақ 3d күйіне n-нің (n=3) 4р күйінен қарағанда кіші мәні жауап береді, сондықтан 3d ішдеңгейі 4р ішдеңгейден қарағанда ертерек толтырылады. Сол себепті, 4р ішдеңгей толтырылғаннан кейін 5S ішдеңгейі толтырылады, өйткені оған n-нің (n+5) бір бөлікке үлкен мәні жауап береді.
2 мысал. 4S ішдеңгейден кейін қай ішдеңгей толтырылады?
Шешімі. 4S ішдеңгейге n+l=4+0=4 қосындысы сәйкес келеді. Дәл осындай n+l қосындысы 3р ішдеңгейде сипаттайды, бірақ бұл ішдеңгейді 4S ішдеңгейден ертерек толтырамыз, өйткені 4S ішдеңгейге басты кванттық санның үлкен мәні жауап береді. Нәтижесінде, 4S ішдеңгейден кейін n+l қосындысы 3р ішдеңгейді сипаттайды, бірақ бұл ішдеңгейді ертерек толтырамыз, өйткені 4S ішдеңгейге басты кванттық санның үлкен мәні жауап береді. Нәтижесінде, 4S ішдеңгейден кейін n+l=5 қосындылы ішдеңгей толтырылады, және де n+l - дің мүмкін комбинацияларының ішінен (n=3, l=2, n=4, l=1, n=5, l=0) інші толтырылатыны ең кіші басты кванттық санына сәйкес келетіні болады, яғни 4S ішдеңгейден кейін ізінше 3d ішдеңгейі толтыралыды.
АО бойынша электрондарды бір энергиялық ішдеңгей шегінде орналастыру Хунд ережесімен анықталады, ережеге сәйкесінше атомның ең кіші энергиясына атомның қосындылыарқасының абсолют мәні максималды болатындай ішдеңгейге АО бойынша электрондарды үлестіру сәйкес келеді, басқа кез келген электрондарды үлестіру кезінде атом қозу күйінде болады, яғни жоғарырақ энергиямен сипаталатын болады.
Мысал 3. Кремний атомының электронды формуласын және бұл атомның қарапайым және қозу күйіндегі валенттік орбитальдарын электрондармен толтырудың жазба схемасын құру керек.
Шешімі. Кремний атомының электронды формуласын құраймыз. 1S 2 , 2S 2 , 2p 6 , 3S 2 , 3p 2 . Бұл атомда валенттік орбитальдар ретінде сыртқы (үшінші) электронды қабат орбитальдары тұрады, яғни 3S -, 3p-мен тотырылмаған 3d орбитальдары. Бұл орбитальдарды электрондармен толықтырудың жазба схемасы келесі түрде болады:
3р ішдеңгейге электрондарды орналастыру бұл жерде Хунд ережесіне сійкес көрсетілген: атомның қосындылы арқасы ең үлкен мәнге ие (1) . Басқа мүмкін болатын 3р ішдеңгейде электрондары орналастыру, Мысалы
немесе
атомның қосындылы арқасының нөлдік мәніне жауап береді және сондықтан атомның қозу күйіне сәйкес келеді.
Біршама энергияны шығындай отырып кремний атомның 3s -электрондарының біреуі бос 3р-орбитальға ауысуы мүмкін; бұл жағдайда атом энергиясы өседі, жасалып шыққан (1S 2 2S 2 2p 6 3S 1 3p 3 ) электронды конфигурация кремнийдің мүмкін болатын қозу күйлерінің біріне сәйкес:
Электронды аналогтар деп барлық элементтері үшін жалпы формуламен сипатталатын орбитальдарына валенттік электрондарын орналасқан элементтерді айтамыз. Элементтердің периодтық жүйесінде электронды аналогтар бір іштоптың құрамына кіреді.
4 Мысал. Не себепті элементтердің периодтық жүйесінде хлор мен марганеі бір топқа жатады? Не себепті әр түрлі іштолтарға жатады?
Шешімі: Атомныңғ электронды конфигурациясы:
Cl 1S 2 2S 2 2P 6 3S 2 3P 5
Mn 1S 2 2S 2 2P 6 3S 2 3P 6 3d 5 4S 2
Хлордың валенттік электроны -3S 2 3p 5 , ал марганец -3d 5 4S 2 ; Осылай бқл элементтер электронды аналогтар бола ыалмайды және бір тішопқа жатпайды. Бірақ бқл элементтердің атомдарының валенттік орбитальдарында бірдей электрон саны бар -7. Сол себепті олардың екеуі де периодтық жүйенің жетінші тобына жатады да, бірақ әртүрлі іш топқа жатады.
Иондалу энергиясы деп атомды оң зарядталған ионға айналдыратын электронды атомнан ажыратуға кеткен энергияны айтамыз. Иондалу энергиясын әдетте электровольтпен (ЭВ) тұжырымдаймыз.
Иондалу энергиясын атомдарды электр өрісінде үдемелі электрондармен атқылау арқылы анықтауға болада. Атомдарының иондалуы үшін жеткілікті болатын электрон жылдамдығы кезінде потенциалвдарсдың ең кіі айырымы берілген элементтің атомының иондалу потенциалы деп атайды. Вольтпен (В) берілген иондалу потенциалы (1) электровольтпен берілген иондалу энергиясына (Е) тең.
Атомнан жеткілікті энергияны шығындай отырып, екі, үш немесе одан көп электронды шығарып тастауға болады. Иондалудың бірінші потенциалы бірінші электронды алып тастау энергиясына сійкес келедң, ал екіншісі - екінші электронды ажырату энергиясына және т. с. с.
Электрондарды атомнан тізбектей ажырату өлшемі бойынша жасалатын ионның оң заряды өседі. Сондықтан әр келесі электронды ажырату үшін энергияның көп бөлігі шығындануы талап етіледі, яғни иондалудың тізбектей потенциалдары (J 1 , J 2 , J 3 …) өседі. Бұл мысалға алынған берилл, бор және көміртегі атомдарынан көрінеді:
Ве В С
J 1 9, 3 8, 3 11, 3
J 2 18, 2 25, 2 24, 4
J 3 253, 9 37, 9 47, 9
Егер алдыңғы электронмен салыстырғанда ажыратылатын электронның басты кванттық саны кіші болса иондалу потенциалы күрт жоғарылайды. Сол себепті Ве (1S 2 2S 2 ) жағдайында J 1 және J 2 арасындағы айырма J 2 және J 3 айырмасынан кем.
Бұл ядродан ең жақын қашықтықта тұрған үшінші электронды ажыратуға кеткен энергия шығынының көптігіне байланысты.
Басқа теңбе-тең шарттарда да ядро ион радиусы кем болған сайын, соншалықты иондалу потенциалы көбірек болады.
Бұл көзқараспен қарай отырсақ периодта ядро зарядының өсуіне қатысты иондалу потенциалының өсуі байқалуы тиіс (бірдей кванттық (басты) саны бар электронды ажыратқан жағмдайда. Шынында да Ве үшін J 1 мен J 2 міндері С-ға сәйкес мәндерден кем.
Бірақ, одан басқа, иондалу потенциалы атом немесе ионныі электрондық конфигурациясынан да тәуелді. Дербес жағдайда, жартылай немесе толық толтырылған ішдеңгейлер жоғарғы тұрақтылыққа ие.
Қарастырылып жатқани атомдарының электрондық конфигурациясын салыстыра отырып,
В 1s 2 2s 2 В 1s 2 2s 2 2p 1 C 1s 2 2s 2 p 2
Ең тұрақты электронды конфигурация Ве атомына сійкес (толық толтырылған 2S-ішдеңгейі) ; сондықтан оны иондау үшін жоғарылау энергия шығындалады. Ядро зарядының өсуіне қарамастан бордың р- электроннын ажырату аз энергияны қажет етеді.
Энергияны сақталу заңының салдары ретінде 1840 жылы эксперименттік жолмен анықталған Г. И. Гесстің (Гесс заңы) және термхимиялық есептеулердің негізін қалайтын еңбегі бар.
Химиялық реакциясының жылулық әсері (яғни реакция нәтижесінде жүйенің ішкі энергиясы немесе энтальпиясының өзгеруі) реакцияға қатысқан заттардың бастапқы және соңғы күйінен ғана тәуелді және процесстің аралық кезеңінен тәуелсіз болады.
Гесс заңынан, дербес жағдайда, термо-химиялық теңдеулерді қосуға, алуға және сандық көбейткіштерге көбейтуге болатыны шығады.
1 Мысал. Көміртегінің газтектес диоксидінің жасалу жылуы (
 H
0
= -393, 5 кДж/моль) мен термохимиялық теңдеуден
H
0
= -393, 5 кДж/моль) мен термохимиялық теңдеуден
С (графит) +2 N 2 O (2) +2N 2 (2) ;
 H
0
=-557, 5 кДж (1)
H
0
=-557, 5 кДж (1)
N 2 O (2) жасалу жылуын есептеу қажет
Шешімі. Ізделініп отырған шаманы х арқылы белгілеп N 2 O -қарапайым заттардан жасалған термохимиялық теңдеуін жазайық:
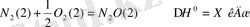 (2)
(2)
Тағы СО 2 (2) -нің қарапайым заттардан жасалған термохимиялық теңдеуін жазамыз:
С (графит) +О
2
(2) =СО
2
(2) ;
 H
0
=-395 кДж (3)
H
0
=-395 кДж (3)
(2) және (3) теңдеулерден (1) теңдеуді алуға болады. Ол үшін (2) теңдеуді 2-ге көбейтіп (3) -ші теңдеуден алып тастаймыз.
С (графит) +2 N
2
O (2) =СО
2
(2) +2N
2
(2) ;
 H
0
=(-393, 5-2х) кДж (4)
H
0
=(-393, 5-2х) кДж (4)
(1) және (2) теңдеулерін салыстырып, белгісізді табамыз.
-393, 5-2х=-557, 5=
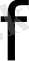 х=82, 0 кДж / моль
х=82, 0 кДж / моль
2. Мысал. Метанның жану реакциясы кезіндегі энтальпияның стандартты өзгерісін
 анықта.
анықта.
СН 4 (2) +2О 2 (2) =СО 2 (2) +2Н 2 О(2)
Ал СО 2 (г), Н 2 О (г) және СН 4 (г) жасалу энтальпиялары сәйкесінше -393, 5, -241, 8 және 74, 9 кДж/моль екені берілген.
Шешімі СО
2
, Н
2
О және СН
4
жасалу реакциялараның термохимиялық теңдеулерін жазайық С(графит) +О
2
(2) =СО
2
(2) ; ) ;
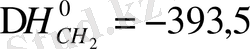 кДж (1)
кДж (1)
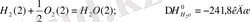 (2)
(2)
С (графит) +2Н
2
(2) =СН
4
(2) ;
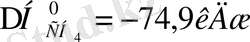 (3)
(3)
- теңдеуге екі еселенген (2) теңдеуді қосып, шыққан теңдеуден (3) теңдеуді шегеріп, қажетті реакциямыздың термохимиялық теңдеуін аламыз:
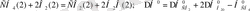
Бұл мәлімттерді қолдана отырып, ізделінді шаманы табамыз;
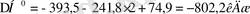
Соңғы мысал Гесс заңының маңызды салдарын көрсетеді, оны қолдана отырып, термохимиялық есептеулерді оңайлатады.
Химиялық рекацияның энтальпиясының стандартты өзгеруі реакциясының өнім жасалуының стандартты энтальпияларының қосындысынан бастапқы заттардың стандартты энтальпиялар қосындысын шегергенге тең.
Реакция теңдеуіне сәйкес әр қосынды сайын реакцияға қатысушы заттардың моль санын ескеру жөн.
3 мысал. 5-ші кестенің мәліметтерінің көмегімен
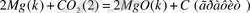
ракциясының
 есептеу.
есептеу.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz