Күкірт қышқылындағы мырыштың еру кинетикасы және электродтық потенциалы жоғары металдардың әсері


«Мырыштың күкірт қышқылында еру кинетикасына, кейбір электртерістілігі жағары металдардың әсері»
Электролит ерітінділерінде металдың өздігінен еру үрдісі зерттеушілердің назарын ертеден аударған. Ол металдардың электрохимиялық коррозиясының негіздерінің бірі болып саналады және гидрометаллургияда көптеген үрдістерді қоса алып жүреді. Жеке алып қарағанда, қорғасынның гидрометаллургиялық өндірісінде металдың қорғасынның еру үрдісі қорғасын қиыршығының көмегімен қорғасын сульфатының қоспалардан ерітіндінің цементациялық арылу тереңдігін анықтайды, сондай-ақ қорғасын электролиз үрдісінің техника-экономикалық көрсеткіштерін анықтайды. Берілген үрдіс никель гидрометаллургиясында және басқа да металдарға ұқсас әсер етеді, сондай-ақ металдарды қышқылдарда ерітіп тұз алуда әсер етеді.
Берілген жұмыстың мақсаты металдық мырыштың күкірт қышқылының су ерітіндісінде еру кинетикасын температураға және ерітінді құрамына байланысты зерттеу, ерітіндіде қорғасынға қарағанда оң электрлі кейбір металдардың қоспаларының бар екендігін анықтау.
1. 2 Қоспасы бар металл ерітіндісінің кинетикасы
Металды біртекті бетте ерітуде электрохимиялық реакция жылдамдығы барлық бөлікте бірдей (эквипотенциалды бет) . Осы жағдай сұйық металға, мысалы сынапты немесе амальгамалы электродқа лайық. Қатты металда осы лайықталық белгілі жақындық ретінде ғана қызмет етуі мүмкін. Егер қатты металл бөліктер кристалл торларырының кемшілігіне байланысты физикалық біртекті болмайды. Жеке кристаллиттер осы нүктелерде электрохимиялық реакциалар кинетикасында көрініс табатын әртүрлі энергия және әртүрлі қасиетке ие болады.
Ерітудің нығайған көрінісінен әлі де ауытқуды металда біртексіз қоспалар бар екендігін анықтауда және оның бетінде әртүрлі химиялық және физикалық қасиетті бөліктер бар екендігін білгенде байқалады. Сондықтан жоғарыда келтірілгендер қандай жағдайда шынайы қатты металға қолданылуы мүмкін екендігін анықтау қажет.
Біртексіз қоспалардың физикалық және химиялық қасиеттерінің негізгі металл қасиеттерінен үлкен өзгешелігінің бар екендігі және осы қоспалар бөлігінде сутегінің бөлінуі төмендетілгені жайлы жағдайлар тіркелген. Осы жағдайда қосындының электродты потенциялы негізгі металл потенциялына қарағанда оң электрлі болуы керек, себебі сутегі бөлінуіне арналған бөліктер жылдам өздік еруге ұшырауы мүмкін.
Бұрынырақта анықталғандай, қоспа және негізгі металл микрогальваний элементтерінің үлкен санын түзеді. Осы элементтердің ішкі кедергісі ерітіндінің электрөткізгіштігі және қоспаның өлшемі мен формасына қарай анықталады. Алғашқы кедергі ерітінді кедергісімен өлшенбейді.
Электрөткізгіштігі төмен ерітінділерде жергілікті электр токтары туындайды. Металда ток қоспаның оң бөлігінен беттің теріс бөлігіне қарай өтеді. Ерітіндіде ток бағыты керісінше. Негізгі металл бетінен токтың өтуінде металдың анодты қышқылдануы болады, ал қоспада сутегінің катодты бөліну реакциясы жүреді.
Қоспаның жұмысы келесі түрде түсіндіріледі. [2] Негізгі металда қоспаның болмауы стационарлық потенциалды тудырады әрі ион разрядының катодты үрдісі және иондалудың анодты үрдісі бірдей жылдамдықпен өткен болар еді. Ал қоспада сутегі ионы разряды жеңілдетілген, сондықтан негізгі металл потенциялының оң жаққа жылжуы байқалады. Осының есебінен негізгі металл еруінің үрдісі жылдамдайды, ал ондағы сутегі бөлінуінің катодты үрдісі баяулайды. Сутегі ионы разрядының жылдамдығы металл табиғатына тәуелді болғандықтан, сутегі бөлінуінің төмен кернеулі қоспасы қышқыл ерітіндісінде жоғары кернеулі металл ерітіндісінің жылдамдығын арттыруы мүмкін. Осындай әрекет темір мен мырыш және сурьма мен қорғасын қоспасында да байқалады. [1]
Беттің катодты және анодты бөліктері ток өткенде поляризацияланады. Локальді элементтердегі ток күші қосылады, егер олардың катодты және анодты бөліктерінің поляризацияның қисығы мен омдық өзара кедергісі белгілі болса.
Металл коррозиясы жайлы әдебиеттерде локальды элементтердің ток күшінің графикалық әдісі катодты және анодты бөліктердің поляризациялық қисығы көмегімен жиі қолданылады. [1. 2]
Осындай диограмманың мысалы 2 суретте көрсетілген.
1. Металдың анодты поляризация қисығы.
2. Қоспаның катодты поляризация қисығы.
1 қисық металдың анодты, ал 2 қисық қоспаның катодты поляризациясына сәйкес келеді. Абсцисса өсіне көбіне ток тығыздығының логарифмін емес, ток күші логарифмін кейде жай ғана ток күшін орналастырады. Тәсілде поляризациялық қисықтың орналасуы металл мен ерітіндінің сипатына ғана емес, сондай-ақ сәйкес бөліктер шамасына да байланысты болады. 2 суреттегі абсцисса анодты және катодты ток күшінің жиынын өрнектейді.
Стационарлық жағдайда микроэлемент жұмысында негізгі металл анодты, ал қоспа катодты поляризацияланады, ал олардың арасындағы потенциалдар айырмасы бастапқыдан төмен болады, сақталынған потенциялдар айырмасы анодты және катодты бөліктерде ерітіндінің омдық потенциялының төмендеуіне сәйкес келеді. (2 сурет)
2 ЗЕРТХАНАЛЫҚ БӨЛІМ
2. 1 Тәжірибенің әдістемесі
Зерттеу 3 суретте көрсетілген құрылғыда орындалған.
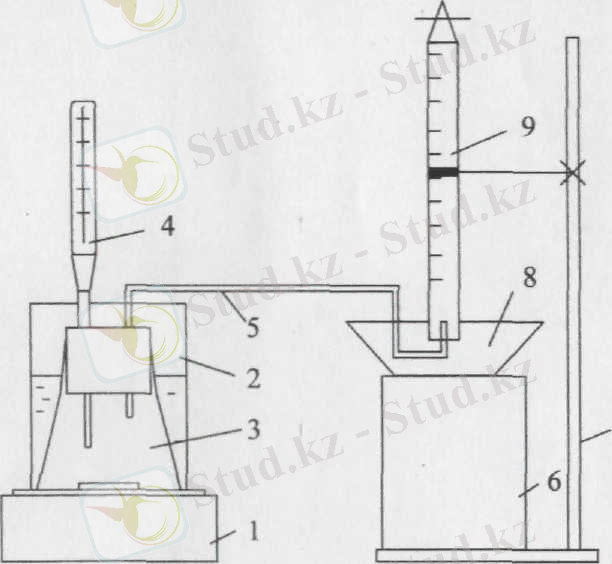
Сурет 3. Күкірт қышқылы ерітіндісінде мырыштың еру жылдамдығын анықтау құрылғысы.
1. магнитті араластырғыш
2. стакан - термостат
3. реакциялық колба
4. термометр
5. ажыратқыш шына түтік
6. подставка
7. штатив
8. су және эксикатор
9. газдық бюретка
Қондырғы сыйымдылығы 0, 14л конустық шыны колбадан тұрады, оған күкірт қышқылының су ерітіндісін құйып мырыш қиыршығын себеді. Колба резина қақпақпен және ажыратушы шыны түтікпен (5) жабылады, олардың көмегімен газ типтес сутегі, мырыштың еру үрдісінде түзіліп 100мл газдың бюреткада судың тесіп өтуі әдісімен жиналуы керек. Су үшін резервуар ретінде эксикатор (9) қызмет етеді. Жиналған газ көлемі қалыпты жағдай тудырды. Бұл үшін бөлу құны 0, 1 0 С термометр көмегімен әрбір тәжірибенің басында және соңында зертханадағы ауа температурасы өлшетіп отырылады. Орташа арифметикалық мәндер есепке алынған. Атмосфералық қысым да ұқсас түрде алынды.
Ерітіндіні термостаттау үшін реакциялық колбаға талап етілген температурамен бір стақан су (2) құйылды.
Ерітіндіні араластыру айналым саны тұрақтылығын қамтамасыз ететін магнитті (1) араластырғыш көмегімен жүзеге асырылады. Күкірт қышқылының ерітіндісі «х. ч» маркалы концентрленген қышқыл ерітіндісін араластыру жолымен алынған. Металл қоспа сульфатының ерітіндісі «х. ч»маркалы тұздардан даярланған. Ерітіндіде 1мл металдың 5мг ионы бар. Қышқыл ерітіндісінің көлемі барлық тәжірибеде, тұрақты 100мл алынған. Еріткіш ретінде барлық жағдайда су алынған.
Мырыш қиыршығы анықталған грануломенриялық құрамда пайдаланылған. Әрбір қиыршық бөлігінің мөлшері 0, 065 тен 0, 1 мм құрайды.
Тәжірибенің бірнеше сериясы мырыштың еру үрдісіне температура және күкірт қышқылының концентрациясының әсерін бағалау мақсатында толық факторлық тәжірибені жоспарлау әдісін пайдалану арқылы орындалды. Осыдан кейін факторлар тұрақты ретінде таңдалынған. Тәжірибенің екінші сериясында мырыштың еру үрдісіне ерітіндідегі мыс, никель, кобальт және кадмий иондарының жеке де, құрамында бола тұрғандағы әсері анықталған.
2. 2 Мырыш ерітіндісі үрдісіне температурамен күкірт қышқылының концентрациясының әсерін анықтау.
Толық фақторлық тәжірибенің жоспарлауы матрицасын температураның және күкірт қышқылының концентрациясының әсерін зерттеуде қолдану қажетті тәжірибе санын минимумға дейін қысқартып, [10], регрессионды теңдеу түрінде алынатын таңдалынған факторлар үрдісінің әсерін бейнелейтін көрнекі тәуелділікті алуға мүмкіндік береді.
Өлшенетін шама мәні әрбір тәжірибеде белгілі уақыт мезетінде екі рет бекітілген.
Жоспарлау матрицасын түрғызу үшін фактордың нольдік деңгейі алынған және жоғарғы және төменгі мәнді алу үшін осы шаманың өзгеру адымы алынған. Температураның нольдік мәні ретінде 25 0 С алынған, ал күкірт қышқылының концентрациясы-0, 1н.
Әрбір факторға сәйкес 5 0 С және 0, 05н шамаларының түрленген адымы таңдалып алынған.
Жоспарлау матрицасы мен оның нәтижесі 3 кестеде көрсетілген.
Кесте 3. Жоспарлау матрицасы және тәжірибелер нәтижесі.
Матрицадан қосу бір параметрдің жоғарғы мәніне сәйкес келеді, минус бір- төменгіге. Температуралық фактор Х 1 мәнімен, концентрациялық Х 2 сипатталады. Х 1 ·Х 2 шамалары үрдіске әсер ететін факторларды сипаттайды.
Нәтижелер У 1 және У 2 сутегі бөлінуінін жылдамдығы мәнімен көрсетілген, көлемді өлшеу тәжірибе аяқталғаннан кейін 5 және 15 минутта жүргізілді, ал параллель емес тәжірибелерде, шама жылдамдығы қатысты болғандықтан күкірт қышқылында мырыштың еру үрдісі стационарлы потенциялға жеткеннен кейін уақатта тұрақты жылдмдықпен өтеді. жылдамдық сутегі көлемінің келтірілген қалыпты жағдайында есептелінді. S 2 шамасы (дисперсия) яғни орташа мәннен квадраттық ауытқу әрбір тәжірибе үшін келесі теңдеумен есептелінді:
S
2
i
=
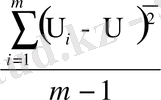 (2. 1)
(2. 1)
Мұндағы m - өлшеу саны
і - өлшеудің тәртіп саны
Регрессионды теңдеу коэффицентінен есептеу үшін, біртектілікке дисперсия нәтижесін бағалау қажет, бұл теңдеу бойынша өрнектелетін Кохрейн критериін пайдалану арқылы жасалды.
G=
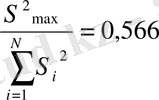 (2. 2)
(2. 2)
Алынған мәнді кестелік мәннен G 1-р (f 1 , f 2 ), салыстырдық, мұнда р=0, 05 химиялық тәжірбиелерге арналған мәндік деңгейі f 1 =m-1 және f 2 =N G 0, 95 (1; 4) =0, 9065 [19] . 0, 566<0, 9065болғанда дисперсиялар біртекті және қайтаөндіру дисперсиясын есептеу келесі теңдеумен шешіледі.
S
2
вос
=
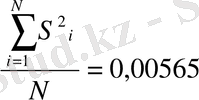 (2. 3)
(2. 3)
Берілген шама регрессия теңдеуінен алынған мәнділік коэффицентін бағалау үшін қажет.
Регрессия теңдеуінің коэффиценті (b j ) келесі теңдеумен анықталады.
b
j
=
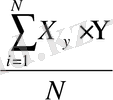 (2. 4)
(2. 4)
b 0 =2, 94, b 1 =0, 85, b 2 =0, 56, b 3 =0, 19 мәндері алынған. Оларға келесі теңдеу сәйкес келеді:
у=2, 94+0, 85·Х 1 +0, 56·Х 2 +0, 19·Х 1 ·Х 2 (2. 5)
мәнділік коэффицентінің бағалауы олардың дисперсиясын есептеді.
S
2
(b
j
) =
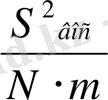 (2. 6)
(2. 6)
Коэффицентердің мәндері Стьюдент критериі арқылы анықталады.
t
j=
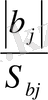 (2. 7)
(2. 7)
Алынған t 0 =110, 5; t 1 =31, 9; t 2 =21, 1; t 3 =7, 1 мәндерін кестелік мәндермен салыстыратын t 1-р (f) мұнда р=0, 05 ал f=(m-1) N
Критерилерді кестелік мәнмен салыстыру f 0, 95 (4) =2, 78 олардың барлығының қажетті әрі t j >2, 78 шартын қанағаттандырады деген қорытындыға келуге болады. Осыдан жоғарыда келтірілген регрессия теңдеуінің (2. 5) соңғы екендігін көреміз.
Теңдеудегі барлық коэффициенттер оң, бұл сутегі бөліну факторының жылдамдығының берілген факторларға тура пропорционал екендігін көрсетеді. Аргументтердегі коэффициеттердің абсолютті мәні үрдіске температураның өзгеруі, концентрацияның өзгеруі әсер ететіндігін көрсетеді. b 0 коэффициентті нольдік деңгейді сипаттайды, басқа сөзбен айтқанда 25 0 С температурада сутегінің бөліну жылдамдығы және 0, 1н күкірт қышқылының концентрациясы болып табылады.
Берілген теңдеу мырыш ерітіндісінің күкірт қышқылындағы еру үрдісіне сәйкес фактордың қателігін ғана білдірмейді, сондай-ақ үрдістің математикалық моделі болып табылады. Жоспарлау матрицасының аргументтерінің мәнін теңдеудегі әрбір тәжірибеге қойып шықсақ, онда осы тәжірибелер үшін сутегі бөліну жылдамдығыныңорташа мәні алынады. Бұ берілген математикалық үрдісті тексеру болып табылады.
2. 3 Мырыштың еру кинетикасындағы қышқыл ерітіндісіне қоспалардың әсері
Зерттеу 0, 1н күкірт кышқылын 25 0 С температурада жүгізілді, өлшенді мырыш қиыршығының салмағы - 1г, қоспа мөлшері 20мг (ион бойынша ) 100мл ерітінді алынды. Тәжірибе нәтижесі 4-11 суретте ерітіндінің ұзақтығынан сутегінің бөлінген көлемінің тәуелділігі түрінде көрсетілген. Әрбір серияда үш параллель тәжірибеден жүргізілді. Мысал ретіндегі нәтиженің қайта өңдеуі 4в суретте берілген үш параллель тәжірибе бойынша тұрғызылған қисық түрінде көрсетілген. 5-11 суретте қисықтар әрбір серияның параллель өлшеулерінің арифметикалық мәніне сәйкес келеді. Көрсетілген мәндерге қарап қайта нәтижесінің қанағаттанарлық екендігін қалай болжауға болады.
Сурет 4. Мырыштың қоспасыз еру ұзақтығына сутегі көлемінің тәуелділігі (үш тәжірибе мәндері)
Сурет 5. Қоспада никель ионы бар мырыштың еру ұзақтығына сутегі көлемінің тәуелділігі.
Сурет 6. Қоспада кобальт ионы бар мырыштың еру ұзақтығына сутегі көлемінің тәуелділігі.
Мырыштың қоспасыз еруінде (сурет 4) қандай да бір кідіріс бақыланған (индукциялық кезең) яғни аралықта газ тәрізді сутегі бөлінбейді. Осы кезеңнің болуы сутегі ионы разряды өтетін катодты бет шамасының жеткілікті еместігін көрсетеді. Осындай бөліктердің пайда болып, катодты және анодты аймақта мырыш дифференциясы жүруіне белгілі уақыт талап етіледі.
Сутегі мырыштың еруінде ұсақ көбіктер бөліп, нәтижесінде ерітінді лайланып кетті, себебі ұсақ көбіктер ірілерге қарағанда батке баяу көтерілді.
Мұндай нәтиже металдың жібуінің артқандығынан болуы мүмкін ол мырыш үшін -0, 63в [14] тең. Металл потенциялының нольдікразряд потенциялымен ауытқуы жағдайынды байқалады.
Мырыштың теңдік потенчиялы минус 0, 73в құрайды. Осыдан мырыштың еруі ісіндегі стационар потенциал -0, 63 тен -0, 73в аралығында жатуы байқалады. Берілген стационарлы потенциалдың кері мәні жоғары катодты және мөлшерленген анодты поляризацияға сәйкес келеді. Сутегіні қалпына келтіру үлкен кернеуліктен өтеді.
Қышқыл ерітіндісінде мыс, никель, кобальт, кадмий иондарының бар болуы соңғысы Ме 2+ +Zn=Ме+Zn 2+ теңдеуіне сәйкес мырыш арқылы қалпына келтіріледі, нәтижесінде мырыш бетінде жаңа фаза, ал бірнеше қоспалар болса - сонша жаңа фаза қалыптасады.
Кадмий ионы (сурет 5), кобальт (сурет 6) және мыс (сурет 7) иондарын қосу жеке тұрғанда да мырыш еру үрдісін белсендіріп, жылдамдығын арттырады. Ион қоспаларының жеке және біріккен әсері мырыш еруі үрдісінде 11 суретте көрсетілген. Мырыштың еру жылдамдығы көрсетілген қоспалардың бірін кен түрде болуында тағы да артады. (9 сурет, 11 суреттегі 6 қисық)
Кадмий қоспасы мырыштың еру үрдісін баяулатады. (8 сурет) және қандайда бір мөлшерде басқа қоспалардың белсенділігін төмендетеді (10 сурет және 11 суреттегі 7 қисық)
Шамасы бойынша үрдіс жылдамдығын білуге болатын ток күшінің қосынды есебі, қышқыл ерітіндісіндегі гальваний жұптарының жұмысы 4 кестеде көрсетілген.
Кесте 4. Әртүрлі жағдайларда тәжірибе басталғана дейінгі 5минутта есептелген ток күшінің мәні.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz