Ерітінділердің құрамы мен қасиеттері: массалық үлес, молярлық концентрация, ерігіштік, еру энергетикасы және кристаллогидраттар


Жоспар
Кіріспе
- Ерітінділердің құрамы және қасиеттері
- Еріген заттың массалық үлесі
- Еріген заттың молярлық концентрациясы
- Қаныққан және аса қаныққан ерітінділер
- Заттың ерігіштігі
- Еритін және ерімейтін заттар
- Сұйылтылған және концентрациялы ерітінділер
- Еру энергетикасы
- Кристаллогидраттар
Пайдаланылған әдебиеттер тізімі
Кіріспе
Химиялық алғашқы мәліметтер және химиялық процестерді қолдан жасай білу ерте заманнан бері белгілі. Химияда басқа ғылымдар сияқты адам қоғамның материалдық мұқтажын өтеуден өсті. Мұнда да басқа ғылымдардағыдай, практикалық білім теориядан бұрынтуды. Іс жүзінде керекті жеке бір химиялық процестерді ( айталық жану, кеннен метал қорыту) оның керегіне пайдалану алғашқа қауым кезінде-ақ болған, мысалы, біздің жыл санауымыздан 3000 мың жыл бұрын месопотомияда кеннен темір, мыс, күміс, қорғасын алған, ал 1200 жыл бұрын. Қытайда түрлі химиялық заттарды алып отырған. Үнді мен Египетте де сол кездерде химиялық жеке өндірістер болған. Әрине осы химиялық білімдер химия ғылым болуынан бірнеше мың жылдар бұрын шыққан Беріректегі құл иеленушілік мемлекеттерде де тұрмысқа керекті химиялық білім өсе берген. Әсіресе ертедегі Египеттекөп химиялық білімдер жинақталған. ХYІІ ғасырдың ортасына дейін химия ғылым деп есептелмеген, оған дейін химия кәсіп, шеберлік ретінде ғана болған. Мысалы, біздің жыл санауымыздан үш ғасыр бұрын ерте замандағы мәдениетті ел-египеттің Александрия деген қаласында ғылым академиясы болған, ондай «құдай-өнері»-химияға арнаулы Серапис сарайы беріліпті-міс, бірақ сонда да, кеннен металл алуды, шыны жасауды, кейбір қышқылдарды, тұздарды басқа да химиялық заттарды ала білген, бірақ мұнда қандай процестер жүретінін оларды меңгеруді білмеген, өйтекені ол кезде бұл химиялық процестердің ғылыми негіздері белгісіз еді.
Алхимия дәуірі химияның өзінде қалыптасқан теория болмағандықтан ол жалпы ғылымдағы үстен теорияның ықпалында болған. Ерте кезде Аристотель (біздің жыл санауымыздан бұрынғы 384-322 жылдар) ілімі үстем болған. Аристотель ілімі мәні затта емес, оның қасиеттерінде, заттың қасиетін өзгертсе, зат өзі өзгереді дейтін. Заттарды өзгертуші «квитессенция» деген бар еді. Аристотелдің ілімін қолдап, она мүлтіксіз, құдай сөзіндей деп танытты.
Ертедегі Египетте, Қытайда, Үндіде және Месопотомияда құнды заттардың бағасыншағатын өлшеуіш -алтынболды. Қолында алтыны бар адам басқа зат ұстаушыға да, зат істеушіге де үстем болды. Сол заманда Александрияда, Аристотель ілімінің әсерінен, жай металдарды алтынға айналдыруғап болады деген ағым туды. Ол үшін квитессенцияның бір түрі. -«философия тасын» табу керек болды. «Философия тасы» алтын жасағаннан басқа кәріні жасартады, ауруды сауықтырады т. т. деп ойлады.
Ол кездегі химияны кәсіп етушінің барлығының арнаны «философия тасын» табу болды. Египетті және басқа шығыс елдерін арабтар жеңіп алған соң (641 ж) олардағы химиялық білімніңбіразы арабтарға көшті. Арабтар ол кездегі химиялық білімді біраз байытты - азот қышқылын, бірнеше тұздарын, басқа жаңа заттарын ашты. Гебер Джафар Ибн Хайан (721-925 ж) сияқты атақты ғылымдары болды. Арабтар химия деген сөзге жұрнақ қосып алхимия деп өзгертті. Арабтар Испаниияны басып алғаннан (711ж) кейін алхимиялық білімдер, әсіресе философия тасын іздеу идеясы, Европа елдеріне тарады. Орта ғасырларды Европа елдерінің химиктері болды. Химия тарихында алхимия дәуірі ұзақ уақытқа (1500ж) созылды. Қорытып айтсақ, алхимия дәуірінен қалған пайдалы істер де бар.
Алхимиктер, көп тәжірибелер жасаунәтижесінде, химиялық жұмыс істеудің толып жатқан тәсілдерін тапты (химиялық рекциялардың үш түрі, қоспаларды (сұйық) ажырату т. б. ) Жаңа заттар алынды; қышқылдар ( НСІ, Н 2 SO 4 , НNO 3 , және патша сұйығы) сілтілер ( Na OH, Ca (ОН) 2 ) түрлі тұздары және мышьк, сурьма, Висмут және фосфор сияқты элеменеттер мұнымен қатаралхимия дәуірі ғылымның дамуына кедергі жасайды. Теориялық негізі Аристотельдің жасалған ілімі болғандықтан, алхимия ғылымға қарсы ағым болып, діни көз қарасты қолдады. Философия тасына өзі ие болып баюдан кейін туған құпияныңзиянды әсерін тигізді . Әрпбір алхимия жаңа бірдеңе тапса оны халыққа басқа ғылымдарға жариялануға тырысатын. Құталарын әкесі балаларына ғана айтып кететін болған химиялық практикада біраз ілгері басқанымен алхимиядан, басқа теория болмады. Осы кезде 1661 ж Роберт Бойль (1627-91 Англия) ескіріп кедергіге айналған алхимия қағидаларына қарсы шығып, оларды мықтоапатайды. Бойль жаңа теория ұсынбағанымен, химияны ғылымижолғБойль жаңа теория ұсынбағанымен, химияны ғылыми жолға қоюға тырысады . « Химиялық элемент деген не?» деп сұрап қойып оған берген жауабы химиялық элементтің осы уақыттағы анықтамасына жуық келеді. Атомдардың бір бірімен жай және күрделі заттар түзіп қосылысатыны сендерге бейорганикалық байланыс түзіледі: ионды, ковалентті ( полюсті және полюссіз) металдық және сутектік. Атомбарарасында ионды немесе ковалентті байланыстың қайсысы түзілмейтінін анықтайтынэлемент атомдарының ең негізгі қасиеттерінің бірі - электртерістілік яғни атомдардың қосылыстарда өзіне электрондар да тарту бейімділігін еске түсірейік. Химиялық байланыс түрлері қосылысатын элемент атомдарының электртерістілігі шамаларының айырмасы қанша үлкен болатынына тәуелді. Байланыс түзуші элемент атомдарының электртерістілігінің айырмасы қанша үлкен болса, Химиялық байланыс типтерінің арасына бірдей бөліп, тек жүргізіп тастауға болмайды. Көптеген қосылыстарда химиялық байланыс ионды байланысқа жақын. Химияның байланыс өз сипаты бойынша шекті жағдайдың қайсысына жақын болса, оны не ионды, не ковалентті полюсті байланысқа жатқызуға болады.
Ерітінділердің құрамы және қасиеттері
Ерітінді деп біртектілігін бұзбай белгілі бір аралықта шамаларын өзгертуге болатын екі немесе одан көп заттардан тұратын гомогенді жүйені айтады.
Сұйық ерітінділер (бұдан әрі тек «ерітінділер» деп айтатын боламыз) сұйық еріткіштен (ол көбіне су болады) және еріген заттан тұрады, еріткішпен араластырғанға дейін олар қатты (КВr), сұйық (H 2 SO 4 ) немесе газ тәріздес (СО 2 ) болуы мүмкін. Сулы ерітінділердегі заттардың жағдайы (ер. ) деп белгіленеді, мысалы КВr (ер) .
Ерітінділер құрамы онда еріген заттың массалық үлесі немесе молярлық концентрациясы шамаларымен беріледі.
Еріген заттың массалық үлесі
Еріген заттың В массалық үлесі ω в - оның массасының т в ерітінді массасына m қатынасы:
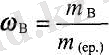
мұндағы т (ер) = т в + т (Н 2 О)
Ерітіндідегі заттың массалық үлесінің бірлігі - оның бір санынан (бірден) немесе 100%-інің үлесі. Мысалы, егер 100 г ерітіндіде 1 г КВr болса, онда ω (KBr) = 0, 01(1%) болады. Мұндай ерітіндіні бір процентті (1%-ті КВr ерітіндісі) деп атайды.
1%-ті тұз ерітіндісінің 100 грамын дайындау үшін, сол тұздың 1 грамын және 99 г су алу керек. Бөлме температурасында судың тығыздығы 1 г/мл, сол себепті 99 мл суды өлшеп алып, оған 1 г тұз салған дұрыс.
Еріген заттың молярлық концентрациясы
Еріген заттың В молярлық концентрациясы с в - сол зат мөлшерінің п в ерітінді көлеміне V (ер) қатынасы:
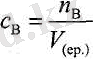
Ерітіндідегі заттың молярлық концентрациясының өлшемі: моль/л.
Егер 1 л ерітіндіде 1 моль КВr болса, онда с(КВr) = 1 моль/л . Мұндай ерітінді бір молярлы деп аталып, 1М деп белгіленеді. Осыған ұқсас 0, 1М, 0, 01М және 0, 001 М деген жазуларға сәйкес деци-, санти- және миллимолярлық ерітінділер деген атау беріледі.
1 л 1М КВr ерітіндісін дайындауға зат мөлшері 1 моль (яғни 119 г) болатын тұз шамасы алынады; оны көлемі 0, 8 л суда (яғни міндетті түрде 1 л-ден аз алады) ерітеді, одан соң көлемін сумен 1 л-ге жеткізеді.
Берілген температурада ерітінді көлемі V (ep) ерітінді массасымен т (ер) және оның тығыздығымен р (ер ) төмендегідей қатынас арқылы байланыста болады:
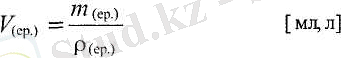
Мысалы, тығыздығы 1, 074 г/мл (1074 г/л) кейбір 100 г ерітіндінің көлемі 93, 1 мл (0, 0931 л) болады.
Қаныққан және аса қаныққан ерітінділер
Қатты заттың (көбінесе тұздың немесе гидроксидтің) суда еру процесін қарастырайық.
Суы бар стаканға (Т=const) заттың алғашқы мөлшерін салғанда, ол толығымен еріп, қанықпаған ерітінді алынады. Мұндай ерітіндіде сол заттың келесі мөлшерлерін, стакан түбінде оның тұнбасы түскенше салып ерітуге болады (мысалы, КВr) .
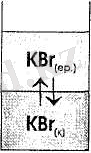
Қаныққан ерітінді алынды. Ерітіндідегі зат пен тұнбадағы осы зат арасында гетерогенді тепе-теңдік күй орнайды:
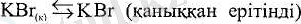
Еріген заттардың бөлшектері бөліну беті арқылы тұнбадан ерітіндіге және керісінше өтеді, бұл жағдайда қаныққан ерітіндінің құрамы, Т = const болғанда, тұрақты болады.
Кейде ерітіндіні ерекше жағдайларда дайындағанда (қанықпаған ыстық ерітіндіні жайлап суыту) зат қаныққан ерітінді мен тұнба емес, аса қаныққан ерітінді түзуі мүмкін. Ондай ерітінділер көбіне тұрақсыз - «түртпе» (заттың кішкене кристалы) салысымен еріген заттың артық мөлшері тұнбаға түсіп, қаныққан ерітінді алынады.
Заттардың ерігіштігі
Қаныққан ерітіндідегі Т = const кезіндегі заттың шамасы сол заттың ерігіштік мөлшерін сипаттайды. Көбінесе ерігіштік 100 г суда еріген заттың массасымен есептеледі; мысалы 20°С-та 65, 2 г КВr/100 г Н 2 О, яғни 20°С-та 70 г калий бромидін 100 г суға салса, тұздың 65, 2 г ерітіндіге (қанығатын) ауысады, ал 4, 8 г қатты КВr (артықтық) стакан түбінде қалады.
Қаныққан ерітіндідегі еріген заттың шамасы берілген температурадағы оның ерігіштігіне тең, ал қ анықпаған ерітіндіде одан көп болатындығын әрқашан есте сақтау керек. Мәселен, 20°С-тағы 100 г су мен натрий сульфатынан NaSO 4 (epiгіштігі 19, 2 г/100 г Н 2 О) тұратын ерітінді құрамында:
15, 7 г тұз болғанда - қанықпаған
19. 2 г тұз болғанда - қаныққан
20. 3 г тұз болғанда - аса қаныққан
Температура көтерілгенде, қ атты заттардың ерігіштігі көбінесе артады (KBr, NaCl), тек кейбір заттар (CaSO 4 , Li 2 CO 3 ) үшін ғана керісінше жағдай байқалады:
Газдардың ерігіштігі температураны жоғарылатқанда төмеңдейді, ал қысымды көтергенде еседі, мысалы, 1 атм қысымда аммиактың ерігіштігі 52, 6 (20°С) және 15, 4 г/100 г Н 2 О (80°С), ал 20°С-та және 9 атм-да- 93, 5 г/100 г Н 2 О.
Еритін және ерімейтін заттар
Ерігіштік шамаларына қарай заттарды:
- жақсы еритіндер - қаныққан ерітіндідегі массасы судың массасымен шамалас (мысалы, 20°-та КВr ерігіштігі 65, 2 г/100 г Н 2 О; 4, 6М ерітінді) ;
- аз еритіндер - қаныкқан ерітіндідегі массасы судың массасынан әлдеқайда аз (мысалы, 20°С-та CaSO 4 ерігіштігі 0, 206 г/100 г Н 2 О; 0, 015M ерітінді) ;
- іс жүзінде ерімейтіндер - қаныққан ерітіндідегі массасы еріткіштің массасымен салыстыруға келмейтіндей аз (мысалы, 20°С-та AgCl ерігіштігі 0, 00019 г /100 г Н 2 О, 0, 134M ерітінді) .
Бөлме температурасындағы әр түрлі заттардың судағы сапалық ерігіштігі 3. 8-кестеде көрсетілген.
Сұйылтылған және концентрациялы ерітінділер
Еріген заттың мөлшері аз ерітінділерді сұйылтылған ерітінділер деп, ал еріген заттың мөлшері көп болса, оларды концентрациялы деп атайды. Мәселен, 1%-ті және 0, 1М КВr ерітінділері - сұйылтылған ерітінділер, ал 32%-ті және 4, ЗМ КВг ерітінділері концентрациялы ерітінділер болады. Осыған қарағанда концентрациялы ерітінділерді жақсы еритін заттар ғана түзе алады, ал сұйылтылған ерітінділерді кез келген ерігіштігі бар заттар түзе береді.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz