Көмірсутектердің сұйық фазада лантан құрамдас табиғи саз катализаторларымен гетерогенді тотығуы


С. ТОРАЙҒЫРОВ АТЫНДАҒЫ ПАВЛОДАР
МЕМЛЕКЕТТІК УНИВЕРСИТЕТІ
ӘОЖ 544. 4:542. 9:665. 64. Қолжазба құқығында
ЕРКИБАЕВА МЕРУЕРТ ҚУАНДЫҚҚЫЗЫ
Көмірсутектердің сұйық фазада лантан құрамдас катализаторлармен гетерогенді тотығуы
02. 00. 15 - катализ
Химия ғылымдарының кандидаты
ғылыми дәрежесін алу үшін дайындалған диссертация
Ғылыми жетекшілері
х. ғ. д., профессор
Сүлейменов М. А.,
х. ғ. к. Нұрғалиев Ж. А.
Қазақстан Республикасы
Павлодар, 2010
МАЗМҰНЫ
Рентгенофазалық және электронды микроскоптық
зерттеу әдістері
НОРМАТИВТІК СІЛТЕМЕЛЕР
Диссертацияда келесі стандартарға сілтімелер жасалды:
ГОСТ 6. 38-90 Унифицирование системы документации. Система организационно-распорядительной документации. Требования к оформлению документов.
ГОСТ 7. 1-84 Система стандартов по информации, библиотечному и издательскому делу. Библиографическое описание документа. Общие требования и правила составления.
ГОСТ 7. 9-95 (ИСО 214-76) Система стандартов по информации, библиотечному и издательскому делу. Реферат и аннотация. Общие требования.
ГОСТ 7. 12-93 Система стандартов по информации, библиотечному и издательскому делу. Библиографическая запись. Сокращение слов на русском языке. Общие требования и правила.
ГОСТ 7. 54-88 Система стандартов по информации, библиотечному и издательскому делу. Представление численных данных и свойствах веществ и материалов в научно-технических документах. Общие требования.
ГОСТ 8. 417-81 Государственная система обеспечения единства измерений. Единицы физических величин.
БЕЛГІЛЕУЛЕР МЕН ҚЫСҚАРТПАЛАР
ДМФА - диметилформамид
ИҚ-спектрі - инфрақызыл спектрі
ккал - килокаллорий
адс - адсорбция
сек - секунд
W - Вольт
кг - киллограмм
см - сантиметр
эВ- электровольт
мА- мегаампер
S -талғамдылық, %
К - конверсия(айналым), %
r - меншіктік каталитикалық белсенділігі (моль/м 2 ∙с)
КІРІСПЕ
Жұмыстың жалпы сипаттамасы. Диссертация көмірсутектердің сұйық фазада лантан құрамдас катализаторлармен гетерогенді тотықтыруға арналған. Осы уақытқа дейін глиоксальді этиленгликолді мыс катализаторымен дегидрлеу арқылы алып келді. Этиленгликолді алу күрделі және көп сатылы реакция екені белгілі. Сол себепті оны ацетиленді тотықтыру арқылы бір сатыда алу өте маңызды болып келеді.
Ацетилен қатарындағы көмірсутектердің сұйық фазадағы тотығуы соңғы уақытқа дейін аз зерттелген, бірақ соған қарамастан органикалық қосылыстардың үлкен және маңызды классына жататын бұл көмірсутектерді зерттеу теориялық және тотығудың бағалы өнімдерін алуда орны ерекше.
Процесті зерттеуде қолданбалы бағыт ретінде ауадан ацетиленді тазарту болып табылады. Басқа бағыты - ацетиленді каталитикалық тотығуы арқылы кеңінен қолданылатын мақсатты және жартылай өнімдерге - формальдегид, ацетальдегид, құмырсқа, сірке қышқылдары және тағы басқаларын алу болып табылады.
Зерттеу тақырыбының өзектілігі . Дүниежүзілік мұнай өндіруші кәсіпорындарының негізгі тенденциясы көмірсутек шикізатын максималды пайдалану арқылы жоғарғы сапалы өнім алуға жаңа технологияларды ендіру болып табылады. Қазіргі уақытта мұнай өндіру қалдықтары мен өндірісте түзілетін құрамаларды мейлінше терең өндеу мәселесі шешімін таппай тұр.
Көмірсутектердің молекулалық оттегі немесе құрамында оттегісі бар газбен жұмсақ каталитикалық тотықтыру мұнай-химиялық синтездеу технологиясының дамуының болашақтағы бағыты болып табылады. Тотығу өнімдері - альдегидтер мен кетондар - техникалық аса қажет полимерлер мен сополимерлердің бастапқы мономері ретінде пайдаланылады. Бұл процестерді зерттеу және оптимизациялау, негізінен, үш бағыт бойынша жүреді:
- газ фазалы тотығу;
- сұйық фазалы гомогенді тотығу;
- сұйық фазалы гетерогенді тотығу.
Газ фазалы тотығу процесі толығырақ зерттеліп, өндіріске кеңінен ендірілген.
Бірақ, сонымен қатар оны өткізу бірнеше факторларға байланысты қиындайды. Көмірсутектердің тотығуы экзотермиялық жолмен жүретіндіктен, катализатордың сәл қызуы көмірсутектердің толығымен тотығуына жол беріліп, соған байланысты процестің талғамдылығы төмендейді. Осы және тағы басқа кемшіліктер процесті сұйық фазада өткізген уақытта жойылады. Сұйық фазалы тотығу процессі температураны төмендетіп және толық емес тотығу өнімдерін талғамды алуға мүмкіндік береді. Сондықтан сұйық фазалы тотығуды пайдалана отырып, өндірісте қолданылатын шетелдік қымбат катализаторлар орнына сапасы жағынан кем түспейтін және бағасы жағынан арзан отандық катализатор өндірісін қалыптастыру, әлі де болса толығымен өз шешімін таппаған мәселе.
Тақырыптың зерттелену дәрежесі. Әлемдік тәжірибеде көмірсутектерді тотықтыру арқылы жоғары өнімдерді алу жолдары зерттеліп, жаңа технологиялар жасалған. Осындай ғылыми жұмыстардың қарқынды дамуына қарамастан көмірсутектерді сұйық фазада табиғи катализаторлар мен гетерогенді тотықтыру толығымен зерттелінбеген.
Жұмыстың ғылыми бағдарламалар жоспарымен байланысы. Диссертациялық жұмыс бұрынғы жоспарға сәйкес жүргізілген жұмыстың жалғасы болып саналатын С. Торайғыров атындағы Павлодар мемлекеттік университетінің химия және химиялық технологиялар кафедрасында «Көмірсутектердің сұйық фазада лантан құрамдас катализаторларымен гетерогенді тотығуы» тақырыбы бойынша жүргізіліп отырған жұмыстың жоспарына, Қазақстан Республикасының БҒМ-нің мемлекеттік тіркеу номері 0197 ҚР 00549 және 0101 ҚР 010012 «Қазақстанның органикалық және бейорганикалық шикізаттарынан алынған материалдар мен заттардың физика-химиялық қасиеттерін зерттеу» атты іргелі зерттеу бағдарламасына сәйкес келеді.
Жұмыс мақсаты. Көмірсутектердің сұйық фазадағы гетерогенді тотығу принциптерін және соған сүйене отыра сулы, сулы ацетатты, диметилформамид орталарында жартылай тотығу өнімдерін алуда тиімді катализаторларды құрастыру.
Жұмыстың мақсатына жету үшін келесі міндеттерді шешу көзделінді:
- Көмірсутектер тотығу реакциясының бағытына еріткіштер табиғатының әсерін анықтау;
- Тотығудың ықтимал механизмін анықтау;
- Көмірсутектер сұйық фазада тотығуы нәтижесінде құрамында оттек бар өнімнің көп мөлшерде бөлінуіне ықпал ететін талғамды катализаторды құрастыру;
- Газды қоспаның компоненттерінің қатынасының процестің талғамдылығына әсерін анықтау.
Зерттеу нысаны және пәні. Зерттеу нысаны - катализатор қатысында көмірсутектерді сұйық фазада гетерогенді тотықтыру процесін зерттеу болып табылады. Зерттеу пәні - табиғи сазға қондырылған лантан құрамдас катализаторларды қолдану.
Жұмыстың ғылыми жаңалығы :
- Алғаш рет Кеміртұз кен орнының сазы тасымалдағыш қызметін атқара отырып, ацетиленді сұйық фазада тотықтыру процесіне пайдаланылды;
- Ағынды қондырғы негізінде ацетиленнің табиғи сазға қондырылған лантан құрамдас катализаторында гетерогенді тотығуы алғаш рет зерттеліп, реакциялардың жүру схемасы ұсынылды;
- Ацетиленді және пропилен тотықтыру және табиғи сазға қондырылған лантан құрамдас катализаторын қолдану арқылы сұйық фазада формальдегид алу жолы қарастырылды;
- Ацетиленді сұйық фазада тотықтыруының алғашқы өнімдері анықталып, сонымен қатар ацетиленнің көмірқышқыл газы мен су түзілетін толық тотығу процесі жүретіні анықталды.
Жұмыстың теориялық құндылығы және практикалық маңызы. Көмірсутек шикізатын өндеуде заманауи қалдықсыз технологияны шығаруды жүйелі түрде шешу. Отандық табиғи және техногенді шикізат негізінде жаңа каталитикалық жүйелерді синтездеу арқылы Қазақстанда өзіндік катализаторлық өндірісінің бой көтеруіне ат салысу.
Отандық мұнай өндеу кәсіпорындарында қалдықсыз өндеу технологиясын дамытуға және өндірісте нанотехнологиялық жаңашылдықтарды ендіру мәселесіне жұмыста алынған нәтижелерді қолдану.
Жүргізілген құбылыстардың нәтижелері және жүйелердің әрекеттесуінен алынған өнімдер С. Торайғыров атындағы Павлодар мемлекеттік университетінің химия және химиялық технологиялар кафедрасында оқылатын арнайы курс дәрістеріне қосымша құрал ретінде ұсынылып отыр.
Қорғауға ұсынылған негізгі қағидалар.
- Ацетиленнің толық тотығуына жол бермейтін әдіс табылып, еріткіштер табиғаты, көмірсутек газдарына қатысты ерігіштік қасиетіне және де реакциялық ортада тотығуға тұрақтылығына байланысты болып келетіні анықталды.
- Табиғи сазға қондырылған лантан құрамдас катализатормен тотығу процесінде пропиленнен пропион альдегиді түзілетіні анықталды.
Жұмыстың талқылануы. Диссертацияның жұмыстың негізгі нәтижелері: «Шоқан тағылымы - 13» атты халықаралық ғылыми - практикалық конференцияда (Көкшетау қаласы, 2008 ж. ) ; «Уәлиханов оқулары - 14» атты халықаралық ғылыми - практикалық конференцияда (Көкшетау қаласы, 2009 ж. ) ; Материалы международной научно-практической конференции «Иртышский бассейн: Современное состояние и проблемы устойчевого развития». -Павлодар, ИнЕУ, -2009.
Автордың жеке үлесі. Жұмыстың тақырыбы бойынша әдеби материалдарды біріктіру және талқылау, жұмыстың тәжирибелік бөлімін орындау, алынған нәтижелерді талдау және өндеу, оларды ғылыми мақала түрінде шығаруда ізденуші тікелей өз үлесін қосты.
Басылымдары. Жұмыстың нәтижелері бойынша барлығы 10 ғылыми жұмыс, оның ішінде мақала ҚР БҒМ білім және ғылым саласындағы бақылау комитетінің басымдары тізіміне енетін журналдарда, ал Халыққаралық ғылыми конференциялардың жинақтарында жарық көрді.
Диссертацияның құрылымы мен көлемі. Диссертациялық жұмыс кіріспеден, үш тараудан, қорытындыдан, 201 басылымды қамтитын отандық және шетелдік әдебиеттер тізімінен тұрады. Жұмыс 97 бетте жазылып, 22 кестемен және 21 суретті қамтиды.
1 ӘДЕБИ ШОЛУ
1. 1 Ацетилен қатарындағы көмірсутектердің тотығуы
Ацетилен қатарындағы көмірсутектердің сұйық фазадағы тотығуы соңғы уақытқа дейін аз зерттелген болып есептеледі, соған қарамастан органикалық қосылыстардың үлкен және маңызды классына жататын бұл көмірсутектерді зерттеу теориялық және тотығудың бағалы өнімдерін алуда орны ерекше.
Процесті зерттеуде қолданбалы бағыт ретінде ауадан ацетиленді тазарту болып табылады. Басқа бағыты - ацетиленді каталитикалық тотығуы арқылы кеңінен қолданылатын мақсатты және жартылай өнім - формальдегид, ацетальдегид, құмырсқа, сірке қышқылдары және тағы басқаларын алу. Бұл процестер жөнінде мағлұматтар патенттер түрінде кездеседі. Мысалы, бор қышқылына сіңдірілген, қақталған саз үстінде ацетиленді тотықтырғанда формальдегид түзіледі. Ағылшын патенттік мәліметі бойынша ацетальдегидтің сірке қышқылымен қоспасы ацетиленнің ауамен 2 - 3 : 1 қатынаста тотығуы нәтижесінде және 573 - 673 К температурадағы су буының артық мөлшерінде алынады. Катализатор ретінде пемзаға орналастырылған мырыш, мыс және никель, ванадий, хром, молибден қышқылдарының тұздары қолданылады. 653 К температурада мырыш ванадатында жүргізілген тәжірибе нәтижесінде алынған: ацетальдегид 75 - 80% және сірке қышқылы 5% [1 - 10] .
Ацетиленнен ацетальдегидті алу кезінде реакция температурасын төмендету үшін су буының орнына су құрамына сәйкес келетін стехеометриялық мөлшерінде араласқан оттегі және сутегімен алмастыруға болады. Катализатор екі немесе одан да көп металдар (Ni, Cu, Fe немесе Mg т. б. платина қатарындағы) оксидтерінен тұруы мүмкін [11 - 15] .
Ацетилен, сутегі, оттегі және азот қоспаларын 2 : 4 : 2 қатынаста 373 К температурада Ni - Pd катализаторынан өткізгенде 8 - 10% этил спирті түзіледі. Бұл әдіс бойынша этил спиртін алу ацетальдегидтің тотықсыздануы деп білуге болады. Спиртті конденсация немесе суда еріту арқылы бөлгеннен кейін қалған газдарды керек құрамға дейін «байытып», реакцияға қайта жібереді. Одан басқа, ацетиленді ацетонға айналдыруға болады. Мысалы, ацетиленнің 1 көлеміне сәйкес су буы мен ауаның 2 - 5 көлемі қоспасын 623 - 723 К температурада катализаторға толы түтікшені қыздырады. Патенттік мағлұматқа сәйкес [2] өнім құрамында 40% ацетон, көмірқышқыл газы, көміртек (ІІ) оксиді, метан және аз мөлшерде ацетальдегид пен формальдегид түзіледі.
Бұл процесті жүргізу үшін алюминий сақиналарына отырғызылған оксидтер мен металдардың басқа да қосылыстары да патенттелген.
Авторлардың [16 - 21] ғылыми еңбектеріне сүйене отырып, ацетальдегидті су буы мен ацетилен қоспасынан оттегі қатысында 623 - 673 К температурада алу үшін, құрамына дегидрлеуші (никель оксиді, мыс, мырыш оксидтері немесе сульфаттары, кобальт селениді, кадмий вольфраматы, мырыш пен вольфрам, кадмий мен молибден оксидтерінің қоспасы) заттарымен белсендірілген алюминий оксиді катализатор ретінде пайдаланылады.
Концентрлі азот қышқылы палладий (ІІ) тұзарының қатысында ацетиленді қымыздық қышқылына дейін тотықтырады. Реакцияға катализатор болып басқа ауыспалы металдар иондары пайдаланылады. Реакцияның жүру механизмі белгісіз болып отыр. Ацетиленнің қымыздық қышқылына дейін тотығуы бірнеше кезеңдерден тұрады деген ой бар, кейбіреулері каталитикалық емес. Қымыздық қышқылының түзілуінің жолын анықтау үшін аралық өнім бола алады деген күдікпен кейбір заттарды азот қышқылымен тотықтырады. Ацетиленнен қымыздық қышқылының түзілуінің аралық өнімі ретінде сірке альдегидін қарастырайық. Яғни, азот қышқылымен ацетальдегидті тотықтыру кезінде 10% шығымдылыққа ие қымыздық қышқылы түзіледі. Реакцияға 48% азот қышқылы мен 303 К температура қажет. Процесс индукциялық кезеңімен ерекшеленеді. Сонымен қатар, палладий (ІІ) иондары қышқылдың түзілуіне ешқандай әсер етпейді [22 - 33] .
Осыдан альдегид тобы карбоксил тобына тотығуымен бірге метил тобының тотығуы жүретіндігі анықталды. Қымыздық қышқылының аз өнімділікке ие болғанын метил радикалының қиын тотығатындығымен түсіндіріледі. Бұл процестің аралық өнімі ретінде глиоксаль да түзілетінділігі ықтимал, бірақ тәжірибе жүзінде дәлелденбеген.
Долгов Б. Н. [34 - 41] зерттеулері бойынша, ацетиленді азот диоксидімен тотықтырғанда 30% астам глиоксаль түзіледі. Қазіргі уақытта глиоксальды этиленгликольды мыс катализаторында дегидрлеу арқылы алады. Бірақ та этиленгликольды алу күрделі және көп сатылы реакция. Сондықтан бұл әдіс бойынша алу қиынға түседі. Сол себепті, глиоксальды ацетиленді тотықтыру арқылы бір сатыда алу өте маңызды.
Ацетиленді толығымен тотықтыратын белсенді катализатор 1 - кестеде көрсетілгендей платина мен палладий болып табылады:
Кесте 1 - Катализаторлар бойынша ацетиленнің толық тотығуының мәліметтері
Тәжірибе жағдайлары: С С2Н2 = 100% болғандағы r - меншіктік каталитикалық белсенділігі, моль/м 2 ∙с
Төмен температурада платина палладийден белсендірек, ал температура жоғарлағанда палладийдің белсенділігі артады, себебі ацетиленнің тотығуының активтендіру энергиясы бұл катализаторда жоғары. Күміс 413 К - де белсенді емес, ацетиленнің тотығуы тек 523 - 573 К жүреді, ал мыс төмен каталитикалық белсенділік танытады [42 - 49] .
Ацетиленнің металдарда тотығу механизмі зерттелмеген. Платина мен палладийде ацетилен бойынша теріс ретті реакциялардан сол көмірсутегінің күшті адсорбцияланғаны және катализатордың «уланғаны» айтуға болады.
Кейбір зерттеулерде ацетилен платинамен берік байланысады деген [50 - 55], яғни ацетиленмен берік байланысқан соң сутегінің тотығуын катализдеу мүмкіндігінен айырылады.
Ацетиленнің аз мөлшерде тотығуы оксидті катализаторларда зерттелген. 473 К температурада меншікті каталитикалық белсенділік тізбек бойынша азаяды: MnO 2 > Co 3 O 4 ; CuO > Fe 2 O 3 > Cr 2 O 3 > NiO.
Мағлұматтар бойынша [56 - 59] белсенді катализатор болып Co 3 O 4 есептеледі. 573 К температурада ацетилен қатарындағы көмірсутектерді мыс оксидінде тотықтырғанда [60 - 65], катализ беткі қабаттың тотықсыздану-тотығу үзілісті схемасы бойынша жүреді. Яғни, реакция механизмінің келесідей схемасын жорамалдауға мүмкіндік береді
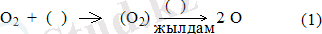

RН - ацетилен қатарындағы көмірсутек, (О) - беткі қабаттағы оттегі, (І) - карбоксилат - карбонат типті аралық комплекс [66 - 68] .
Ацетиленнің тотығу реакциясында жоғарғы белсенділікке гопкалит MnO 2 -CuO типті күрделі катализаторлар ие (MnO 2 : CuO = 1, 5 : 3) . Күмістің аз мөлшерде қосындысы бұл катализаторларды промоторлейді және оның су буымен «улануын» төмендетеді.
Промотор ретінде [69 - 76] кобальт және церий оксидтері зерттелген. Ең жақсы катализатор болып 10% Ag қосылған MnO 2 - CuO (6 : 4) есептеледі. Ол ұзақ уақыт бойын жұмыс істейді және реакция барысында MnO 2 - тің аз мөлшерде қайта орнына келуі байқалады. Ацетиленнен тазалау үшін эффективті катализатор болып күміспен промотирленген марганец диоксиді есептеледі. 483 К - де күмісті енгізген кезде β - MnO 2 және β - MnO 2 ∙Н 2 О меншікі белсенділіктері артады (2 - кесте) .
Катализатордағы промотор күйі соңына дейін зерттелмеген. Оны әр түрлі орталарда ерітілген Н 2 О, NH 4 OН, HNO 3 - Н 2 О 2 күміс мөлшерімен анықтайды [77 - 83] . Ең үлкен үлесті болып [85 - 88] 55 - 63 % аммоний гидроксийдінде еріген күміс есептелінеді. Күміс еритін аммиакты жүйеге айналатын оксид күйінде болады және жеке фаза түзбейді [89 - 91] . Марганец (ІV) оксидімен байланысы күміс оксидінің жарамдылығын төмендетеді [91] .
Күміс перманганатының жоғары активтілік көрсететіндігі жөнінде мәліметтер бар [92 - 95] . Палладий күміспен салыстырғанда, марганец оксидінің промоторы ретінде белсенділігі төмендеу. Сол себепті, промоторлену эффекті промотор табиғатымен қоса промотирленетін оксид табиғатына да байланысты.
Кесте 2 - Реакциялық қоспада оттегінің артық мөлшеріндегі ацетиленнің марганец оксидті катализаторында тотығуы
Тәжірибе жағдайлары: * - β- MnO 2 және β - MnO 2 +Н 2 О негіздегі катализаторлардағы күмістің беттік концентрациясы бірдей.
С 2 Н 2 концентрация-сы
5∙10 -8 моль/л тең болғандағы r∙10 -7 (моль/м 2 ∙с)
β - MnO 2
+ 0, 072% Ag *
Оксидті күміс және палладиймен промоторлегенде, оларды механикалық араластыруға да болады, бірақ адсорбциялық дайындау әдісі катализ процесі кезінде ацетилен-ауа ылғалданған қоспасын қолданғанда бірталай мүмкіндіктер береді.
Катализатор құрамында күміс оксидінің болуы мен оның белсенділігі үлкен қызығушылық тудырады. β - MnO 2 ∙Н 2 О + Ag контактісінің жоғары белсенділігі берілген гидратталған оксидте катализ процесіне тұрақты және аммиакта еритін күміс оксидінің максималды мөлшерімен анықталады. Кобальт оксидімен промотирленген катализатор қолданғанда, күмістің концентрациясы әлдеқайда жоғары. MnO 2 - Ag 2 O және Со 2 О 3 - Ag 2 О катализаторларының бастапқы жоғары белсенділігі оның құрамындағы күміс оксидінің болуымен түсіндіріледі. Күміс оксиді өз алдына өте белсенді, бірақ істен тез шығып қалады да, белсенділігі төмендейді. Сол себепті де механикалық жолмен жасалған MnO 2 - Ag 2 O және Со 2 О 3 - Ag 2 О катализаторлардың белсенділігі тез төмендейді.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz