C- және N-орынбасқан пиперидин-4-ондар: синтез әдістері және фармакологиялық әлеуетінің әдеби шолуы


НЕГІЗГІ БӨЛІМ
1 ӘДЕБИ ШОЛУ
1. 1 Пиперидин-4-ондарды алу әдістері
Қазіргі таңда пиперидин-4-ондарды синтездеу жөнінде тәжірибелік материалдардың жиналғаны соншалық, тіпті оларды реакцияның жүру бағытына байланысты екі түрге бөлуге болады /1, 2/:
- α, β, α′, β′-Дивинилкетондар мен олардың туындыларының
(α, β, α′, β′-дивинилкетондардың қос байланысы бойынша спирттердің, судың, екіншілік аминдердің және т. б. қосылуының өнімдері) аммиакпен және біріншілік аминдермен тұйықталуы.
Бұл әдістің тобына кетондардың карбонилді қосылыстармен, амииакпен және біріншілік аминдермен конденсациясы; кетондикарбон қышқылдары эфирлерінің альдегидтермен аммиак және біріншілік аминдер қатысындағы реакциясы, сонымен қатар Манних реакциясын жатқызуға болады. Соңғы жатқызылған әдістер бұл жағдайларда реакция барысында аралық қосылыстар ретіндегі α, β, α′, β′-дивинилкетондар мен олардың туындыларының түзілуімен түсіндіреді.
- Дикман әдісі бойынша құрамында азот бар дикарбон қышқылының күрделі эфирлерінің тұйықталуы /3/.
1. 1. 1 C- және N-орынбасқан пиперидин-4-ондарды синтездеу әдістері
Қаныққан азотты гетеротұйықтардың маңызды және қызықты бөлімдерінің бірі С- және N- орынбасқан пиперидин-4-ондар болып табылады, онда С 3 және С 5 үшін сутегі атомы және карбонил топтары кең көлемді биологиялық әсерімен жаңа әртүрлі қосылыстар әкелу үшін әрі қарай химиялық түрленулер жасайтын реакциялық қабілеттілік орталықтарын ұсынады.
Бастапқы қосылыстардың қол жетімділігі, синтездің қарапайымдылығы, әрі қарай түрлендірудің мүмкіншілігі және үлкен фармакологиялық потенциалы арасынан жоғары және әртүрлі биологиялық активтілігі бар препараттар табылған пиперидин-4-онның орынбасқан туындыларының қатарында физиологиялық активті заттарды (ФАЗ) іздестіруде бағытталған синтетиканы жүзеге асыру үшін маңызды аргумент қызметін атқарады. Бұл препараттардың көпшілігі медицинада және ауыл шаруашылығында кеңінен қолданылады.
Пиперидин-4-онды алудың алғашқы әдісін 1874 жылы Ресейде Н. Н. Соколов және П. А. Лачиновтар /1/ және оларға тәуелсіз Германияда Гейнц /2/ жасады, яғни олар дәнекерленген ампулада қаныққан аммиакты қыздыру арқылы триацетонамин деп аталатын 2, 2, 6, 6-тетраметилпиперидин-4-он қосылысын синтездеді.
Гейнц /3/ мезитил окисі және диацетонамин түзілу сатысы арқылы өтетін пиперидин-4-онды алу процесін жасады. Кейіннен Маттер /4/ бұл реакцияны бөлме температурасында зерттеп диацетонаминді негізгі өнім ретінде бөліп алды, онда қымыздық қышқылы әртүрлі альдегидтер мен кетондармен реакцияға тез түсіп α, α - орынбасқан пиперидин-4-он түзетінін көрсетті. Бірақ γ-пиперидонды алудың бұл әдісі шығымының аздығынан шектеулі ғана қолданылады.
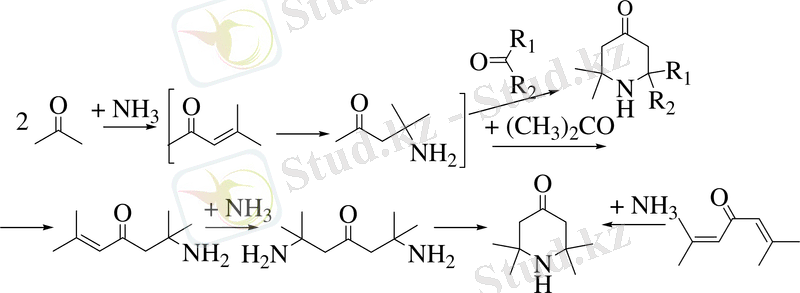
Әрі қарай мақсатталған өнімнің шығымын жоғарылату мақсатымен Соколов және Гейнц әдісін жақсарту үшін көптеген талпыныстар жасалғаны сипатталған. Сонымен, сұйық аммиак немесе алдын ала дайындалған хлористі кальцийдің аммиакатын пайдалану арқылы жасаған Э. Г. Розанцевтың жұмысында /5/ триацетонамин шығымының біршама жоғарылағаны байқалады. Бұл реакцияны әрі қарай зерттеулер хлористі кальцийдің аммиакатының орнына ауыспалыкатионды смола немесе Льюис қышқылын қолдануға болатындығын көрсетті.
Ацетонға ұқсас басқа кетондар да әрекеттеседі. Сонымен, метилэтилкетонның амииакпен конденсациясында 2, 3, 6-триметил-2, 6-диэтилпиперидин-4-он /6/, диэтилкетоннан - 3, 5-диметил-2, 2, 6, 6-тетраэтил диэтилпиперидин-4-он /7/ алынған.
Келтірілген реакцияларда кетондар метиленді және карбонилді компоненттер ретінде түседі. Біршама жоғары шығымды гетеротұйықты кетондар альдегидтердің карбонилді компоненттері ретінде қолдану арқылы алынған.
Соколов және Гейнц /1, 2/ басылымынан кейін жиырма жыл өткен соң дивинилкетондардың аммиакпен алғашқы өкілдерінің бірі, форон тұйығында қорытындылатын триацетонамин синтезінің жаңа әдісін ұсынды /8/. Кейіннен Терентьев және Гурвичтер /9/ зерттеген бұл реакция сатылы түрде өтеді деп болжады. Одна аммиак немесе біріншілік амин алдымен бір, содан кейін екі байланыс арқылы қосылып, соңында пиперидин тұйығы болып тұйықталады.
Қазіргі уақытта тирацетонаминді синтездеудегі көптеген әдістердің ішіндегі тиімдісі тапқан өндірісте қолданылатын, Азингер аппаратында /6/ ацетонның аммиакпен каталитикалық конденсациясы болып табылады.
Триацетонамин туындылары медицинада және химиялық өндірісте қолданылады. Олардың негізінде он тоғызыншы ғасырдың соңында кокаинның синтетикалық ауыстырғыштары (α- және β-эйкаиндер), синтезделіп алынды, ол өз уақытында медицинада практикалық қолданылған жергілікті жансыздандыратын құрал ретінде табылған.
Триацетонамин қазіргі уақытта пириленнің эффективтілігі жоғары ганглиоблокатор өндірісінде гипертония ауруын емдеу үшін табылып қолданылатын бастапқы заттың түйінді ролін атқарады /10/. Аминокетонның және олардың кейбір туындыларының каталитикалық тотығуынан полимеризация реакциясының ингибиторлары, антиоксиданттар, синтетикалық зерттеулерде құрылымдық үлгілер ретінде реакцияның элементарлы актісінің жылдамдық константасын анықтау үшін пайдаланылатын тұрақты иминқышқылды радикалдар алынады /11/.
1899 жылы Петренко-Критченко қызметкерлерімен /12/ ацетонкарбон қышқылының диэтилэфирі және бензалдегидтің қоспасын құрғақ аммиакпен қанықтырып, келесі аралық 3, 5-дикарбэтокси-туындысын сабындау дәне декарбоксилдеу арқылы 2, 6-дифенилпиперидин-4-онды алудың негізгі әдісін жасады:
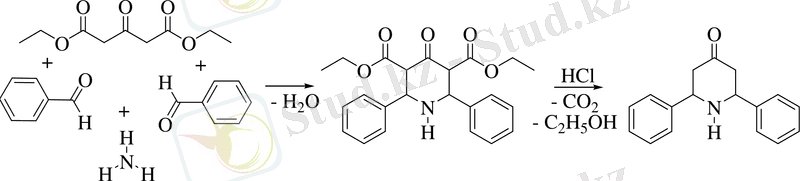
Осыған сүйене отырып, ацетоннан және екі молінен пиперидон синтезделді, сонымен бірге соңғысын Ридельмен /13/ дибензальацетон және метиламиннен алды:
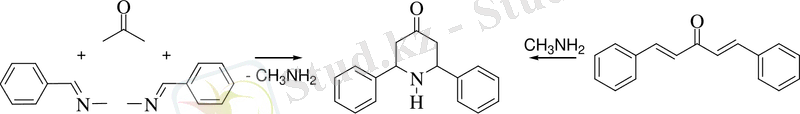
Петренко-Критченко әдісі Манних тарқатқан әдіспен дамыды /14, 15/, ол ацетонкарбон қышқылы эфирінің орнына диэтилкетонның формальдегидпен және метиламинмен конденсациясынан симмтериялық 1, 3, 5-триметилпиперидин-4-он синтезі алынды:
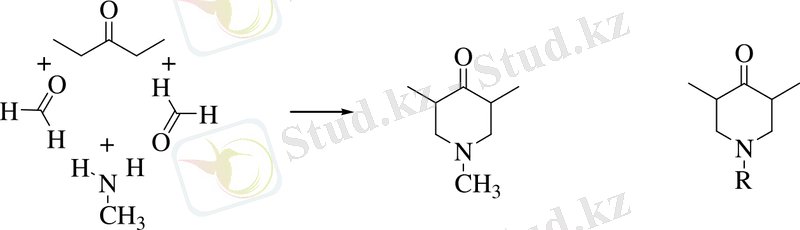
Формальдегидті басқа май қатарының алдегидтеріне (сірке, пропион, май) ауыстырғанда және әртүрлі біріншілік аминдерді пайдаланғанда олардан орынбасқан пиперидондардың толық қатары синтезделді /16/.
Манних реакциясы - әлсіз қышқыл ортада жүретін реакция. Ол диалкиламинметил топтарымен кетондар және альдегидтердің α-алкилденуіне әкеледі /17/:
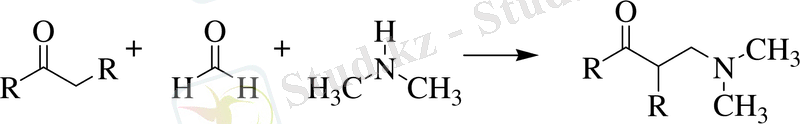
мұнда, R = H, C n H 2n+1 , Ar
Электрофильді бөлшектер аминнен және формальдегидтен түзілген иминді ион болып табылады. Реакция сутегі атомының енолизациясына қабілеттілігі бар альдегидтер мен кетондар үшін жалпы жеткілікті болып табылады.
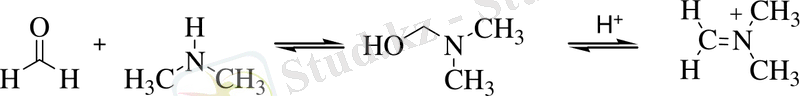
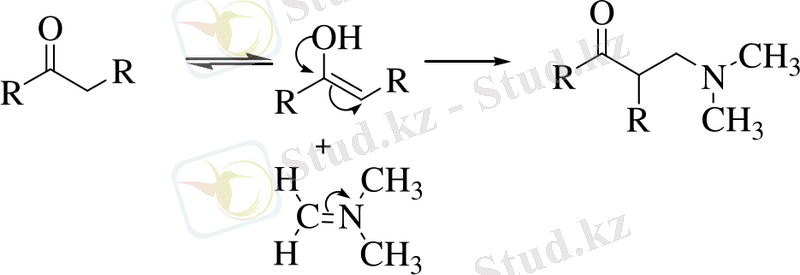
мұнда, R = H, C n H 2n+1 , Ar
Арнаулы мақсаттар үшін екіншілік аминдерді пайдаланумен шектеледі, себебі біріншілік аминдермен негізгісі диалкилдеу процесі болып табылады. Бірақ, диалкилдеу реакциясы кейбір тұйықтүзу реакцияларында табысты қолданылуы мүмкін, мысалы /18/:
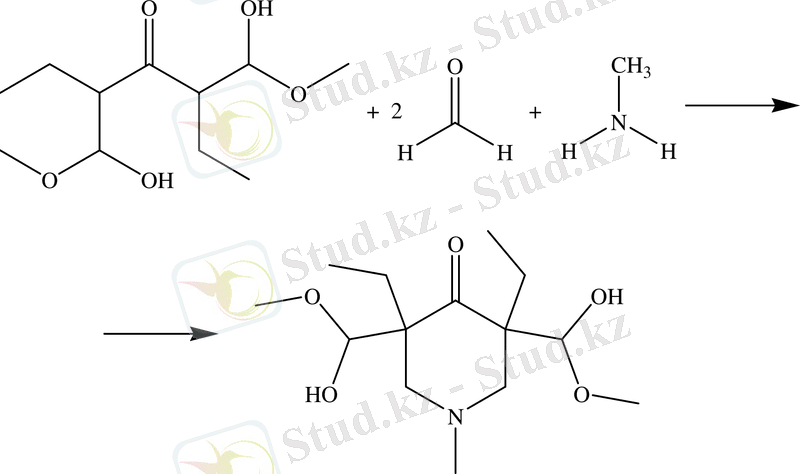
Майлар қатарындағы формальдегидті басқа альдегидтерге ауыстырғанда және әртүрлі біріншілік аминдерді қолданғанда 2, 3, 5, 6 жағдайларындағы орынбасар бар пиперидин-4-ондар алынған. Сондай-ақ сірке қышқылында орынбасарлы пиперидин-4-ондар жоғары шығыммен алынатыны зерттелген.
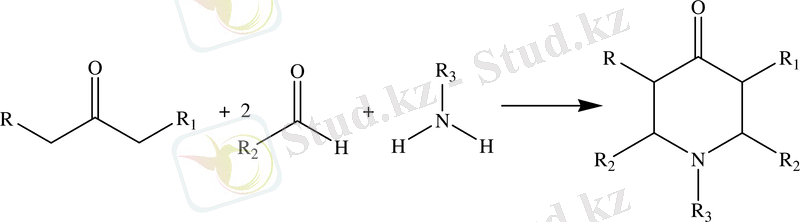 мұнда, R, R
1
, R
2
, R
3
= H, C
n
H
2n+1
, Ar
мұнда, R, R
1
, R
2
, R
3
= H, C
n
H
2n+1
, Ar
Г. С. Миронованың зерттеулері /17, 18/ Манних реакциясында амфотерлік жүйеде күрделі катализдік жағдайының орны бар екенін көрсетті. Онда алдымен, формалин және аминнен R 2 NCH 2 + катионы түзіледі, содан кейін бұл катионның анионмен жылжымалы сутегі атомы бар конденсациясы жүреді. Катионның түзілуі қышқылдармен, аниондар - негіздермен индукцияланады. Қышқылдың көптігі конденсацияның бірінші сатысында теріс білінеді, ол қажетті аниондардың түзілуіне кедергі келтіреді, ал сілтінің көптігінен катиондардың түзілуі басым болады. Сондықтан Маннихтің әрбір реакциясы үшін ұтымды аймақ рН-қа байланысты болады.
Манних реакциясы үшін ең күшті еріткіш сірке қышқылы болып табылады деп есептеледі. Сонымен, метилбензилкетонның бензальдегидпен және метиламинмен конденсациясы сірке-спирт ортасында ең жоғары шығыммен (34 %) 1-метил-2, 3, 6-трифенилпиперидин-4-онның /21/ түзілуіне әкеледі.
Манних реакциясымен қол жеткізген пиперидин ядросындағы көптүрлі орынбасарлар жанама реакциялармен көпкомпонентті реакциялық қоспаларда азап шегеді, онда реакция өнімдерін арнайы тазалаудан өткізуге тура келеді.
1. 1. 2 α, β, α′, β′-Дивинилкетондар мен олардың туындыларының аммиакпен, біріншілік аминдермен немесе сумен тұйықталуы
И. Н. Назаров ашқан сынап (II) тұзының әсерімен изомеризациясы, сонымен қатар дивинилацетиленді көмірсутектердің гидратациясы әртүрлі гетеротұйықты кетондарды синтездеуге мүмкіншілік береді /22-32/.
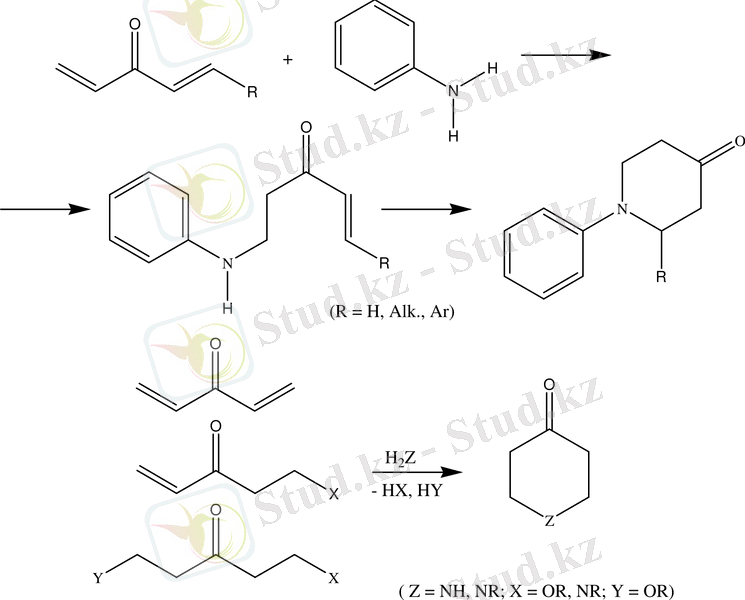
И. Н. Назаров және В. А. Руденко /26/ аммиак және біріншілік алифатты аминдер көп жағдайларда α, β, α′, β′-дивинилкетондармен тұйықталу реакциясына түседі деп көрсетеді.
Тұйықталу ароматты аминдердің сусыз ортасында жүрмейді, онда орынбасарсыз винил тобы бойынша аминнің қосылуы байқалады. Ал реакцияны судың каталитикалық мөлшерінің қатысында жүргізгенде тұйықталу байқалады /23/. /23/ Мақаланың авторлары тұйықталудағы реакция бағыты және өнім шығымы ароматикалық аминдердің негізгі күшіне әсер етеді деген қорытынды шығарады. Сонымен, п -фенетидинмен тұйықталудағы өнім шығымы (К=2, 15 10 -9 ) 61 % құраса, ал п -толуидинмен (К=2 10 -10 ) - 25 % құрайды.
И. Н. Назаровпен жасалған α, β, α′, β′-дивинилкетондар мен олардың туындыларын сумен, аммиакпен және біріншілік аминдермен тұйықтап пиперидин-4-ондар және тетрагидропиран-4-ондарды алу әдісі құрамында бір және бірнеше гетероатомы бар, әртүрлі моно- және политұйықты азот-, оттегіқұрамды кетондарды синтездеу және стереохимиялық зерттеулер үшін негіз болып табылады /33-37/.
Бұл жұмыстарда N-орынбасқан 2-метил-, 2, 5-диметилпиперидон-4 /38-42/ және 4-кетопергидрохинолинді ассиметриялық синтездеу және абсолютті конфигурациясын құру бойынша зерттеулер ерекше орын алады. Оптикалық белсенді α-фенилэтиламинмен қайтааминдеуге негізделген пиперидон-4-ті ассиметриялық синтездеу мүмкіншілігі көрсетілген. Ассиметриялық аминдеудің оптикалық шығымы 50 % құрайды, бұл энантиомердің бөлінуінің пиперидолға сәйкес жеке диастереомерлерге айналуын дәлелдейді.
Жоғарыда көрсетілгендей, ұқсас реакциялар аммиак және біріншілік аминдердің катысуымен де, қатыспауымен де карбонилді қосылыстардың альдегидтермен конденсация реакциясы тұйықталу реакциясы болып табылады.
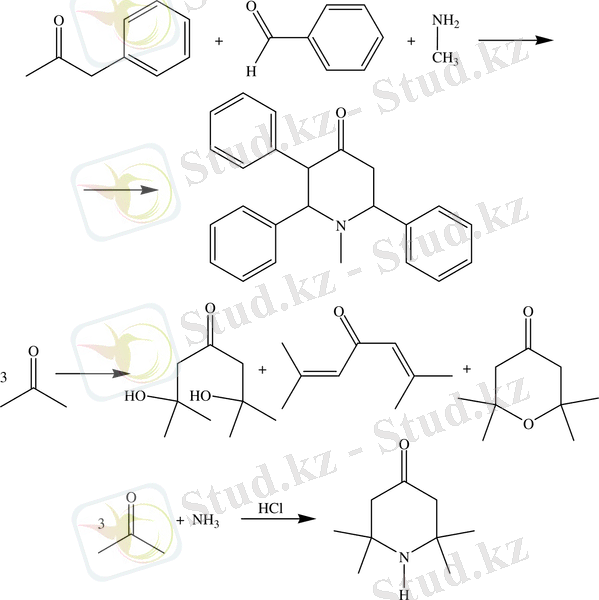
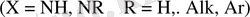
Метилбензилкетонның бензальдегидпен және метиламинмен сірке-спирт ортасындағы конденсациясының нәтижесінде 34 % шығыммен 1-метил-2, 3, 6-трифенилпиперидин-4-он алынды /43/. Ал ацетонның аммиакпен конденсациясында (хлорлы кальций, катионалмастырғыш шайырлар, Льюис қышқылы) катализатор қатысуындағы сияқты, олардың қатысуынсыз да 2, 2, 6, 6-тетраметилпиперидин-4-он түзілген /44/.
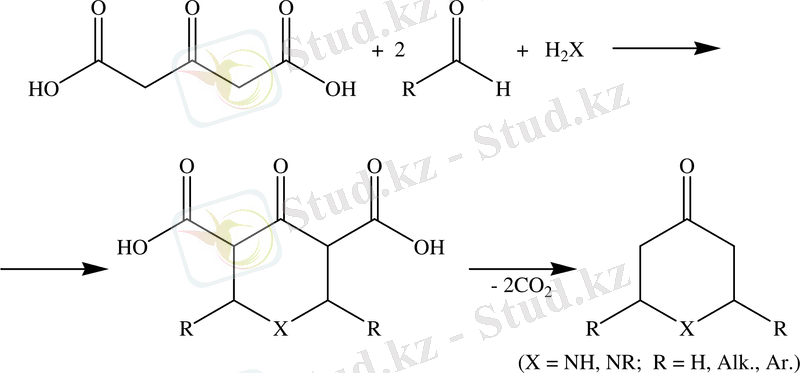
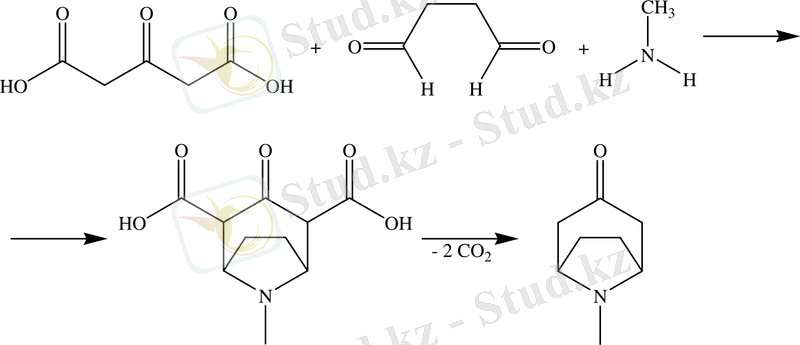
Осы кетонмен Петренко-Криченко реакциясы - амин қатысында ацетондикарбон қышқылы эфирінің альдегидпен конденсациясын көруге болады /45-49/. 2, 6-Дифенилпиперидон-4 шығымы 50-70 % құрайды. Бұл реакция Робинсон бойынша тропанон синтезі негізіне тиісті болып келеді.
1. 1. 3 2, 5-Диметил- және 1, 2, 5-триметилпиперидин-4-он синтезі
α, β, α′, β′-Дивинилкетондардың аминмен әрекеттесуінен алынған γ-пиперидондар қатарындағы 2, 5-диметил- және 1, 2, 5-триметилпиперидин-4-ондарды алудың тиімді әдісін жасайтын зерттеулерге көп көңіл аударуды қажет етеді, себебі олар физиологиялық белсенді заттар синтезі үшін бастапқы өнімдер, соның ішінде "Промедол" /27, 50/ және "Рихлокаин" /51/ анальгетиктері терминалды, инфильтрлі, өткізгіштік сияқты анестезияның барлық түрлері үшін анестезиялық белсенділікке, сонымен қатар дерматопротекторлық әсеріне, спазмолитикалық, антинекратикалық белсенділікке ие болып келеді.
Алғаш рет 2, 5-диметилпиперидин-4-онды И. Н. Назаров пен В. А. Руденко /26/ синтездеді, онда жеке алынған , 1-метокси-2-метилгексен-4-он-3 және 1, 5-диметокси-2-метилгексанон-3 аммиактың сулы ерітіндісімен әрекеттесіп сәйкес шығымдармен 10, 9, 12, 0, 51, 3 % алынды. Сулы спирттегі гидратациясында жоғарыда көрсетілген кетондардың қоспасы түзіледі, бұл кетондардың қоспасын пайдалана отырып 2, 5-диметилпиперидин-4-онды алу қызығырақ болды.
Бұл жұмыс И. Н. Назаров, Н. С. Простаков, Н. Н. Михеевтермен жүзеге асырылды /52/. Болат баллонда жүргізілген реакция нәтижесінде 2, 5-диметилпиперидин-4-онның шығымы 28 % - 34, 7 % құрады.
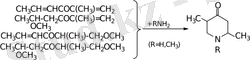
Кетондардың қоспасын аммоний ацетатының сулыметанол ерітіндісімен (1 % сірке қышқылының артық мөлшерімен) әрекеттестіріп жүргізілген реакцияда колбадағы гетеротұйықты кетондардың шығымы 41, 6 % (кетонның реакциясында алынған) және 48, 1 % (реакцияға түскен кетондар) құрады. Бұл реакцияны аммоний ацетатының сулы ерітіндісімен жүргізгенде өнім шығымы 39, 1 және 41, 4 % - ға дейін төмендегені байқалады. Барлық жағдайларда 2, 5-диметилпиперидин-4-оннан басқаларында өнімдер конденсацияның соңында алынады.
А. Ш. Шарифканов және басқалары /53/ тербелетін автоклавта (А-200, Венгрия) жүргізілген реакцияда 2, 5-диметилпиперидин-4-он шығымына реакцияның ұзақтығының, температурасының және реагенттердің қатынасының әсерін зерттеді. Реакцияны жүргізу үшін 70-100 % құраммен айдалған кетондардың қоспасын қолданды. Зерттеулер кетон: аммиак қатынасын жоғарылатқанда өнім шығымының жоғарылап, 1:14 қатынасында максималды 57, 7 % жететінін, ал содан кейін төмендейтінін (1:20 қатынасында шығым 52, 8% құрайды) көрсетті. Бұл зерттеулерде реакция температурасы 60-62 0 С аймағында тұрақталып, реакция уақыты 6 сағатты құрады. Ары қарай зерттеулер, өнімнің максималды шығымы (1:12 қатынасы, 60-62 0 С температурасы) үш сағаттан соң (46, 5 %) байқалатынын көрсетті. Гетеротұйықты кетондардың шығымы 2 және 6 сағаттан соң сәйкес 42, 7 және 39, 1 % құрайды. Ең соңында температура әсері келесі нәтижелерде айқындалды: құрамында 70 % кетондары бар қоспа үшін реагенттердің қатынасы 1:14 және реакцияның ұзақтығы 2-3 сағатта өнім шығымы 80-82 0 С температурада 55, 5-56, 3 % құраса, 98-100 0 С температурада - 38, 9 % құрады. Сонымен, зерттеу жұмыстарын жүргізген авторлар және монометокси- мен диметоксикетон қоспасының сулы аммиакпен тұйықталуының тиімді әдісі келесідей болады деп шешті: 1:14 реагенттердің қатынасында, 80-82 0 С температурада, 2-3 сағатта. Сонда 2, 5-диметилпиперидин-4-онның шығымы 55, 5-56, 3 % жетеді.
Жоғарыда көрсетілгендей /26/, 2, 5-диметилпиперидин-4-онның ең аз шығымы жағдайында байқалады. К. Х. Токмурзин және басқаларының зерттеулерінде немесе кетондардың қоспасын ( артығымен) аммиактың сулы-метанолды ерітіндісімен (реагенттердің 1:5 қатынасында және 80 0 С температурада) ағын түріндегі қондырғы арқылы жібергенде және қоспаны 2-3 сағат бойы қыздырғанда 2, 5-диметилпиперидин-4-онның шығымы 80 % жететінін көрсетті.
1, 2, 5-Триметилпиперидин-4-он және оның монометокси- және диметоксикетондардың қоспасын метиламиннің сулы ерітіндісімен әрекеттестіргенде жоғары шығыммен алынатыны зерттелді.
2, 5-Диметилпиперидин-4-он синтезі туралы көптеген жұмыстар гетеротұйықты кетондардың сонымен қатар стереохимиясын да зерттеуге бағытталған. Көміртегінің екі ассиметриялық атомдарының бар болуы екі стереоизомердің (транс- және цис- формада) бар екенін алдын ала болжайды. 2, 5-Диметилпиперидин-4-онды жеке формаға бөлу үшін жасалған көптеген әрекеттер нәтиже бермеді, бірақ бір изомер бөліп алынды /54/.
Циклогексан жүйесінің конформациялық анализінің принципінен шығатын, ұқсас пиперидиндермен, 1, 2, 5-триметилпиперидин-4-он үшін аса тұрақты (энергетикалық тиімдірек) изомер тұйықтағы (транс-изомер) экваторлы орынбасарларының максималды сандарымен саналады.
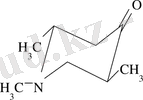
Бұл нәтижелер МФПДП/3 /55/ жақын ССП МО ЛКАО және екі еселенген спектроскопия NOE SY /56/ әдістерін пайдалану арқылы пиперидин-4-онның конформациялық анализінен алынды. Соңғы жұмыста азот атомы үшін бөлінбейтін электрондар жұбының аксиалды орналасуы дәлелденген.
1. 1. 4 Дикман реакциясы бойынша пиперидин-4-ондарды алу
Дикман реакциясын қолданудың (сілтілік агенттер қатысында дикарбон қышқылы эфирінің тұйықталуы циклді кетоэфирдің түзілуіне әкеледі) ең кең таралған аймақтары пиперидин-4-ондарды және тетрагидропиран-4-ондарды алу болып табылады /57/.
Сансыз көптеген тәжірибелік мәліметтер жоғары шығымдардың көрші карбалкоксил тобымен метилен тобының бар болуы жағдайында байқалатынын көрсетеді. Метин тобының жағдайында - шығым төмендейді және тәжірибелік зерттеулер мысалы, натрий гидриді немесе натрий амиді сияқты көптеген күшті негіздерді пайдалануды талап етеді.
Реакция жылдамдығына карбалкоксил тобының β-жағдайында орналасқан орынбасарларының табиғаты әсер етеді. Метил тобы метилен компонентінің белсендігін төмендетеді, ал орынбасарлар электрон тығыздығын өзіне тартып (мысалы, карбэтокситобы) күшейтеді.
Дикман реакциясын жүргізу үшін сілтілік агенттер ретінде металл натрий және калий, сілтілік металдың алкоголяттары, амидтері және гидридтері пайдаланылады, себебі гидридтерді пайдаланғанда пиперидин-4-ондардың шығымы жоғарылайды /57-63/.
Сол сияқты, Дикман реакциясын қолданғанда әртүрлі γ-гетеротұйықты кетондарды синтездеуге көп мүмкіншілік берді. /57/ Жұмыста пиперидин-4-ондарды алу туралы 20-дан аса әдебиеттік сілтемелер келтірілген, олардың көп бөлігі N-алкилпиперидон-4 және N-алкил-3-метилпиперидон-4 синтезіне жатады.
E. A. Prill және S. M. McElvain натрий этилатының қатысында еріткіш ортасында немесе еріткіштің қатысуынсыз 1-метилпиперидон-4 алды. Онда натрий этилаты ең жоғары конденсирлеуші агент болып табылатыны анықталды. Ал реагенттерді еріткіштермен (мысалы, бензолмен) сұйылту конденсация реакциясына қолайлы болып келеді /60/. Онда еріткіш ретінде толуол және ксилол қолданылды. N-алкил-β, β′- орнына пиперидин-4-ондарды алу үшін біріншілік аминдердің акрилнитрил туындыларына қосылғандағы өнімін пайдалануға болады. Сонымен, С. К. Әлімжанова және басқалары бис(2-цианэтил) метиламиннен 1-метилпиперидон-4-ті 53 % шығыммен синтездеп алды /64/.
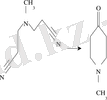
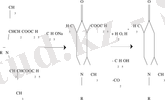
мұнда, R = H, C n H 2n+1
Сол сияқты, Дикман реакциясы негізінде 2, 5-диметилпиперидин-4-он алу әдісін жасаған ҚазМУ органикалық химия кафедрасының қызметкерлерін де атап өтуге болады /65/.
Тағы да 2-карбоксипропил-2′-карбоксиизопропил эфирі барий тұзының пиролизбен әрекеттесуінен түзілген 2, 5-диметилпиперидин-4-он синтезін де ерекше бағалауға болады /66/. Бірақ бұл реакция Дикман реакциясына жатпайды, бірақ түрлену түрі бойынша Дикман реакциясына ұқсас болғандықтан бұл бөлімге жатқызамыз.
Шамасы, бұл реакциядағыдай басқа пиперидин-4-ондар алынуы мүмкін.
1. 2 Пиперидин қосылысының физиологиялық активтілігі
Кез келген профильдің дәрігерінің жиі кездесетін көптеген мәселелері бұл қатерлі синдромды жою және профилактикасы екені белгілі. Бұл мәселені шешудің бірден бір жолы жалпы жансыздандыру болып табылады, бірақ оны қолданғанда маңызды кедергілер және қосымша эффектілер болуы мүмкін. Осының барлығы көптеген жағдайларда клиникада жалпы жансыздандыратын, әсіресе жергілікті жансыздандырумен амбулаторлық операциялар және ауыратын манипуляциялар жүргізетін поликлиникалық тәжірибелерде қолдануға кедергі келтіреді /67/. Қазіргі тенденцияға байланысты емханаға стационардан ауырлық орталықтарына тасымалдаудағы жергілікті жансыздандыру мәселесі үлкен маңыздылықты алады.
Жергілікті анестетиктерді қолдануда көптеген жанама эффекттер, тән анальгетиктер, жеке алғанда дәріге тәуелділіктен құтылуға мүмкіндік береді, яғни есірткі сияқты мұндай әлеуметтік мәселені шешуде оң роль атқарылуы күмәнсіз /68/. Осыған байланысты жаңа көптеген эффективті, улылығы аз және ұзақ уақыт әсер ететін жергілікті анестетиктерді іздеу өзекті болып табылады.
Органикалық қосылыстардың арасынан жергілікті анестетиктерді синтезі үшін қолданылуы мүмкін пиперидин туындылары үлкен қызығушылықты тудырып отыр /69/.
Пиперидин сақинасы − көптеген алкалоидтардың құрылымды фрагменті юолып табылады, мысалы атропин, кокаин, лобелин, кониин , пельтьерин. Пиперидин алғаш рет пипериннен бөлініп алынды − қарабұрышты алкалоиды. Пиперидин пипидиннің тотықсыздануынан алынып, конденсация реакциясында катализатор ретінде қолданылады. Пиперидин туындылары жергілікті жансыздандыру және спазмолиттік құралдар ретінде дәрілік препараттар сияқты қолданылады. Пиперидин есірткі және психотропты заттардың IV (прекурсор) тізіміне кіреді.
Пиперидин туындыларының арасынан кокаинды ауыстыратын эйкаин деп атпен шығатын оксипиперидиннің бензой эфиріне деген қызығушылық тудыруда. Ғылыми химия ойы кокаинның құрылысын анықтағаннан кейін ғана келді. Эйкаиндар өзінің құрылысымен соңғы болып еске салады, бірақ олар едәуір оңай. Кокаин тәрізділер жансыздандырғыш әсерге ие болады.
α, α 1 -Триметил хлорсутекті тұзын, γ- ұсынатын иллюстрациялар үшін эйкаин В құрылымын төмендегідей келтіруге болады /70/:
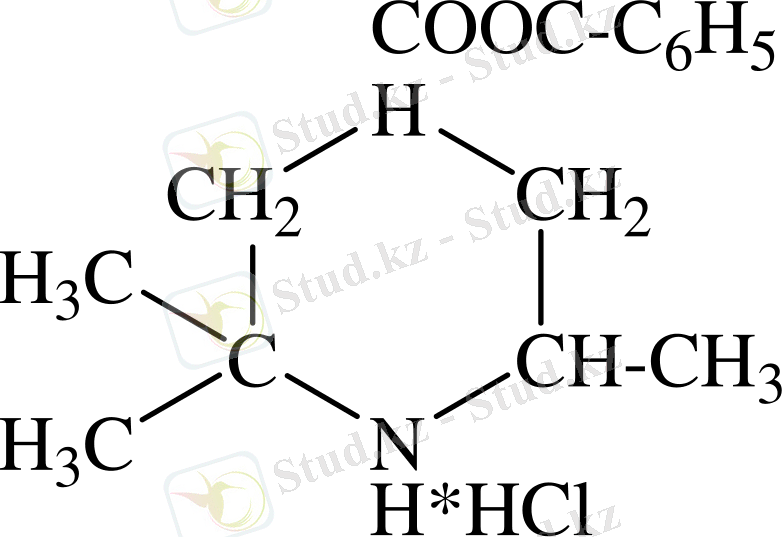
Лидол (долантин, демерол, мепередин) − N-метил-γ-фенил-γ-пиперидинкарбон қышқылының этил эфирінің тұзқышқылды тұзы болып табылады.
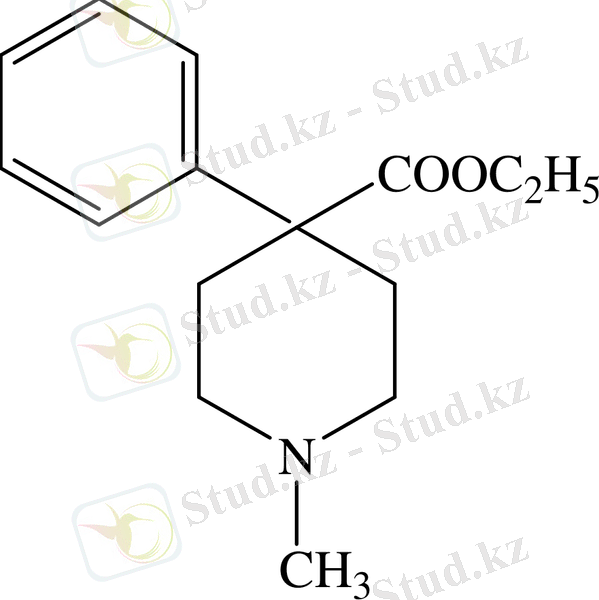
Лидол - ақ кристалды ұнтақ, балқу температурасы 185-188, 5˚; суда және спирттер жеңіл ериді, ал эфирде қиын ериді,
Лидол алғаш рет атропинге құрылымы жағынан ұқсастығы бар пиперидин туындылаының арасынан антиспазмолиттерді іздестірген кезінде 1937 жылы алынған болатын. Бұл түрдегі қосылыстардың спазмолиттік және жансыздандырғыштық қасиеттері бар екені анықталды.
Лидолда спазмолиттік (папаверинді- және атропинтәрізді) және анальгетикалық (морфинтәрізді) әсерлері бірдей болып келеді, бұл препаратқа үлкен практикалық мән әкеледі. Ол морфинді ауыстырғыш сияқты кең көлемде қолданылады, әсіресе тегіс мускулатура түйілулерге (бүйрек, бауыр, ішек түйнегі, тамыр жүйесінің спастиялық күйлері - мигрень, стенокардия және тағы басқалар) байланысты қатысты ауруларда.
Лидол скополаминмен қатар бала тууда жансыздандыру ретінде де қолданылады.
Лидол морфинге қарағанда интенсивтілігі бәсең және аз уақыт әсер етеді. Алайда опиын препаратын толығымен ауыстыра алмайды, бірақ лидолды қолданғанда морфин, пантоион және басқа есірткілерді қолдануды біршама қысқартады.
Лидолдың аналгетик ретінде біршама кемшіліктері бар: тыныс алу және қан айналымына ауыр тиетін ықпалы және әдетке айналу мүмкіндігі (ұзақ уақыт қолданғанда) /71/.
Күшті аналгетикті және спазмолитті әсері бар препараттар N-алкил-γ-фенил-γ-пиперидол күрделі эфирлерінің арасынан табылды, яғни «төңкерілген» түрде сияқты қатысатын құрамында лидол бар күрделі эфирлі топтамасы.
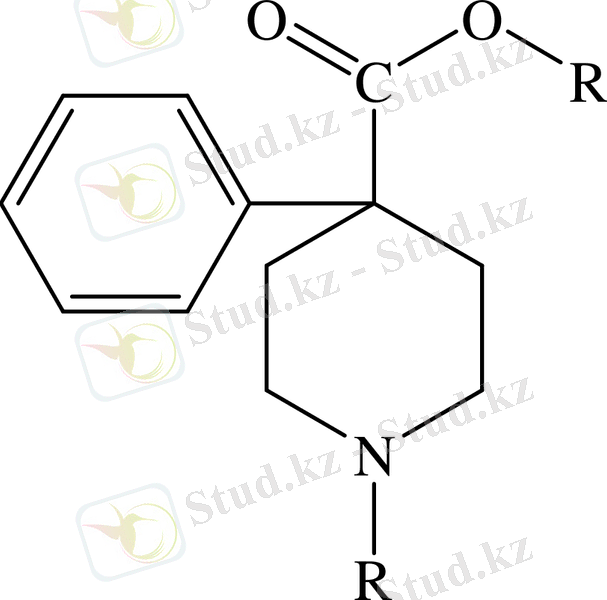
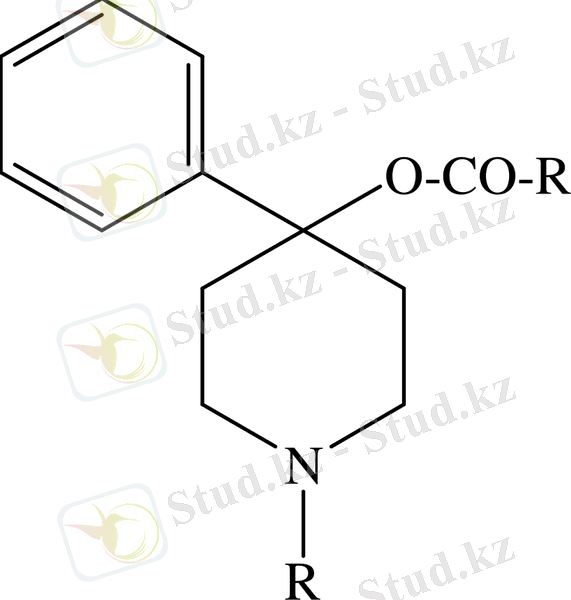
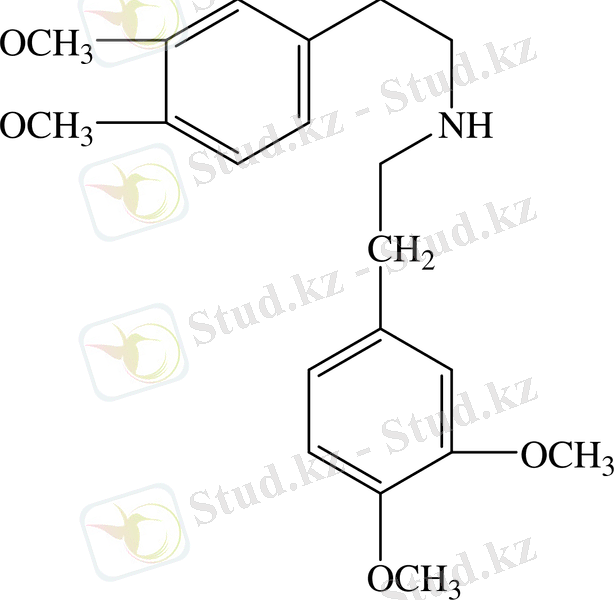
Бұл қатардағы бағалы препараттардың бірі И. Н. Назаровтың синтездеген промедол (1, 2, 5-триметил-4-фенил-4-пиперидол пропион эфирі) болып табылады /72/.
Промедол күшті анагетикалық белсенділікке ие препараттардың бірі. Промедол ЦНС-тегі әсері жағынан морфинге жақын: ол қатерлі импульстердің ЦНС-нің қабылдауын азайтады, шартты рефлексін жаншиды. Басқа наркотикалық аналгетиктер тәрізді ЦНС-тің жиынтық қабілеттілігін азайтады, новокаин және басқа жергілікті анестетиктердің анестезирлеуші әсерін күшейтеді. Промедол көбінесе, қатерлі синдромды басатын айрықша қасиетіне байланысты ұйықтататын эффект көрсетеді.
Морфинмен салыстырғанда промедол тыныс алу орталығына аз қатер төндіреді, сондай-ақ жылжымалы жүйке орталығын және құстыратын орталықты азайтады. Ішкі органдардың тегіс мускулатурасына аздап спазмолиттік әсер етеді, бірақ бұдан миометрияның тонусы жоғарылайды және оның қысқаруы күшейеді.
Промедол фенилпиперидиннің синтетикалық туындылары болып табылады және химиялық құрылысы бойынша морфин молекуласының фенил-N-метилпиперидинді бөлігіне ұқсас болып қаралуы мүмкін.
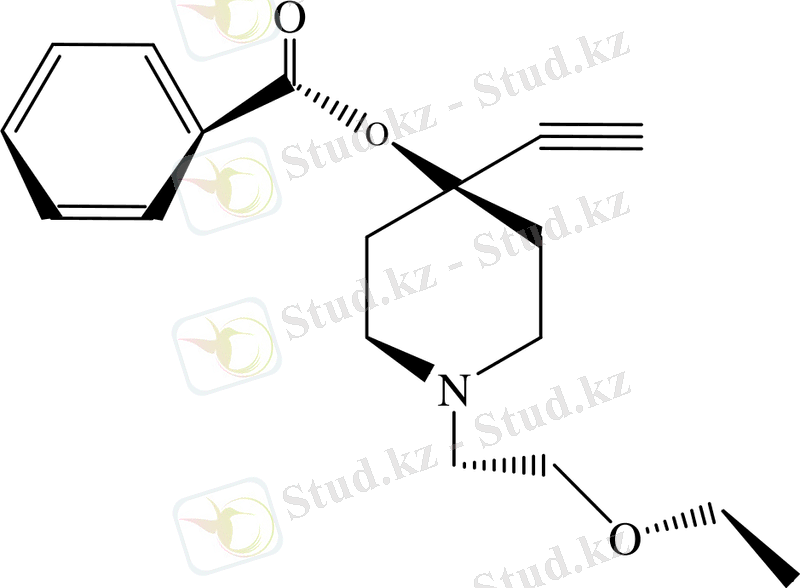
Казкаин - эффективтілігі жоғары жергілікті анестетик және антиритмик. Казкаин препараты Новокузнецк ХФЗҒИ, С. Д. Асфендияров атындағы Қазақ ұлттық медицина университеті және Ә. Б. Бектұров атындағы химия ғылымдары Институтының ғалымдары мен мамандарының күшімен бірлесіп жасалды.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz