Изопроцестер: изотермиялық, изобаралық, изохоралық, адиабаттық және политроптық процесстер


ҚАЗАҚСТАН РЕСПУБЛИКАСЫНЫҢ БІЛІМ ЖӘНЕ ҒЫЛЫМ
МИНИСТРЛІГІ
ШӘКӘРІМ атындағы СЕМЕЙ МЕМЛЕКЕТТІК УНИВЕРСИТЕТІ
Инженерлік-технологиялық факультеті
(факультет атауы)
«Техникалық физика және жылуэнергетика»кафедрасы
(кафедра атауы)
Мамандыққа кіріспе
(пән атауы)
СӨЖ
(жұмыс түрі)
Изопроцесс түрлері
(жұмыстың тақырыбы)
Орындаған: Сералиева А. С
Топ: ТЭ-517
Тексерген: Сейсенбаева М. К
Семей
2015
Мазмұны
КІРІСПЕ1. ГАЗ ЗАҢДАРЫ4
1. 1. Изотермиялық процесс5
1. 2. Изобаралық процес6
1. 3 Изохоралық процесс6
1. 4. Адиабаталық процесс7
Қортынды10
Пайдаланған әдебиеттер11
Идеал газ күйі теңдеуінің көмегімен газ массасы және үш параметрдің - қысым, көлем немесе температура - біреуі өзгермей қалған жағдайдағы процестерді зерттеуге болады. Газдың бір параметрінің 1 мәні тағайындалып, қалған ек1 мәні арасындағы сандық, тәуелділікті айқындайтын заңдарды газ заңдары деп атайды.
Параметрлердің біреуінің мәні өзгермей қалған кезде өтетін процестер изопроцестер деп аталады. Изопроцестер табиғатта кең таралған және техникада жиі пайдаланылады.
Шынында да, ешбір процесс қандай да болмасын қатаң тағайындалған бір параметрдің мәнінде жүрмейді. Температураның, қысымның, немесе көлемнің тұрақтылығын бұзуға әсер ететін қандай да бір жағдайлар болады. Тек лабораториялық жағдайларда ғана кайсыбір параметрлердің тұрақтылығын тым дәлірек сақтағга болады, бірак жұмыс істейтін техникалық кұрылғылар-да және табиғатта бұл іс жүзінде әсте мүмкін емес. Изопроцесс-бұл нақты процестің идеалдандырылған моделі. Ол шындықты тек жуық қана бейнелейді
1. 1. Изотермиялық процессТемпература тұрақты болғанда мак-роскопиялық, денелердің термодинамикалық, жуйесі күйінің өзгеру процесін изотермиялық, деп атайды . Газ температурасын тұрақты етіп ұстау ушін ол температурасы тұрақты болып тұратын үлкен жүйемен- термостатпен -жылу алмасатындай болуы қажет. Өйткені сығылғанда немесе ұлғайғанда газдың, температурасы өзгеретін болады, Егер атмосфералық ауаның, температурасы бүкіл процесс барысында елеулі өзгермесе, онда ол термостат қызыметін атқара алады. (1-сурет ) Егер газдың температурасы өзгермесе, онда оның берілген массасы ушін газ қысымының көлемге көбейтіндісі тұрақты болады.
Бұл заңды тәжірибе жүзінде ағылшын ғалымы Р. Бойль(1627-1691), одан біраз кейінірек француз ғалымы Э. Мариотт (1620-1684) ашты. Сондықтан ол Бойль - Мариотт заңы деп аталады.
Бойль-Мариотт заңы кез келген газ ушін, сондай-ақ олардың қоспасы үшін де, мысалы, ауа ушін де дұрыс. Тек атмосфералық қысымнан бірнеше жүз есе жоғары қысымдарда ғана бұл заңнан ауытқу елеулі түрде байқалады.
Атмосфералыққа жақын қысымдарда Бойль-Мариотт заңының дұрыстығына алдыңғы параграфта сипатталған қондырғ ының көмегімен көз жеткізуге болады.
Тұрақты температурада газ қысымының көлемге тәуелділігі график түрінде изотерма деп аталатын қисық сызық арқылы кескінделеді. Газдың изотермасы қысым мен көлемнің арасындағы кері пропорционал тәуелділкті өернектейді. Қйсык сызықтың мұндай түрін математикада гипербола деп атайды.
Әр түрлі тұрақты температураға әр түрлі изотермалар сәйкес келеді. ЕгерV=const болса, температура жоғарылағанда қысым күй теңдеуіне
pV=
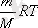 (1)
(1)
Компрессормен ауаны сығу процесін немесе ыдыстары ауаны сорып шығарғанда поршень астындағы ауаның ұлғаюын - шамамен изотермиялық процесс деп есептеуге болады. Шынында, бұл жағдайда температура өзгеретіні рас, алайда алғашқы жуықтауда ондай өзгерісті елемеуге де болады.
1. 2. Изобаралық процесҚысым тұрақты болғанда термодинамикалық, жүйе күйінің өзгеру процессі изобаралық деп аталады қысымы өзгермесе газдың кез келген күйінде көлемнің температурараға қатысы тұрақты болып қалады. P=const болғанда,
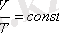 (2)
(2)
Егер газ қысымы өзгермесе, берілген массалы газ ушін көлемнің температураға қатысы тұрақты болады .
Бұл заңды 1802 жылы француз ғалымы Гей-Люссак (1778-1850) тәжірибе жүзінде тағайындаған және сондықтан ол Гей-Люссак заңы деп аталады. P=const болғанда, қатысқа сәйкес тұрақты қысымда газдың көлемі температураға сызықтық тәуелді болады, яғни:
V=const. T (3)
Бұл тәуелділік график түрінде изобара деп аталатын түзумен кескінделеді
1. 3 Изохоралық процесс
Изохоралық процесс. Газдың көлемі тұрақты, яғни V=const., ал температура(T) мен қысым(V) өзгеретин термодинамикалық процесті изохоралық процесс деп айтады.
Изохоралық процессті көлемі өзгермейтін герметикалық (тұмшаланған) ыдыстағы газдар мен сұйықтықтарда жүзеге асыруға болады. Дене көлемінің өзгеруіне ішкі энергиясының өзгеруі жылудың жұтылуы не шығуы есебінен атқарылады. Температураның өзгеруіне байланысты газдың (сұйықтықтың) қысымы да өзгереді. Изохоралық процесс кезінде идеал газдың қысымы температураға пропорционал (Шарль заңы) болады.
Нақты (идеал емес) газда Шарль заңы орындалмайды. Өйткені газға берілген жылудың белгілі бір бөлігі бөлшектердің өзара әсерлесу энергиясын арттыруға жұмсалады. Ал қатты денедегі изохоралық процессті атқару техникалық жағынан едәуір күрделі болып келеді. Сығылғыштығы өте аз қатты денедегі кез келген изотермалық процесті, бірнеше ондаған килобар қысымға дейін, изохоралық процесс деп есептеуге болады.
1. 4. Адиабаталық процесс
Адиабаталық процесс-қоршаған ортамен жылу алмаспайтын физикалық жүйеде өтетін термодинамикалық процесс. Адиабаталық процесс жылу өткізбейтін (адиабаталық) қабықшалармен қоршалған жүйелерде өтеді деп есептелінеді. Сыртқы орта мен жүйе арасында жылу алмасып үлгере алмайтындай уақытта тез өтетін процестер (жылу оқшаулағыш қабықшалары болмайтын) адиабаталық процесс ретінде қарастырылады. Оған мысалы, дыбыстың ауада таралуы, жылу қозғалтқыштарының цилиндрі ішіндегі газдың сығылуы (немесе ұлғаюы) т. б. жатады. Газ сығылғанда температура көтеріледі, ұлғайғанда- төмендейді. Адиабаталық процесс қайтымды және қайтымсыз процесс түрінде өтуі мүмкін. Шинаны немесе допты үрлеу кезінде сорғының ауаны тез сығыуы салдарынан ол қызады. Газдың ішкі энергиясы оны сығатын сыртқы күштердің атқаратын жұмысы есебінен артады. Газдың тез ұлғаюы кезінде оның салқындау құбылысын бақылыуға болады. Ол үшін үлкен шыны бөтелкеге су құйып, түтін енгізеді және сорғы көмегімен оған айдайды. Бұл кезде бөтелкедегі судың жоқ болып кетуі булануы ондағы ауа температурасының жоғарлағаның дәлелі болып табылады. Бөтелкедегі ауа қысымының ауа берліктей артуы, оның тығының атылып кетуіне әкеледі. Ауа жылдам ұлғая отырып бөтелкеден шыға бастайды, ал бөтелкеде қалың тұман пайда болады, ол ұлғаю кезіндегі ауаның салқындағаның көрсетеді.
Газ ұлғайып, өзінің ішкі энергиясының кему есебінен жұмыс істейді. Тез сығылу немесе ұлғаю кезінде қоршаған ортамен жылу алмасып үлгермейтіндігі қарастырылған мысалдардан көрінеді. Бұл жағдайларда аз уақат аралығында Q=0 деп санап, бұл процестерді адиабаталық процесстер ретінде қарастырамыз. Мұнда термодинамиканың 1 заңы U+A=0 немесе U=-A түрінде өрнектеледі. Бұл адиабаталық процесс кезіндегі газдың сығылуы, оның ішкі энергиясының артуын тудыратынын және теріс жұмыс атқарлатының көрсетеді.
Ұлғаю кезінде газдың ішкі энергиясы кемиді, оның есебінен оң жұмыс атқарылады. Адиабаталық процессті графикте адиабата деп аталады. Іштен жану қозғылтқыштарының цилиндіріндегі жану қоспасының поршеньмен сығылуын немесе ондағы отын жанғанда газ тәрізді өнімдерінің жылдам ұлғаюын адиабаталық процесстерге жатқызады. Оларға: бомба, снаряд, миналардың жарылыстары. Адиабаталық процесс - атмосферада адиабаталық процесс - қоршаған ортамен жылу алмасуынсыз болып тұратын (жер бетімен, ғарышпен, жанасатын ауа массасымен) ауаның термосерпіндік өзгерісі. Шуақты күні Жерден қызған ауа қабаттары жылдам көтеріледі. Тығыз емес қабаттарда олар ұлғаяды да, салқындайды, түйдек бұлттар пайда болады. Айнымалы жұлдыздардың жарқырау периодының өзгерісі олардың сыртқы қабатарының адиабаталық ұлғаюы иен сығылуының қайталанатын процестріне байланысты. Бұл процесстер айнымалы жұлдыздар-цефеидтерде дәлме -дәл белгілі уақыт аралығында қайталанады. Цефеидтің қабығы ұлғайғанда, оның атемпературасы мен қысымы тез төмендейді. Қабықшаны сыққанда, ондағы газдың температурасы мен қысымы бастапқы шамасына дейін артады. Әрі қарай бұл процесстер қайталана береді. Мұндай процестердің ұзақтығы, процесстің аумағына байланысты.
Адиабата (гр. adiabatos- өтпейтін) - адиабата - қайтымды (адибаттық) процесті бейнелей алатын қисық, графикалық сызық
Адиабаттық процесс кезінде система сыртқы денелерге қарсы жұмысты тек өзінің ішкі энергиясының есебінен ғана атқара алады дегенді білдіреді. Ал керісінше, адиабаттық процесс кезінде сыртқы денелер системаға жұмыс атқаратын болса оның ішкі энергиясы артады. Егер газ адиабаттық ұлғаю кезінде қоршаған ортаға қарсы жұмыс атқаратын болса, онда оның ішкі энергиясы азаяды. Демек бұл жағдайда газ салқындау керек.
Термодинамиканың екінші бастамасы жылу машиналарының жұмыс істеу принциптерін байқаудан қалыптасты. Жылу машинасының термиялық п. ә. к. η=0 болуы үшін Q2=0 шарты орындалуы керек, яғни берілген жылу мөлшерінің көп бөлігі жұмысқа айналса, машинаның соғұрлым тиімді болатыны анық. Сөйтіп, жылу машинасы тек қыздырғыштан алынған жылу мөлшері Q1 арқылы жұмыс өндірер еді, ал бұл мүмкін емес. Француз инженері С. Карно (1796-1832) 1824 жылы жылу машинасының жұмыс істеуі үшін міндетті түрде температурасы әртүрлі екі жылу көзі болуы керек екенін дәлелдеді.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz