Микрогетерогенді жүйелер: қасиеттері, жіктелуі және практикалық маңызы


ҚАЗАҚСТАН РЕСПУБЛИКАСЫ БІЛІМ ЖӘНЕ ҒЫЛЫМ
МИНИСТРЛІГІ
ШӘКӘРІМ атындағы СЕМЕЙ МЕМЛЕКЕТТІК УНИВЕРСИТЕТІ
БӨЖ
Тақырыбы:
"Микрогетерогенді жүйелер және олардың практикалық маңызы"
Орындаған: ХО - 303 тобының студенті Бабешкина Анна
Тексерген: Баяхметова Бұлбұл Баяхметовна
Семей 2015ж
Мазмұны:
Коллоидты химия және дисперстілік туралы түсінік
Эмульсия
Коллоидты химияның орны
ДИСПЕРСТІЛІКБарлық ғылым не өндіріс салалары сияқты коллоидты химия да өздерінде кездесетін өзіндік ерешеліктер мен қасиеттерге, өлшемдер мен көрсеткіштерге орай жіктеле келіп, сұрыпталады. Ондағы қайсыбір қасиеттер бір-біріне ұқсас болғандықтан, олар өзара бірігіп кетеді. Мұны кеңістікте орналасқан денемен де теңестіруге болады, өйткені осы дененің кеңістіктегі нақтылы орнын табу үшін үш өлшемді координатаны не олардың проекциясын пайдалану қажет. Демек, коллоидты жүйені сипаттау үшін оны әртүрлі қасиет, ерекшелік тұрғысынан жіктеу керек. Солардың бірі дисперстілік.
Дисперстілік бойынша немесе дисперсті жүйедегі дисперсті фаза өлшемі бойынша, яғни дисперсті бөлшектің дисперсті система-дағы дисперсті фаза өлшемі бойынша, яғни дисперсті бөлшектіц өлшемін, ұнтақтылығын көрсететін өлшеміне орай жіктеу көрсетілгендей бөлінеді: ірі дисперсті, жоғары дисперсті (микрогетерогенді), коллоидты және молекулалық. Мұндағы ірі дисперсті системаның бөлшектері сүзгіш қағаздан өтпейді, кәдімгі микроскопта көрінеді, өзінен жеңіл ортада жүзгін ретінде аз уақыт болып, тез отырады, ал өзінен ауырлау ортада жүзгін ретінде жүре береді. Система жоғары дисперсті болса, бір-шама тұрақты, бөлшегі ұсақтау, сүзгіш қағаздан оңай өтсе де жар-тылай өткізгіштерден өтпейді, кәдімгі оптикалық микроскопта көрінбейді, дисперсті ортада жүзгін ретінде ұзақ сақталады.
Агрегаттық күй. Белгілі үш агрегаттық күйге сәйкес дисперстік системаны 9 түрге бөлуге болады (1-кесте) . Әдетте әрбір түрді ондағы бос әріптерді қысқартып, бөлшек алымына дисперсті фазаны, ал бөлшек бөліміне дисперсті ортаны жазады. Заттағы дисперсті фазаның дисперсті ортада шекті ерігіштігі - дисперсті системаның пайда болуындағы қажетті жай. Мысалы, дисперсті г/г системасындағы газдардың бір-бірінде шексіз еритіндігінен әдетте көріне бермейді.
1-кесте
Жоғары дисперсті системаларды зольдер дейді және осыған орай дисперсті ортаның сипатына сәйкес гидрозольдер, органика-лық зольдер, аэрозольдер болып бөлінеді. Ал ірі дисперсті системадағы қатты фазаның сұйық ортада таралуын жүзгіндер (сус-пензиялар), ал фаза да, орта да сұйық болса, оны эмульсиялар дейді.
Құрылым. Барлық дисперсті системалар құрылым жағынан еркін (бос) дисперсті және біріккен (байланысқан) дисперсті бо-лып бөлінеді. Еркін дисперсті система дегеніміз - дисперсті фаза мен дисперсті орта бірімен-бірі өзара байланыспай әрқайсысы бос жүретін дисперсті система. Оған жүзгіндер, эмульсиялар, аэро-зольдер мен жалпы зольдер жатады. Дисперсті фаза мен дисперсті орта өзара берік байланысқан системаларды байланысқан дис-персті система дейді. Оған капиллярлі кеуек заттар, диафрагмалы денелер, жұқа пленка - мембраналар, кәдімгі полимерлер, қатты ерітінді - қорытпалар жатады.
Фазааралық әрекет. Дисперсті фаза мен дисперсті ортадағы заттар фазааралық беткі қабатта әрқашанда молекулааралық әсерлесу күшінің есебінен әрекеттесіп жатады және мұндағы әре-кеттесу дәрежесі әртүрлі болуы мүмкін. Мінеки, осы әрекеттесу шамасына орай дисперсті системалар лиофильді және лиофобты болып бөлінеді. Лиофильді системалар тобына жататын дисперсті системадағы дисперсті фаза мен дисперсті орта өзара әрекеттеседі. Мүның нәтижесінде жалпы химиядан белгілі сольватацияға (еріт-кіш су болғанда гидротация) ұқсас, дисперсті фаза бөлшегінің ай-наласында дисперсті орта бөлшектерімен қоршалған қабат лайда болады. Ал, лиофобты системалар тобына енетін дисперсті фаза мен дисперсті ортадағы заттар өзара нашар әрекеттеседі.
Фазалық өзгешелік. Жоғары молекулалық қосылыстардың ері-тінділері нағыз молекулалық ерітінді болса да оларға коллоид-ты күйдің көптеген белгілері тән. Мысалы, жоғары молекулалық қосылыстар өздігінен ерігенде әуелі жекеленген макромолекула-ларға ыдырап бірфазалы, гомогенді, тұрақты және қайтымды сис-тема құрайды. Ал, дисперстілік система қасиетіне едәуір әсер ететіндіктен, жоғары молекулалық қосылыс ерітінділері жоғары дисперсті, гетерогенді системаларға тән ортақ қасиеті болуы ке-рек. Расында да жоғары молекулалық қосылыс ерітінділері диф-фузия жылдамдығы, ультра сүзгіштен өтпеуі, құрылымы, оптика-лық, электрлік қасиеті тарапынан алғанда, олар нағыз ерітіндіден гөрі коллоидты системаға жақын. Дисперсті системаларды тағы да үлкен екі топқа бөлуге болады: жүзгіндер (суспензиодтар) және молекулалық коллоидтар. Жүзгіндер дегеніміз өзін қоршаған ортадан анық белгіленген фи-зикалық шегі бар, атомдар немесе молекулапардың бірігіп өз алдына жеке агрегат күраған бөлшектерден тұратын жоғары дис-персті, гетерогенді системалар. Ал, молекулалық коллоидты сис-темалар дегеніміз, жеке кинетикалық өлшем ретінде болатын мо-лекулалардың сольваттануын өздігінен қүрайтын, тұрақты және қайтымды бір фазалық гомогенді системалар. Мұндағы ірі молекулалардың өлшемі коллоидтық дисперстілік өлшеміне шамалас болады. Мінеки осы тұрғыдан алғанда жоғары молекулалық қо-сылыс ерітінділері дисперсті молекулалық коллоидты системаға /катады, ал олардың гомогенділігі беткі бос энергия, фазааралық шек жайлы ойлауға да мүмкіндік қалдырмайды. Бұл да тек олардың өзіне ғана тән қасиет.
Эмульсиялар .
Эмульсия деп - бір-бірінде ерімейтін екі сұйықтан түзілген дисперсті жүйені айтады. Жүйеге агрегаттық тұрақтылық беру үшін беттік - активті заттар (ПАВ) енгізеді, олар эмульсия стабилизаторы - эмульгатор ролін атқарады.

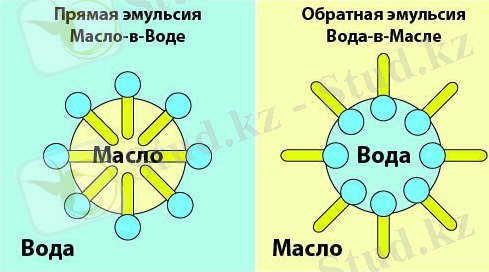
Тура май-су (м/с) және кері су-май (с/м) эмульсиялар болады.
Эмульсияларды к о н ц е н т р а ц и я л а у және д и с п е р г и р л е у әдістерімен алуға болады. Дисперсионды әдісте роторлы - пульсационды аппараттар голюгенизаторлар және т. б. көмегімен үздікті сілку және механикалық диспергирлеу әдістері қолданады.
Седиментатция - дисперсті фаза талшықтарының бетке қалқып шығуы немесе тұнуы (мысалы, қаймақты сүттен бөлу) . Бұл кезде эмульсияның толық бұзылуы жүрмей, бірі екіншісіне қарағанда дисперсті фазаға бай, екі эмульсия түзіледі.
Коалесценция - эмульсияның толық бұзылуы, таза түрде екі сұйық фазаның бөліуне әкеледі.
Инверсия (фазалар айналуы) - бұл бір эмульсия түріне араластыра отырып көп мөлшерде басқа типті эмульсияға айналуы.
Эмульсиялар өзара араласпайтын екі сүйықтан пайда болады, олардың біреуі дисперстік фазаның, ал екіншісі дисперсиялық ортаның ролін атқарады. Дисперстік фаза тамшылар түрінде дисперсиялық ортада ілінген күйде болады, көбінесе судан және май деп аталатын сұйықтан тұратын эмульсиялар жиі кездеседі. Эмульсиялар 2 түрлі болып бөлінеді: судағы май (м/c) және майдағы су (с/м) .
Тұрақтылығы жоғары концентрленген эмульсия дайындау үшін табиғаты гидрофобты және гидрофильді болып келген стабилизаторлар (эмульгаторлар) қолданылады.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz