Жылутехника негіздері: қысымнан энтропияға дейін


ҚАЗАҚСТАН РЕСПУБЛИКАСЫНЫҢ БІЛІМ ЖӘНЕ ҒЫЛЫМ МИНИСТРЛІГІ
СЕМЕЙ қаласының ШӘКӘРІМ атындағы МЕМЛЕКЕТТІК УНИВЕРСИТЕТІ
Инженерлік-технологиялық факультет
(факультеттің атауы)
«Техникалық физика и жылуэнергетика» кафедрасы
(кафедраның атауы)
СӨЖ
(жұмыстың аты)
Мамандыққа кіріспе
(пән аты)
Жылутехниканың теория негіздері. Қысым, температура, көлем, энтропия, энтальпия
(жұмыстың тақырыбы)
Орындаған: ТЭ-517 тобы студенті Тексерген: Сейсенбаева М. К.
(Оқытушының аты-жөні)
Тулегенов М. К.
(қолы) (Студенттің аты-жөні)
(баға) (күні) (қолы) (күні)
Семей қ.
- ж.
1. Қысым 2
1. 1 Сыналанған қысым 3
2. Температура. 3
2. 1 Температуралық шкаласы 4
2. 2 Кельвин температуралық шкаласы 4
2. 3 Ремюр температуралық шкаласы 4
2. 4 Фаренгейт темературалық шкаласы 4
2. 5 Цельсий темературалық шкаласы 4
3. Көлем4
4. Энтропия 5
4. 1 Энтропия туралы ұғым 5
5. Энтальпия7
Пайдаланылған әдебиеттер
1. Қысым
Қысым бір дене екінші дене бетіне (мысалы, ғимарат іргетасының грунтқа, сұйықтықтың ыдыс қабырғасына, қозғалтқыш цилиндріндегі газдың піспекке, т. б. ) әсер еткенде пайда болатын қалыпты күштің (дене бетіне перпендикуляр) қарқындылығын сипаттайтын физикалық шама. Егер денеге әсер ететін күш оның бетіне біркелкі таралса, онда қысым (р) былай өрнектеледі:
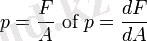 (1)
(1)
Мұндағы S - дене бетінің күш түсетін бөлігінің ауданы, F - сол бөлікке перпендикуляр түсірілген күштердің қосындысы. Күш біркелкі таралған жағдайда қысым дене бетінің барлық нүктесінде бірдей болады, ал күш біркелкі таралмаса, онда қысым бір нүктеден екінші нүктеге өткен сайын өзгеріп отырады. Тұтас, үздіксіз орта үшін сол ортаның әрбір нүктесінің қысымы туралы ұғым енгізіледі. Бұл ұғым сұйықтық пен газ механикасында маңызды рөл атқарады.
Тыныштықтағы сұйықтықтың кез келген нүктесінің барлық бағытындағы қысымы бірдей болады. Бұл жағдай қозғалыстағы идеал (үйкеліссіз қозғалатыс) сұйық пен газ үшін де орындалады. Тұтқыр сұйықтықтың берілген нүктедегі қысымы ретінде өзара перпендикуляр үш бағыттағы (х, у, z - осьтері бағытындағы) қысымның орташа мәні р = (рх+ру+рz) /3 алынады. Газдардың кинетикалық теориясы бойынша, газды ортадағы қысым жылулық қозғалыстағы газ молекулаларының бір-бірімен, газдағы денелермен және ыдыс қабырғаларымен соқтығысуы кезінде импульстың берілуімен байланысты болғандықтан мұны “жылулық” қысым деп атайды. Ол газдың абсолют температурасы (Т) мен бірлік көлемдегі газ молекулаларының санына (n) пропорционал: р = nkT, мұндағы k = 1, 38. 10-23 Дж/К - Больцман тұрақтысы.
Сұйықтықтар мен қатты денелердің қысымы денелердің бір-біріне жақындауы кезінде олардың атомдарының бірін-бірі тебуі нәтижесінде пайда болады. Мұны “суық” қысым дейді. Тыныштықтағы сұйықтық салмағының әсерінен оның ішінде h тереңдікте пайда болатын қысымды гидростатикалық қысым деп атайды: р = rgh, мұндағы r - сұйықтықтың тығыздығы, g - еркін түсу үдеуі. Егер сұйық бетіне сырттан р 0 қысымы түсірілетін болса, онда h тереңдіктегі сұйық қысымы: р = р 0 + rgh өрнегімен анықталады. Қысым физикалық, химиялық, механикалық, биологиялық, т. б. құбылыстарда елеулі рөл атқарады; манометр, барометр, вакуумметр тәрізді құрылғылардың және әр түрлі қысым датчиктерінің көмегімен өлшенеді. Қысымның Бірліктердің халықаралық жүйесіндегі өлшем бірлігі - Паскаль (Па) . 1 Па = Н/м2. Бірліктердің МКГСС жүйесінде кгс/см 2 , сондай-ақ жүйеден тыс өлшем бірліктері: атмосфералық (физикалық атмосфера), мм сынап бағанасы, мм су бағанасы.
1. 1 Сыналанған қысымСыналанған қысым -қатты дене беттерінің арасындағы аралықтағы сұйыққа- быршағының күйін сипаттайтын термодинамикалық параметр.
2. Температура
Температура (лат. temperatura - араластырылуға тиісті, өлшемдес болу, қалыпты күй) - макроскопикалық жүйенің термодинамикалық тепе-теңдік күйін сипаттайтын физикалық шама. Егер оқшауланған немесе тұйықталған жүйе термодинамикалық тепе-теңдік күйде болса, онда оқшауланған немесе тұйықталған жүйенің кез келген бөлігінде температура бірдей болады. Ал егер жүйе тепе-теңдік күйде болмаса, онда жылу (энергия) оның температурасы жоғары бөлігінен температурасы төмен бөлігіне қарай ауысып, белгілі бір уақыт өткеннен кейін жүйенің барлық бөліктеріндегі температура өзара теңеседі. Молекула кинетикалық теория тұрғысынан тепе-теңдіктегі жүйенің температурасы сол жүйені құрайтын атомдардың, молекулалардың, т. б. бөлшектердің жылулық қозғалысының қарқындылығын сипаттайды. Мысалы, классикалық статистикалық физиканың заңдарымен сипатталатын жүйе үшін бөлшектердің жылулық қозғалысының орташа кинетикалық энергиясы жүйенің абсолют температурасына тура пропорционал болады. Бұл жағдайда температура дененің жылыну (қызу) дәрежесін сипаттайды. Жалпы жағдайда температура жүйе энергиясының энтропия бойынша алынған туындысымен анықталады және ол әрқашан оң болады. Осылай анықталған температура абсолют температура немесе термодинамикалық шкала температурасы деп аталады. Бірліктердің халықаралық жүйесінде абсолют температураның бірлігіне кельвин (К) қабылданған. Көп жағдайда температураны Цельсий шкаласы (t) бойынша өлшейді. Ал t және Т бір-бірімен: t=T-273, 15К теңдігі арқылы байланысқан (мұнда Цельсий градусы кельвинге тең) . Дене температурасы термометр арқылы өлшенеді. 2. 1 Температуралық шкаласыТемературалық шкаласы- қалыпты кысым кезінде мұздың еру нүктесі нөл градусқа, ал қайнау нүктесі - 80 градусқ теӊ.
2. 2 Кельвин температуралық шкаласыКельвин температуралық шкаласы- температура бірлігі ретінде кельвин алынатын термодинамикалык температуралык шкала.
2. 3 Ремюр температуралық шкаласыРемюр температуралық шкаласы - қалыпты қысымда мұздың еру нүктесі нөл градуска, ал судың кайнау нүктесі 80 градуска сәйкес келетін температуралык шкала. Муздын еру температурсы 0 градуска сайкес келеды.
2. 4 Фаренгейт темературалық шкаласыФаренгейт темературалық шкаласы - қалыпты қысымда мұздың еру нүктесі 32 градуска, ал судың кайнау нүктесі 212 градуска сэйкес келетін температуралық шкала.
2. 5 Цельсий темературалық шкаласыЦельсий темературалық шкаласы - калыпты кысымда мұздың еру нүктесі нөл градуска, ал судың кайнау нүктесі 100 градуска сәйкес келетін температуралык шкала.
3. Көлем
Көлем - геометриялық денелердің кеңістіктен алатын бөлігін сипаттайтын шама. Көлем геометриялық денелерге байланысты негізгі шамалардың бірі болып табылады. Қарапайым жағдайда Көлем дене ішіне сиятын бірлік кубтардың санымен өлшенеді. Ежелгі Шығыста] (Вавилон, Мысырда) денелердің Көлемін есептеуде түрлі математикалық ережелер қолданылды (мысалы, толық және қиық пирамидалар, цилиндрлер, т. б. ) . Күрделі денелердің Көлемі былай анықталады. Тік бұрышты параллелепипедтің ішіне орналасқан М дене, параллель жазықтықтармен қыры а -ға тең кубтарға бөлінеді. а нөлге тез ұмтылып, шексіз кеми берсін. Vn - М денесіне сиятын кубтар Көлемінің қосындысы, ал Wn - М денесінің ішінде кемінде бір нүктесі болатын кубтар Көлемінің қосындысы болсын. Егер V = Vn және W = Wn шектері өзара тең болса, онда олардың ортақ мәні V осы М денесінің Көлемі деп аталады. Дененің Көлемі мына формула бойынша анықталады:, мұндағы интегралдау кеңістіктің көрсетілген дене орналасқан бөлігін толық қамтиды.
4. Энтропия
Энтропия (грек. еntropіa - бұрылыс, айналу) - тұйық термодинамикалық жүйедегі өздігінен жүретін процестің өту бағытын сипаттайтын күй функциясы. Энтропияның күй функциясы екендігі термодинамиканың екінші бастамасында тұжырымдалады. Энтропия ұғымын термодинамикаға 1865 ж. Р. Клаузиус енгізген. Кез келген А және В күйлеріндегі жүйе Энтропиясы мәндерінің Q - жүйеге күйіδайырымы мына формула арқылы анықталады:, мұндағы шексіз аз квазистатик. болып өзгергенде берілетін жылу мөлшері, Т - жүйенің абс. темп-расы; интрегал екі күйді өзара жалғастыратын кез S=Q/Т. Ал∆келген қайтымды жолмен алынады. Изотерм. процесс жағдайында: кез келген қайтымды жолмен алынатын тұйық процесс үшін: . Соңғы теңдік Q/Т түріндегі толық дифференциал болатындығының қажеттіδЭнтропияның dS= және жеткілікті шарты, ал Энтропия - күй функциясы. Энтропияның абс. мәні термодинамиканың үшінші бастамасы бойынша анықталады және ол бойынша абс. нөл темп-рада кез келген жүйенің Энтропиясы нөлге айналады. Адиабаталық оңашаланған жүйелеріндегі қайтымды процестер кезінде Энтропияның мәні тұрақты болып қалады да, қайтымсыз процестер кезінде Энтропияның мәні артады; барлық реал процестерінде Энтропияның мәні артады (Энтропияның арту заңы) . Статист. физикада Энтропия статист. ) деп аталатын шамамен байланыстырады. Больцман принципінеΩ∆салмақ (, мұндағы k -Ω∆сәйкес: S=kІn Больцман тұрақтысы. Сонымен Энтропия - термодинам. тепе-тендік күйдегі макроскоп. денелерге тән қасиет. Ол бірліктердің халықаралық жүйесінде (СИ) Дж/К арқылы өрнектеледі. Энтропия ұғымы ғылымның көптеген салаларында (физика, химия, т. б. ) маңызды рөл атқарады. С. Асанов
4. 1 Энтропия туралы ұғымЕркінше алынған қайтымды циклды қарастыралық. Циклды бөлшектеу көмегімен, элементарлы Карно циклын шексіз көп санды теңдікті, мына түрде жазуға болады:
- dq1T1= dq2T2
Тұйықталған пішін бойынша, интегралдау кезінде және dq 2 теріс таңбаларын есептеп табамыз.
- ʃdqқайтT1= 0.
Мұндағы, dq қайт - таңбасы кезіндегісі, қаралып отырған айналмалы процесстегі қайтымды түріне, ерекше көңіл аударылуы тиіс. Сонымен, келтірілген жылулықтың интегралды суммасы үшін, қандай болса да, қайтымды циклда нөлге тең. Бұл Клаузиус теңдеуі деп аталады. Жылу динамикасында формуласын Клаузиус теңдеуі деп, ал формуласының оң жақ бөлігінің теңдеуін, Клаузиус интегралы деп атайды. Қандай да тұйық жол үшін, математикалық қажетті және жеткілікті шарт, ол:
- ds = dq/T
толық дифференциал болады. 1-2 еркінше алынған жол бойындағы интеграл, әр уақытта тең:
Шарт бойынша, жылулықты dq жеткізу процессі қайтымды деп есептеледі. Сонымен, S - функция жағдайы. Оны энтропия деп атайды. Формуладағы 1/T үстіңгі көрсеткішінде тұрған, толық емес дифференциал dq үшін интегралдаушы көбейткіш болады. Еркін қайтымды айналмалы процесс үшін алынған формуладан, энтропия S және абсолютты температура Т бар екендігі туралы тікелей қорытынды шығады да, теңдеумен анықталады, оны қайтымды процесстер үшін, жылу динамикасының екінші заңының теңдеуі деп атайды.
Қайтымды изотермиялық процесс (T=const) кезіндегісін теңдеуден табамыз:
Қайтымды адиабатты процесс кезіндегі, dq=0 болғанда:
- ds = 0; S2- S1= 0; S = const.
Қайтымды адиабатты процесс, энтропияның өзгеруін болдырмайды. Сондықтан, оны, изоэнтропийлі процесс деп атайды. Екі рет кездесетін көрсеткіштердің бар болуына сәйкес, сыртқы ортамен, энергетикалық пішіндегі әрекетте болуы. Әрекеттік шарты үшін, байланыстырушы температура Т жылу алмасуы және меншікті энтропия S жолымен, осындай қос көрсеткіштерді құрады. Энтропия экстенсивті (аудитивті) шама болады, себебі энтропия зат, осыған қарағанда оның анықтамасы, осы заттардың (S = mS) санды мөлшеріне пропорционалды, Т мұнда S функциясында болады.
Энтропияның абсолютты шамасын, кейбір тұрақты дәлдікпен есептеуге болады. Себебі, оның абсолютты шамасына емес, энтропиялық өзгеруіне жиі көңіл аударады, оның бастапқы есептелуін шартты түрде таңдайды (әрекеттегі қалыпты физикалық күй, ал су үшін, үш қатты нүкте күйі) . Энтропия бірлігі - Дж/(кгК) . Химиялық реакцияны зерттеу кезінде тұрақтыны білу үшін, энтропияның абсолютты шамасының бастапқысын есептеуі үшін өте үлкен практикалық мәні бар. Нернстің ашқан принципінің атауы ндағы, Нернстің жылулық теоремасымен көрсетілген тұрақтылығын таңдауды іске асыруға болады. Теореманың тұжырымдауына байланысты, қандай да болмасын жүйенің энтропиясы кезіндегі абсолютты нольде, әр уақытта нөлге тең жағдайында қабылдануы мүмкін.
- limsr->0= 0
Бұдан көрінгендей, жүйелер жағдайының T-> К температура кезіндегі, барлық мүмкіндік өзгеруі, энтропияның тұрақты кезінде өтеді. Сондықтан, жүйелер күйінің (қалай болса солай) Т= 0 К кезіндегісін бастапқы есептеу үшін таңдайды. Сонымен, қайтымды процесстер бойынша алынған интеграл
- ,
T=K кезіндегі, қалай болса солай алынған бастапқы жағдайының, А жағдайына арналған энтропияның абсолютты шамасын көрсетеді.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz