Электролиттер мен электролиз: NaCl ерітіндісінің электролизінің теориясы мен өндірістік қолданылуы


Мазмұны
1. Электролиттер және бейэлектролиттер
2. Электролиз туралы түсінік
3. NaCl электролизі
Қорытынды
Пайдаланылған әдебиеттер
1. Элек т ролиттер және бейэлектролиттер
Электролиттер және бейэлектролиттер - кейбір заттардың ерітіндіде тоқ өткізетіні ал, кейбір заттардың сол жағдайларда тоқ өткізбейтіні бәріне белгілі.
Суда ерігенде немесе балқығанда электр тогын өткізетін заттар электролиттер деп аталады. Судағы ерітінділері немесе балқымалары электр тогын өткізбейтін заттар бейэлектролиттер болып табылады.
Электролиттерге негіздер, қышқылдар және тұздардың көбі ал, бейэлектролиттерге көптеген органикалық заттар жатады. Ерітіндіде электролиттер иондарға ыдырайды осының арқасында олар тоқ өткізеді. Ерітіндіде неғұрлым ион көп болса соғұрлым тоқ жақсырақ өтеді.
Электролиттер екінші текті өткізгіштерге жатады. Электролиттердегі электр тогын тасымалдаушылар оң және теріс иондар болып табылады. Электролиттердегі электр өрісін электролиттік ваннаға батырылған электродтар - анод пен катод тудырады. Катодқа қарай қозғалатын иондарды катиондар деп атайды, ал анодқа қарай қозғалатын иондарды аниондар деп атайды.
Электролиттердің ерітіндіде иондарға ыдырауы электролиттік диссоциация деп аталады. Мысалы, NaCl ерітіндіде түгелдей Na+ және Cl- иондарына ыдырайды.
2. Электролиз туралы түсінік
Электролиз - электролит ерітіндісі немесе балқымасы арқылы электр тогын жібергенде жүретін тотығу-тотықсыздану реакциясы.
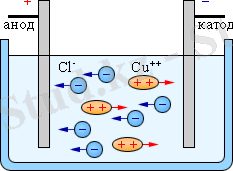
Электролизде катод теріс зарядталады, оған қарай катиондар қозғалып, сол жерде олар тотықсызданады. Анод оң зарядталады, оған қарай аниондар қозғалып, сол жерде олар тотығады. Электролиз процесі - эндотермиялық процесс, себебі ол электр энергиясы арқылы жүзеге асады.
Электролиз кезіндегі химиялық процестер электролит түріне орай, еріткішке байланысты, электрод әзірленген заттың табиғатына сәйкес және басқа да қосымша қосылыстар сияқтыларға қарай сан алуан болуы мүмкін. Электролит арқылы тұрақты ток өткенде катодта электролиттің катионы нейтралды атомға айналып, электродтың беткі қабатында қалады. Мұндай процесс анодта да жүреді және электролит аниондары нейтралданады. Электролиз кезінде пайда болатын нейтрал атомдар мен атом топтары бос күйінде өте тұрақсыз болғандықтан олар өзара не еріткіш пен еріген заттардың моле-кулаларымен химиялық реакцияға түсуі мумкін. Сол сияқты бұл компоненттер электрод әзірленген затпен де химиялық әрекетке түсуі ғажап емес. Электролиз кезінде жүретін барлық реакциялар тотығу-тотықсыздану реакциясының айқын сипатын көрсетеді: катодта тотықсыздану, анодта тотығу процесі жүреді.
Электролиз кезінде система арқылы сыртқы электр көзінен тұрақты ток өткенде, осы ток күшінің әсерінен электродтың күші өзгеруі мүмкін. Мысалы, электродтағы металл пластинасына токтың оң заряды берілгенде, ол ерітіндідегі су молекуласының металмен әрекеттесу процесін жеңілдетеді, сейтіп металл иондары ерітіндіге ауысады, яғни электрод пластинасы ери бастайды. Ал, осы системадағы екінші электрод әзірленген металл пластинасына теріс заряд берілгенде, керісінше, металдың ерітіндіде еруі қиындап, ерітіндідегі металл катионы зарядсызданып, пластинаның беткі қабатына орналасады.
3. NaCl электролизі
NaCl ерітіндісінің электролизі - сулы ерітіндідегі электрохимиялық процестің ең типтік мысалы. Бұл, сонымен бірге, ең қарапайым және экономиялық тиімді бір уақытта үш бағалы өнім - хлор, сутегі және натрий гидроксидты арзан және кеңінен таралған шикізаттан - ас тұздан, алу әдісі. Қазіргі кезде хлор, сутегі және натрий гидроксид өндірісі сулы ерітіндінің электролизімен екі тәсілмен өндіріледі: болат катодымен диафрагмалы және сынап (сұйық) катодымен диафрагмалы емес. NaCl ерітіндісінің электролизінің газтәрізді өнімдері - хлор және сутегі - электролиздің қандай да бір тәсілімен алғанда концентрациясы жоғары және таза болуымен ерекшеленеді. Сынап катодпен электролиз жүргізген кезде үшінші өнім - натрий гидроксидінің да концентрациясы жоғары және химиялық таза. Осы барлық артықшылықтар хлор өндірісінің химиялық әдістерін толық ығыстырып электрохимиялық әдісін кеңінен қолдануға мүмкіндік берді.
Электродтардағы негізгі үдерістер .
NaCl -ң сулы ерітіндісінің электролиз кезінде теориялық түрде катодта
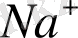 және
және
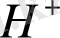 катиондарының, ал анодта
катиондарының, ал анодта
 и
и
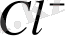 аниондарының разряды болуы мүмкін. Электродтаиондардың қайсысы және қандай ретімен разрядталатыны біріншіден иондардың разрядтануының шамасы мен потенциал қатынасына тәуелді. Катодта реакция теңдеуі бойынша сутегі түзіледі:
аниондарының разряды болуы мүмкін. Электродтаиондардың қайсысы және қандай ретімен разрядталатыны біріншіден иондардың разрядтануының шамасы мен потенциал қатынасына тәуелді. Катодта реакция теңдеуі бойынша сутегі түзіледі:
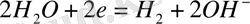 (а)
(а)
Сулы ерітіндіден қатты болат катодында разрядтану потенциалдары сутегі ионымен салыстырғанда электрлік теріс мәні көбірек болғандықтан (
 ;
;
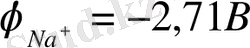 ) натрий иондарының разрядтануы мүмкін емес
) натрий иондарының разрядтануы мүмкін емес
Ерітіндіде қалған гидроксил иондары натрий иондарымен натрий гидроксид ерітіндісін түзеді
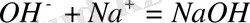 (б)
(б)
Анодта мына теңдеу бойынша хлор түзіледі
 (в)
(в)
қаныққан NaCl ерітіндісінде хлор иондарының разрядтану тепе-тең қайтымды потенциалы гидроксил иондарымен салыстырғанда жоғары (
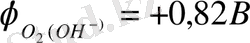 ;
;
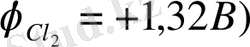 . Бірақ көмір және графиты анодтарда
. Бірақ көмір және графиты анодтарда
 иондарының разрядтануының аса кернеуі
иондарының разрядтануының аса кернеуі
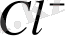 иондарынан жоғары, сондықтан, негізінде (в) реакция бойынша газтәрізді хлор бөлінеді.
иондарынан жоғары, сондықтан, негізінде (в) реакция бойынша газтәрізді хлор бөлінеді.
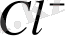 -ң разрядтануының тепе-тең потенциалының шамасы азайғандығынан бастапқы ерітіндіде NaCl -ң концентрациясының жоғарлануы хлор бөлінуіне себеп болады. Электролиздің қосынды үдерісі
-ң разрядтануының тепе-тең потенциалының шамасы азайғандығынан бастапқы ерітіндіде NaCl -ң концентрациясының жоғарлануы хлор бөлінуіне себеп болады. Электролиздің қосынды үдерісі
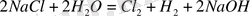
Анодта жүретін қосалқы реакция - өттегінің бөлінуі
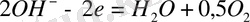 (г)
(г)
көміртектің қостотқығының бөлінуі (бөлініп жатқан өттегі анод көмірімен әрекеттескенде)
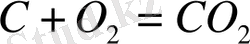 (д)
(д)
натрий хлоратының бөлінуі
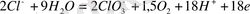 (е)
(е)
Ерітіндіде гипохлорит, хлорат және натрий хлорит түзілуімен екінші реттік химиялық реакция жүреді

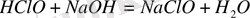


- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz