Арендер және бензолдың құрылымы, қасиеттері, алынуы және қолданылуы


Жоспары:
Кіріспе
- Арендер
- Бензол
- Бензол молекуласының құрылысы
- Арендердің гомологтары, атаулары мен изомерлері
- Арендердің алынуы
- Арендердің қасиеттері
- Арендердің жеке өкілдері және олардың қолданылуы
Пайдаланылған әдебиеттер
Арендер
Арендер - хош иісті көмірсутектер ("Углеводороды ароматические") мақаласын қараңыз. [1]
Арендердің алғашқы табылған мүшелерінің өздеріне тән жағымды иістері болғандықтан, оларды ароматты көмірсутектер деп те атайды.
Бірақ кейінірек ароматты көмісутектерге жататын көптеген заттардың хош иістері болмайтыны анықталды. Осыған қарамай, тарихи қалыптасып қалған бұл атау осы кезге дейін қолданылып келеді.
Арендер - молекулаларының құрамында бензол сақинасы (бензол ядросы) бар жалпы формуласы С n Н 2n -6 болатын көмірсутектер. Арендердің ең арапайым мүшесі - бензол С 6 Н 6 .
Бензол
Бензол - оңай қайнайтын түссіз, сұйық зат, ол суда ерімейді және өзіне тән иісі бар. Салқындатқан кезде ол оңай қатайып, ақ түсті кристалды массаға айналады, оның балқу температурасы 5, 5°С.
Бензолдың молекулалық формуласы С6Н6. Бұл формуладан бензолдың өте қанықпаған қосылыс екенін көреміз: қаныққан көмірсутектердің формуласына сәйкес келу үшін, бензол молекуласына 8 атом сутегі жетіспейді.
Осыған қарамай, егер бензолды бромды суға немесе калий пеманганаты ерітіндісіне қосып, шайқап араластырса; қанықпаған қосылыстарға тән реакцияларды көре алмаймыз. Сірә, бұған түсінікті заттың химиялық құрылысынан іздеу керек болар.
Бензолдың құрылысын анықтауды оның синтезінен бастау керек. Активтелген көмір салынып, 650°С шамасына дейін қыздырылған түтік арқылы ацетилен өткізгенде, көп мөлшерде бензол алынады.
Қазіргі заманғы физикалық әдістер бензол молекуласының циклді құрылысы бар екенін және көміртегінің барлық алты атомы да бір жазықтықта жататынын анықтады. Сөйтіп, Кекуле формуласы атомдардың қосылу тәртібін дұрыс көрсететінін растады. Енді молекуладағы атомдар- өзара қалай қосылатынын анықтау қажет болды.
Зерттеу молекуладағы барлық кеміртегі атомдарының арақашықтығы бірдей екенін 0, 140 нм шамасында тең екенін көрсетеді. Осының өзі ғана бензолда жай және қос байланыстардың жоқ екенін дәлелдейді, өйткені мұңдай жағдайда көміртегі атомдарының арақашықтығы шамамен біреуінде 0, 154 нм, ал екіншісінде 0, 134 нм болар еді. Электрондық теория бұл құбылысты былай түсіндіреді.
Бензол молекуласындағы көміртегінің барлық атомдары гибридтену күйіңде болады. Көміртегінің әрбір атомының гибридтік үш электрон бұлты (пішіні созылған көлемдік сегіздікке ұқсас) сақина жазықтығыңда көміртегінің көрші атомдарымен екі ð - байланыс түзеді, сірә, осы үш байланыс арасындағы бұрыш 120° шамасына тең болса керек. Гибридтенуге қатыспайтын және көлемдік сегіздік пішінді симметриялы төртінші электрон бұлты - байланыс жазықтығына перпендикуляр орналасқан. Көміртегі атомдары ядроларының арақашықтығы бірдей болғандықтан, ондай бұлттардың әрқайсысы көрші көміртегі атомдарының электрон бұлттарымен бірдей қалыптасады. Молекулада жеке-дара үш ʼn - байланысы түзілмейді, көміртегі атомдарының бәріне ортақ, алты электроннан құралған бір ғана ʼn - электрон жүйесі пайда болады. Молекуладағы ортақ осы электрон бұлты әсерінен көміртегі атомдарының арақашықтығы 0, 154 шамасынан 0, 140 нм шамасына дейін кемиді. Барлық көмірсутектер сияқты бензол да жанады. Ол жанған кезде ацетилендегідей өте көп мөлшерде көміртегі болғандықтан түтін бөледі.
Бензолдың суда еріген броммен әрекеттесе алмайтынына көзіміз жетті. Бірақ ол басқа жағдайда броммен өзара әрекеттеседі.
Химиялық қасиеттері жөнінде бензол қаныққан көмірсутектер мен қанықпаған көмірсутектер аралығынан орын алады. Ол қаныққан көмірсутектерге де, қанықпаған көмірсутектерге де тән реакцияларға кіріседі, бірақ бұл кезде орын басу реакциясы бензолда қаныққан көмірсутектерге қарағанда оңайырақ жүреді, ал қосып алу реакциясы қанықпаған қосылыстармен салыстырғанда қиынырақ жүреді. Бензолдың электрондық құрылысының ерекшелігі оның қасиеттеріне осылайша әсер етеді.
Фензол өте көптеген органикалық қосылыстарды синтездеуге негізгі зат болады. Нитрлеу реакциясы арқылы нитробензол C6H5NO2 алады; бензолды хлорландыру арқылы, хлорбензол С6Н5СL (еріткіш) және басқа да хлор туындыларын алады. Бензолды синтездегеңде дәрі-дәрмеіктік және хош иісті заттар, әр түрлі бояулар, үлкен молекулалы қосылыстарды және т. б. синтездеуге арналған мономерлер алу үшін бастапқы өнім ретінде пайдаланады. Ол еріткіш ретінде де қолданылып қасиеттерін жақсарту үшін мотор жанармайына қосылады.
Бензолдың және басқа да көмірсутектерінің хлор туындылары ауыл шаруашылығыңда өсімдіктерді химиялық жолмен қорғау құралы ретінде қолданылады. Мысалы, бензолдағы сутегі атомдарының орнына хлор басу нәтижесінде түзілетін өнім - гексахлор-бензол С6Н6 қатты қара күйеге қарсы бидай мен қарабидай тұқымын құрғақ өңдеу үшін қолданылады. Басқа көмірсутектердің галоген туындыларынан гексахлорбутадиенді C4CL6 атауға болады, оның құрылысы, 1, 3-бутадиенге ұқсас, жүзімдіктерде филлоксераға қарсы қолданылады. Гексахлорбензол мен гексахлордиеннің құрылымдық формулаларын жазыңдар.
Ауыл шаруашылығында зиянды бунақденелілермен күресу, арамшөптерді құрту, өсімдіктерді аурулардан қорғау, т. с. с. үшін басқа да көптеген химикаттар пайдаланылады.
Олардың кейбіреулерімен біз кейінірек танысамыз. Улы химикаттарды қолдану үшін олардың қасиеттерін жақсы білу және оларды пайдалану ережелерін қатал сақтау шарт. Өйткені оларды пайдалану ережелері дұрыс сақталмаса, адамға қауіпті және қоршаған табиғатқа орасан зиян келтіреді.
Бензол алу. Бензол алудың негізгі көзі - тас көмірді кокстеу. Кокстеу процесінде - ауа жібермей көмірді қатты қыздырғанда көптеген ұшқыш өнімдер түзіледі, сол өнімдерден басқа заттармен қатар бензол алынады.
Бензол молекуласының құрылысы
Жалпы формуласы С n Н 2n -6 болғандықтан, бензолды өте қанықпаған қосылысқа жатқызуға болар еді. Бірақ бензол бромды сумен және калий перманганатының ерітіндісімен әрекеттеспейді, яғни қанықпаған қосылыстарға тән реакцияларға түспейді. Осылай бензолдың құрамы мен қасиеттерінің арасында біздің түсінігімізше сәйкессіздік туады. Бензол буы мен сутек газының қоспасын катализаторы бар қыздырылған түтік арқылы өткізсе, бензолдың бір молекуласы сутектің үш молекуласын қосып алып, құрылысы бізге таныс циклогексан түзіледі екен:

Бензол бұл қасиетті тек циклді құрылысты болғанда ғана көрсете алады деп тоқтам жасауға болады. Молекула құрамындағы көміртектің алты атомы цикл жасап тұйықталады және олар өзара қос байланыс пен дара байланыс арқылы кезектесіп жалғасады деп, бензолдың құрылымдық формуласын ең алғаш неміс ғалымы А. Кекуле ұсынды (1865 ж. ) .
Бірақ құрамында үш қос байланысы болса, бензол қанықпаған көмірсутектерге тән қасиеттер көрсетіп, бромды су және калий перманганатының ерітіндісімен әрекеттесер еді.
Сонымен бұл формула:
а) құрамында қос байланыс болғанымен, бензол неге қосылу реакцияларынан гөрі, орынбасу реакцияларына бейім;
ә) бензол молекуласындағы барлық көміртек атомдарының араларындағы байланыстардың ұзындықтары неге бірдей;
б) бензол молекуласының химиялық тұрақты болуы неліктен, т. б. сұрақтарды қанағаттандыра алмады. Бірақ Кекуле ұсынған формула бензолдың химиялық қасиеттерін толық сипаттамағанымен, осы уақытқа дейін қолданылып келеді.
XX ғасырдың басында ғана әр түрлі физикалық тәсілдерді пайдаланудың аркасында, бензол молекуласының құрылысын түсіндіруге мүмкіндік туды. Бензол молекуласы жазық пішінді. Барлық көміртек атомдары ұқсас, электрон тығыздығы бірдей бөлінген, көміртек атомдарының арақашықтықтары өзара тең (0, 140 нм) . Бензол молекуласы тең қабырғалы жазық алтыбұрыш пішінді болады.
Барлық көміртек атомдарының s-байланыстары мен р-электрон тығыздығының біркелкі бөлінуі (орналасуы) нәтижесінде едәуір берік және бәрі бірдей "ароматты" байланыс түзіледі. Яғни, бензол молекуласындағы барлық көміртек атомдары арасындағы байланыстар "таза" дара байланыстардан да, қос байланыстардан да өзгеше болады. Бензолдың бұл қарастырылған құрылымдық формуласы жоғарыда қойылған сұрақтарға (бензол неліктен қосылу реакцияларына бейім емес, неге барлық алты қабырғалары тең және неге химиялық тұрақты, т. б. ) жауап бере алады. Бензол молекуласының барлық алты қабырғаларының ұзындықтары бірдей 0, 140 нм-ге тең болады. Бензолдағы С-С байланыстардың энергиясы 490 кДж/моль-ге тең дара байланыс пен қос байланыстар мәндерінің арасындағы сан болады.
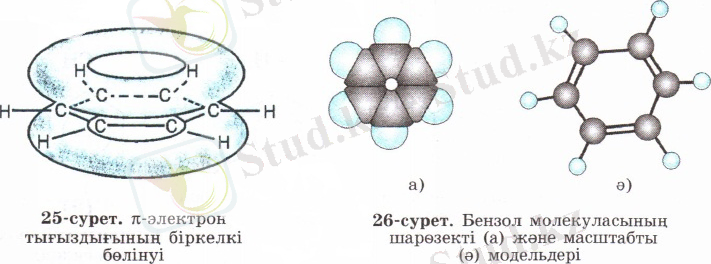
Молекуласында электрон тығыздығының біркелкі бөлінуін ескеріп, бензолдың құрылымдық формуласында ортақ байланысты тең қабырғалы алтыбұрыштың ішіндегі дөңгелек арқылы да бейнелеуге болады. Сонымен қатар кемшіліктерін ескере отырып, Кекуле ұсынған формуланы да пайдалануға болады.
Арендердің гомологтары, атаулары мен изомерлері
Ароматты көмірсутектерді жүйелеу номенклатурасы бойынша арендер деп атайды. Бензол молекуласының сутек атомдары көмірсутек радикалдарына алмасқанда, бензолдың гомологтары түзіледі:
- бензол: С6Н5- H
- метилбензол: С6Н5- СН3
- этилбензол: С6Н5- С2Н5
- пропилбензол: С6Н5- С3Н7
Бензолдың гомологтарын атау үшін қалыптасқан тривиальді атаулар да қолданылады: метилбензолды толуол, диметилбензолды ксилол, изопропилбензолды кумол, винилбензолды стирол деп атайды.
Молекуласында бірнеше радикалдары бар қосылыстарды атау үшін бензол сақинасындағы көміртек атомдары нөмірленіп, қосылысты атағанда орынбасардың орны сандар арқылы көрсетіледі. Егер бензол молекуласының екі сутек атомы радикалдарға алмасқан болса, онда бензолдың орто-, мета-, пара- туындылары түзіледі. Оларды атағанда, қысқаша бірінші әрпімен белгілейді: орто - о , мета - м , пара - п . Немесе әріптердің орнына сандар арқылы белгілеулер де қолданылады.
С 6 Н 5 - тобы фенил радикалы , С 6 Н 5 - СН 2 - бензил радикалы деп аталады.
Арендердің алынуы
Арендерді, негізінен, тас көмір шайыры мен мұнайды фракциялап айдап алады. Сонымен қатар мұнайды өңдегенде және көмірді кокстегенде түзілетін газдарды синтездеу арқылы да алынады.
1. Сәйкес алқандарды катализатор қатысында ароматтап дегидрлегенде (риформинг) бензол мен оның туындылары түзілетінін білесіңдер:
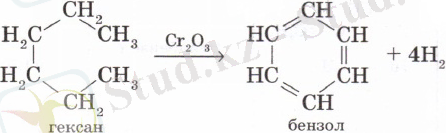
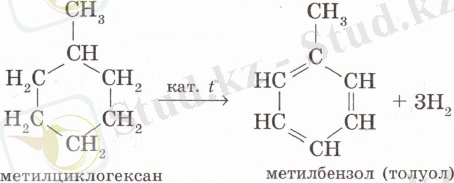
2. Арендерді циклогексан мен оның гомологтарын дегидрлеп алуға болады. Н. Д. Зелинский мұнайдың құрамындағы циклогександы Pt, Pd катализаторлары қатысында 300°С температурада дегидрлеп бензол алды:
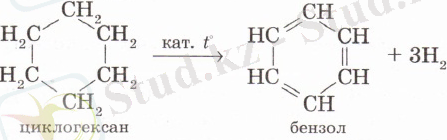
Осы келтірілген жағдайларда циклогексан туындыларын дегидрлегенде, бензолдың туындылары түзіледі:
3. Ацетиленді белсендендірілген көмір қатысында қыздырып бензол алуға болатынын сендер өткен тақырыптардан білесіңдер:
4. Бензолдың гомологтарын катализатор (алюминий хлориді немесе темір (III) бромиді) қатысында бензолды алкилдеп алуға болады:
Арендердің қасиеттері
Физикалық қасиеттері
Арендердің бастапкы мүшелерінің өздеріне тән иістері бар, олар суда ерімейтін, сұйық заттар. Органикалық еріткіштердің біразында жақсы ериді және өзі көптеген органикалық заттарды ерітеді. Бензол гомологтарының салыстырмалы молекулалық массаларының өсуіне байланысты балқу және қайнау температуралары заңды түрде артады. Бензол улы.
Бензол буымен үнемі дем алу анемия, лейкемия сияқты ауруларға ұшыратады. Толуол мен басқа гомологтарының зияндылығы бензолға қарағанда төмендеу.
Химиялық қасиеттері
Арендер орынбасу, қосылу және тотығу реакцияларына түседі.
Орынбасу реакциялары. Бензол ядросы едәуір тұрақты болғандықтан, бензолға орынбасу реакциялары тән.
1. Галогендермен орынбасу реакциялары темір (III) тұздарының қатысында жүреді:
Хлормен де бензол осылай әрекеттеседі.
2. Нитрленуі. Нитрлеуші қоспаның (концентрлі күкірт және азот қышқылдарының қоспасы) қатысында қыздырғанда, бензолдан нитробензол түзіледі:
... жалғасы
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz