Қышқылдық-негіздік титрлеу: қисық сызықтар, индикаторлар және индикаторлық қателер; фармацевтикалық анализдегі қолданылуы


Тақырыбы: «Қышқылдық-негіздік титрлеу қисық сызықтары. Индикаторлар. Қышқылды-негіздік титрлеудің индикаторлық қателері. Фармацевтикалық анализде қышқылдық-негіздік титрлеудің қолданылуы»
Тақырыбы: Қышқылдық-негіздік титрлеу қисық сызықтары. Индикаторлар. Қышқылды-негіздік титрлеудің индикаторлық қателері. Фармацевтикалық анализде қышқылдық-негіздік титрлеудің қолданылуы.
Мақсаты: Қышқылдық-негіздік титрлеу және оның жіктелуі туралы түсінікті қалыптастыру.
Дәріс жоспары:
1. Қышқылдық-негіздік титрлеу қисық сызықтары.
2. Индикаторлар.
3. Қышқылды-негіздік титрлеудің индикаторлық қателері.
Дәріс тезистері:
- Күшті қышқылды күшті негізбен ( немесе қарама -қарсы ) титрлеу қисығы.
Күшті қышқылды күшті негізбен титрлеу механизмі мынандай теңдеумен сипатталады:
+ О рН = 7
Күшті қышқылды күшті негізбен немесе қарама-қарсы титрлегенде эквиваленттік нүкте нейтралдану нүктесіне сәйкес келеді (рН=7), себебі күшті қышқыл мен күшті негізден түзілген тұз гидролизденбейді және бейтарап орта көрсетеді, яғни рН = 7. Мысалы: 100 мл 0, 1 н күшті қышқылдың ( ерітіндісі 0, 1 н күшті негіздің (NaOH) ерітіндісімен титрленеді.
НСІ + NaOH NaCL + O
+ O
Титрлеу үрдісіне дейін рН = 1 күшті қышқылдың 0. 1 н ерітіндісі болады. Осы ерітіндіге 90 мл 0. 1 н сілті (NaOH) ерітіндісі құйылғанда, қышқылды 90% титрленеді. Бос қышқылдың мөлшері бастапқыдан он есе азаяды, яғни бос қышқылдың концентрациясы 0. 01 немесе моль/л, ал рН =2 болуы керек. Қышқылдың ерітіндісіне 99 мл сілті құйылғанда, қышқылдың мөлшері тағыда он есе төмендейді, яғни оның концентрациясы 0. 001 немесе моль/л болып, ерітіндінің рН жуық шемемен болып, ерітіндінің рН жуық шемемен 3 тең болады. Ал қышқылдың ерітіндісіне 99, 9 мл сілті құйылатын болса, қышқылдың концентрациясы 0. 0001 немесе моль/л ге дейін төмендеп ерітіндінің рН 4 ке дейін жоғарылайды.
Титрлеу үшін алынған 100 мл 0. 1 н қышылдың ерітіндісіне концентрациясы сондай 100 мл сілті құйылғанда, яғни эквивалентті мөлшері қосылғанда, эквиваленттік нүкте орнайды. Бұл уақытта ерітіндіде осы реакцияның нәтижесінде пайда болған тұз ғана болады. Түзілген тұз гидролизге ұшырамайтындықтан pH=7. Дәл осы кезде титрлеуді тоқтату керек.
Бірақ күшті қышқылды күшті негізбен титрлеу барысындағы рНтың өзгерісі туралы толық мәлімет алу үшін есептеулерді сілтінің 100 %ті артық мөлшеріне дейін жалғастырамыз.
Айталық, сілтінің артық қосылған мөлшері 0. 1 мл, яғни 100, 1 мл болсын. Сілтінің осы қосылған артық мөлшері (0. 1 мл ) пайда болған иондардың концентрациясы, қышқылдың тура осындай артық мөлшерінен пайда болған иондардың концентрациясына тең болады. Яғни [ ] = моль/л, осыдан [ ] = моль/л, ал рН=10. Осылайша сілтінің артық мөлшері бір мл болса, [ ] = , [ ] = моль/л, рН=11 т. т. Алынған нәтижелерін титрлеу қисығы түрінде көрсетуге болады
Қисықтың солдан оңға қарай бағыты қышқылды сілтімен титрлеу кезіндегі рНтың өзгерісін, ал қарама-қарсы, оңнан солға қарай сілтіні қышқылмен титрлеуді сиппаттайды. Титрлеу қисығы бойынша эквиваленттік нүкте нейтралдану нүктесіне (рН=7) сәйкес келеді.
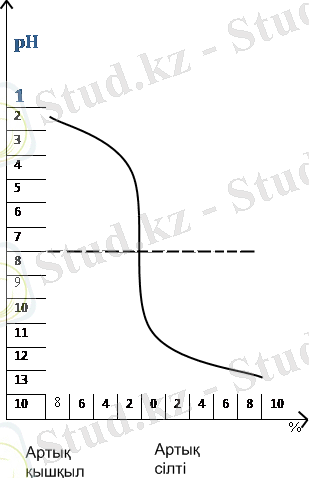
Бұл жағдайда титрлеу соңына жақындағанда рНтың күрт өзгеретінін байқауға болады. Шынында да сілтінің жуық шамамен барлық мөлшері құйылғанда (99, 9мл) рН 1-ден 4-ке дейін өзгереді де, ал қышқылдың артық мөлшерінен сілтінің артық мөлшеріне ауысқанда рН 4-тен 10-ға дейін күрт өзгереді. Жұмысшы ертіндінің аздаған артық мөлшерінен болатын рН күрт өзгерісі титрлеу секірмесі деп аталады.
Іс жүзінде ертінділердің кішірек көлемдері қолданылатын болғандықтан, бұл өзгеріс жұмысшы ертіндінің 1-2 тамшысынан ғана болуы мүмкін.
рН=рК-Iq
теңдеуі бойынша 1-2 тамшы жұмысшы ертіндінің көлемінен рН-тың күрт өзгеруіне қатынасының күрт өзгерісі, яғни индикатор бояуының күрт өзгерісі сай келу керек. Индикаторды таңдау ережелеріне сәйкес, титрлеу үшін қолданылатын индикатордың титрлеу көрсеткіші титрлеу секірмесінің бойында жатуы қажет. Біздің мысалымызда титрлеу көрсеткіштері 4 пен 10ның арасында болатын индикаторларды пайдалануға болады. Мысалы, метилоранж (рТ=4), фенолфталеин (рТ=9), т. б.
РН секірмесі температураға және титрленетін ерітінділердің концентрациясына тәуелді болады. Температура жоғарлағанда және ерітінділердің концентрациясы төмендегенде титрлеу секірмесі кішірейеді.
Осыдан күшті қышқылды күшті негізбен (немесе қарама-қарсы) титрлеу үрдісі бойынша мынадай қорытынды жасауға болады;
- Эквиваленттік нүкте нейтралдану нүктесіне дәл келеді.
- Ара қашықтығы үлкен титрлеу секірмесі болады.
- Титрлеу көрсеткіші рТ=4-10 индикаторларды пайдалануға болады.
Индикаторлар- молекулалық және иондық түрлердегі түстері әр түрлі, күрделі құрылысты органикалық қышқылдар және негіздер. Бір түсті және екі түсті индикаторларды ажыратады. Алғашқысында тек бір түрі, екі түстілерінде - екі түрі де боялған. Бір түсті индикатор - фенолфталеин - қышқыл және бейтарап ортада түссіз, себебі молекулалық түрде болады. Сілтілік ортада фенолфталеин протон жоғалтып, анион түріне өтеді, таңқурай (малина) түске ие болады. Екі түсті индикатор - метилды қызыл-сары, қышқыл ортада қызғылт түстес, бейтарап және сілті ортада сары түсті.
Индикатор ерітіндіге өте аз мөлшерде қосылады, ол рН әсер етпейді. Индикатор ерітіндіде иондарға ыдырайды.
H Jnd + ( 8. 3)
Бұл тепе-теңдік концентрациясының өзгеруіне сай титрлеу кезінде ығысады. Негізінен түс өзгеруі рН екі бірлігін қамтиды. рН қай мәнінде индикатор түсін өзгертеді. ( 8. 3) теңдікке әсерлесуші массалар заңын қолданайық.
= (8. 4)
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz