Химияға кіріспе: пәннің негіздері, даму тарихы және іргелі заңдар


ХИМИЯ ПӘНІ
Химия - жаратылысты зерттейтін ғылымдардың бірі.
Жаратылыс дейтініміз - бізді айнала қоршаған материялық дүние Бұл материялық дүние адам баласының сана - сезімінен тыс, оған тәуелсіз, өз бетімен жасап тұрған объективті" болмыс, «материя дейтініміз, ол біздің сезім мүшелерімізге әсер ету арқылы түйсік туғызушы; материя дейтініміз бізге түйск арқылы берілетін объективтік болмыс».
Материя, материялық дүние, жаратылыс жайында түсінік толық, дұрыс болу үшін, онда өнебойы өзгеріс, өсу, өшу, даму процестері, үздіксіз қозғалыс болатындығын естен шығармау керек Материя әрдайым қозғалыста болады. «Қозғалыс - материянын. бар екендігінік формасы. Еш жерде, еш уакытта қозғалыссыз материя болған емес, болуы мүмкін де емес . . . » (Ф. Эн-гельс) .
Демек, қозғалыс - материянын бөліп алуға болмайтын өзімен бірге жаралған қасиеті. Материя мен оның қзғалысы жойылмайды да, жанадан жаралмайды да, ол- мәңгілк.
Материя қозғалысынын, түрлері әр қилы: заттың бір орыннан екінші орынға қозғалуынан бастап, онын, қызуы және салқындауы, жарық шығаруы, химиялык әрекеттесуі, тіршілік. процестері, ең ақыры ойлау - осының барлығы материяның қозғалысының түрлері.
Адам жаратылыс зерттеуде болсын, не күнделікті тұрмысында болсын жаңа айтылып өткен кең тусініктегі материямн емес, омың нақты көріңісімен, материяның жеке тұрімен кездеседі. Матер тұрақты физикалық қасиеттері бар әрбір түрі з а т деп аталады, мысалы, шыны, темір, уран, бор, гелий т. б. жеке заттар.
Күнделікті бақылауымызда бұл заттар өнебойы өзгсріске ұшырйтындығын байқаймыз, мысалы, тау жыныстаы күйрейді, у буға айналып ұшады, темір тоттанады. Осы өзге істердің барлығы - материя қозғалысының жеке түрлері.
Материяның нақты көрінісі (заттар) өте көп, материя қозғалысының түрлері де қилы-қилы, осыған сәйкес жаратылысты зерттейтін ғылымдар да түрлі салаға бөлінеді.
Химия материя қозғалысының химиялық түрін зерттейді, яғни зат негізінен өзгеріп, бір заттан екінші жаңа зат түзілуіне байланысты туатын материя қозғалысының түрін зерттейді.
Материя қозғалысының химиялық түрін - химиялық өзгеру процесін - кебінесе химиялық реакция деп атайды. Реакцияласушы және реакция нәтижесінде түзілетін заттардың санына және сапасына қарай химиялық реакциялардың төрт түрі болады.
X и м и я - з а т т а р д ы ң б і р і - б і р і н е а й н а л ы п ө з геруін зерттейтін ғылым. Химия - заттардың құрамын, құрылысын, қасиеттерін өзгерістерін, өзгеріс жағдайын, әрі м е н қа б а т б о л а т ы н құбылыстарды ғ ы л ы м .
Химиялық зерттеу әдістерінің бірі - бақылау, бірақ ол заттарды және түрлі құбылыстарды үстіртін бақылау және сипаттап жазумен қанағаттанбайды, сол құбылысты терең түсіндіруді мақсат етеді. Құбылысты түсіндіру үшін оиын мазмұнына терең бойлап, ол құбылысты туғызатын себептерді тауып, оның, болу жағдайын анықтайды.
Міне, осы үшін жаратылыстын түрлі құбылыстарын, процестерін (реакцияларын), қолдан жасалған жағдайда зерттейді, оны т ә ж і р и б е не эксперимент деп атайды.
Химик бір құбылысты не процесті зерттеп отырғанда, келген ойының, жорамалының дұрыс екенін білу үшін тәжірибе қойып шешеді. Ондай жорамалды гипотеза дейді.
Егер тәжірибе жүзінде гипотезаның дұрыстығы анықталса, ол тек бір бұл құбылыс емес, жаңа құбылыстарды түсіндіруге жол ашатын болса, онан шығатын қорытындылар ақиқат шындыққа дәл келіп жатса, онда гипотеза теорияға айналады.
Сонымен, химия ғылымы алдына қойған міндеттерді шешуде бақылау, гипотеза, тәжірибені негізгі зерттеу әдістері ретінде пайдаланып, олардың нәтижесінде анықталған мәліметтерді түсіндіру үшін теорияларды басшылыкқа алады.
Өзімізді қоршаған жаратылыс дүниеліктерін танып-білуде, оларды кәдеге асырып, тұрмысымызда пайдалануда химия ілімінің алар орыны ерекше.
Химия ілімі - заттардың қасиеттерін, олардың өзара әрекеттесуін, түрленуін, осылардың нәтижесінде құрамы мен құрылымының өзгеріске ұшырауын қарастырады.
Химияғылымы өзінің даму барысында сан-салаларға бөліне отырып, түп бастауыш «жалпы және бейорганикалық химиядан» алады десек қателеспейміз.
Химия ілімінің теориялық негіздері мен іргелі заңдылықтарын тужырымдап зерттеумен «Жалпы химия « бөлімі айналысады.
Ал, периодтық кестеде жинақталған химиялық элементтер және олардан түзілген жай, күрделі заттардың қасиеттерін, түрленулерін зерттейтін сала, «Бейорганикалық химияның» еншісіне тиесілі
Химиялық элементтер, олардан түзілген қосылыстардың құрылым-құрылысымен, қасиетінің арасындағы байланыс заңдылығын негізге ала отырып, жаңа бейорганикалық заттар алу, соңғы саланың ең басты мәселесі болып табылады.
Ал, алдын-ала болжамжасау және осы болжамының іс жүзінде орындалуы, кез-келген ғылым саласына тән нәрсе.
Айта кететін жайт, іс жүзінде орын алған құбылыстармен өзгерістерді жүйелі түрде жинақтаи ғылыми тұрғыда талқылау үшін «Жалпы және бейорганикалық химия» саласы, негізінен мынандай іргелі дүниеліктерге сүйенеід.
1. Атом құрылысының квантты-механикалық теориясы және химиялық элементтердің периодтық кестесі;
2. Зат қасиетінің, оның құрылымымен құрылысына негізделген квантта химиялық құрылыс теориясы;
З. Химиялық термодинамикадан туындайтын химиялық тепе-теңдік ілімі.
ХИМИЯ ДАМУЫНЫҢ БАСТЫ КЕЗЕНДЕРІ
Адамзат баласы көне дәуірден-ақ химия ілімін тұрмыста күнкөріс мақсатында пайдалана білген. Өзін қоршаған орта дүниеліктерін өз мұқтажына жарата білу, жағдайын жақсарту жолында тынымсыз еңбек еткен.
Жалпы тіршілік иелері табиғаттың тылсым құпияларына көз жеткізу барысында, саналы-санасыз тұрде ғылымның әртүрлі салаларын ұдайы жетілдірумен келген жане келеді де.
Алғашқы отты пайдалануды үйреніп, жер жырту, аң аулау үшін әртүрлі темір құраддарды жасан, әсемдік үшін бояуларды өндіруге қол жеткізген адамзат баласы, өз тарихында кәсіптік -тұрмыстық химиямен (ремесленная химия) айналысып жатқанын сезінген де жоқ.
Біздің жыл санауымызға дейінгі 3000 жылдары қытайлықтар мен Месопотамия тұрғындары отын ретінде ағаш көмірін қолдана отырып металл қорытуды, қыш және шыны бұйымдарын өңдеп, өндіруді жеткілікті дәрежеде меңгере білген. Жыл санауымызға дейінгі 600-100 жылдары грек мәдениетінің өркендеу барысында оқымыстылар дүниені танып-білуге ден қоя бастады. Әлем таныған ойшыл Аристотель жаратылыс дүниеліктерінің бәрі де төрт бастамадан яғни Жер - Ауа - От және Судан тұрады деп тұжырымдады .
Ылғалдық
Жылылық Салқындық
Құрғақтық
1 - сурет. Дүниенің түп төркінінің құрамдас бөліктері
Дүниенің түп төркіні болып келетін осы төрт элементтің өзара қосылуынаы жылылық, құрғақтық, салқындық және ылғалдық қасиеттері туындайды. Мысалы, ауа және су қосылуынан ылғал, ал ауамен от қосылуынан жылылық туындайды деп түсіндірген.
Грек философтары Демокрит, Левкипп, Эникур және Лукрецийлер дүниедегі заттардың бәрі де бөлінбейтін өте ұсақ бөлшек атомдардан тұрады деген пікірде болды.
Ал енді «химия» сөзінің шығу тарихына келсек, бұл туралы кесімді бір пікір жоқ.
Кейбір тарихшылар бұл сөз ертедегі гректердің «хима» деген сөзінен, яғни металдарды қорыта білу өнерінен шыққан десе, Византиялық оқымыстылардың айтуы бойынша химия дегеніміз алтын және күмісті қолдан жасанды даярлау деп түсіндірген.
Көп жағдайда «химия» сөзін ежелгі Египет тұрғындарыяың анықтамасымен байланыстырады, өйткені химия дегеніміз «алхимия» сөзінен туындаған дейді. Ертедегі Египет Ал Хим деи аталып «қара жер елі» мағынасын білдіретін болғандықтан, алхимия "егигют ғылымы" деген ұғымды білдірсе керек дегенге саяды. Тарихи деректерге сүйенсек, біздің жыл санауымызға дейінгі Ш- ғасырда-ақ Египеттегі Александрия қаласында Ғылым Академиясы құрылып, химия іліміне Серапис храмы берілген екен. Ал жалпы «химия» атауы латынның «Сһіmіа» сөзінен туындап, интернационалдық сөз болып саналады.
Дегенмен, ертеден грек сөздерінде «хюмос», «хюма», «химевскис» яғни шырын, құю, араластыру сөздері ұшырасатын болғандықтан, бұларды да алхимия сөзіне жақындығы бар деп есептейді. Ал «ким» - ескі қытайда - алтын деген мағынаны білдіреді. Олай болса бұл қытайлықтардың да химия ілімін дамытуда өз сүрлеуі болғандығын айғақтайды. Енді осы химияның даму кезендеріне қысқаша тоқталалық.
Алхимия және ятрохимия кезеңі . ( көне дәуірден ХVІІ ғасырға дейін) . Адамзат баласы ежелден -ақ асыл тас, құнды заттардың қадір қасиетін бағалай білген. Осы салада қалайы, қорғасын, темір металдарынан ерекше бір «философиялық тас» көмегімен немесе әмбебап еріткіш «алкатест» жәрдемімен бағалы алтын, күміс алуға болады деп тынымсыз
зерттеулер жүргізген. Сонымен қатар, адамзат баласына мәңгілік өмір беретін, жастығын сақтап қалуға себепші болатын «өмір эликсирі» (эликсир жизни) деген сұйық зат болатындығы туралы пікір үстем болған. Осындай ізденістегі зерттеушілерді алхимиктер, ал осы бағыт алхимия деп аталынды.
Бір қызығы осы алхимиктер қатарына ағылшын физик-математигі Ғұлама ғалым Исаак Ньютонды (1643-1727) да жатқызуға болады.
Алхимия негізінен ғылымда екі бағытгы дамытуға себепші болды.
Бірінші бағыт - медицина жэне фармацевтика.
Екіншісі жану, металл қорыту, ауа құрамын, газ қасиетерін зерттеу салалары.
ХVІғасырда химияның дәрі-дәрмек жасау бағыты кең дамып өріс ала бастады.
Швейцария дәрігері Парацельс (1493-1541) «Химия мақсаты дәрі-дәрмектер жасауға арналады» деп жазды. Парацельс оқуы бойынша жаратылыс дүниеліктері негізінен үш бастамадан яғни: түз (дене) [соль (тело) ] - сынап (жан) [ртутъ (душа) ] - күкірттен (рух) [сера (дух) ] - түрады деп түжырымдалды. Осы бір дүниеліктің біреуінің жетіспеуі адамзатты ауруға шалдықтырады және кеселді осы жетіспейтін элементті адам организміне енгізу арқылы жазып алуға болады делінді. Медицина және химия саласындағы бұл кезең (ХVІ-ХVШ ғ. ) гректердің іаtros - дәрігер, яғни ятрохимия деген атпен танымал.
ХVII-ғасырдың екінші жартысынан бастап ағылшын ғылымы Р. Бойль (1627-1691) химиялық қосылыстардың тегі бірдей деген ұғымды ұсынды. Ол элемент деген түсінікті кіргізе отырып, зат құрамын анықтап талдауға арналған іс-тәжірибелерді ретіне келтіріп жүйелей білді. Химияның мақсаты тек алтын алуда емес, дүниені танып білуде екендігін мәлімдей отырып, алхимия, ятрохимия көзқарастарының негізсіздігін, ол өзінің «Химик-скептйк» еңбегінде жария етті.
Флогистон теорнясы
Медицина, металлургия және химия өнеркәсіптерінің дамуы көптеген құбылыстарға дәйекті түрде жауап беруді алға тартты. Осы орайда XVIII ғасырдың басында тотығу-тотықсыздану процесстерімен, жану табиғатымен айналысқан неміс химигі және дәрігер Г. Э. Шталь (1659-1734) өзінің флогистон теориясын ұсынды. Грек сөзінен ұшқыш, тұтанғыш деген мағынаны білдіретін флогистон теориясының негізгі қағидасы жануға бейім кез-келген заттың құрамында «флогистон» дүниелігі болатындығын тұжырымдады. Жану барысында ол затты тастап үшып шығып кетеді. Мысалы, металдар жану барысында флогистонынан айырылып тотыққа айналады, ал қайтадан флогистонды қосып алу барысында, олар, металл қалпына келе алады делінді.
Келтірілген тұжырымының дұрыс еместігін М. В. Ломоносов (1711-1765) онан соң А. Лавуазье (1743-1794) өз зерттеулерінде дәлелдей білді. Олар жану дегеніміз кез-келген заттың «ауа бөлшектерімен « химиялық әрекеттесуі деген көзқараста болды.
Жалпы М. В. Ломоносов ғылымның кез-келген саласына қомақты үлес қоса білген ғалым. Сол кезеңде үстем болып келген денелердің белгілі бір жылу қоры (теплород) болады деген көзқарасқа қарсы өзінің тұжырымын, яғни дене бойындағы жылу олардың қүрамындағы бөлшектер -«корпускулалардың» қозғалуынан туындайтындығын атап көрсетті. Физикалық химияның негізін сала отырып, қозғалыс және материя сақталу заңдылығын тұжырымдап «флогистон» деген ұғымды жоққа шығара білді. М. В. Ломоносов химиялық реакцияларды зерттеу барысында өлшемдік тәсілдерді кең пайдалана отырып, химия пәнінің өз алдына ғылым болып қалыптасуына үлкен үлес қосты. Зат массасының сақталу заңын атом - молекулалық іліммен үйлестірген М. В. Ломоносов бүгінгі химия ғылымында іргелі заңдылықтар авторы болып есептелінеді.
теңдіктермен төмендегіше сипатталады:
Е=mс
2
; Е=
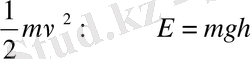
Мұндағы, Е - энергия; т - зат массасы; g - еркін түсу удеуі; V, с - дене немесе жарық жылдамдықтары; һ - биіктік.
Зат массасьның сақталу заңы;
Химиялық реакцияға қатынасатын заттардың массасы реакщя нәтижесінде тузілетін заттардың массасына тең.
Энергия сақталу заңы .
Энергия жоқтан бар болмайды, бар нәрсе жоғалмайды тек бір түрден екінші түрге айналып өзгеріп отырады.
Ал, М. В. Ломоносов бұл заңдылықтарды былайша қорытқан болатын: «Табиғатта болатын барлық өзгерістердің мәні мынада: бір денеден бір нәрсе қанша кемісе, екіншісіне сонша қосылады, бір жерден бірнеше материя азайса басқа жерде соншама артады . . . Дәл осы айтылған заңдылық қозғалыс ережесі үшін де орынды: өзге бір денені қандай күшпен қозғалысқа келтірсе, сонша күшті ол өзінен жоғалтады». Осы тұрғыдан қарағандаМ. В. Ломоносов ашқан және «табиғаттың жалпы заңы» деп қарастырған бұл заңды «Зат массасының және энергияның сақталу заңы» деп атаған жөн. Кейбір оқулықтарда массаның біршама бөлігін энергияға айналып кетті деген қате пікірлер де айтылады. Есте ұстар жай:
Масса материяға тән қасиет және оның инерттігін айқындаушы шама ал энергия болса осы материяға тән қозғадысты сипаттаушы шама. Сондықтан масса және энергия ұғымдары материяға тән қасиеттерді сипаттай отырып, өзара бір-біріне түрленбейтіндігін және бір-бірімен нақты теңдеулер арқылы байланыста болатындығын естен шығармаған абзал.
Авогадро гиютезасы. Көлем-қатынас заңы
Тәжірибе жүзінде француз ғалымы Жозеф Луи Гей-Люссак химиялық реакцияға түскен газдардың көлемдерінің қатынасы бүтін сандардың қатынасындай болатындығына көз жеткізді. Мысалы, хлорлы сутек түзілу барысында сутек, хлор жэне хлорлы сутек көлемдерінің қатынасы 1:1:2 тең.
H 2 +CL 2 →2HCL
(I) (I) (2)
Ал су түзілу барысында сутек, оттек және су буының көлемдерінің қатынасы 2:1:2 тең, яғни:
2Н 2 + О 2 = 2Н 2 О
(2) (1) (2)
Іс жүзінде алынған мәліметтерді қорыта келе Ж. Л. Гей-Люссак мынадай тұжырым жасады:
Тұрақты температура және қысымда химиялық реакцияға қатынасушы газдардың көлемдерінің өзара қатынасы жай бүтін сандардың қатынасындай болады.
Келтірілген тұжырым «көлем қатынас заңы» деп аталады, Ал итальян ғалымы А. Авогадро газ күйіндегі заттармен жүргізілген тәжірибелерге сүйене отырып өз гипотезасын ұсынды:
1. Бірдей жағдайда (қысым және температура) әртүрлі газдардың бірдей көлемінде молекула сандары өзара тең болады.
2. Газ күйіндегі жай заттардың молекулалары екі атомнан тұрады.
Мысалы, сутек, азот, хлор, оттек және т. б.
Сутегімен хлор әрекеттесу барысында түзілген хлоры сутек көлемі әрекеттесуші хлормен сутек көлемдерінің қосындысына тең, яғни жеке-жеке сутегінің және хлордың әрбір молекуласы екі
атомнан тұратындығын білдіреді. Егер, сутегімен хлор молекуласы бір атомнан тұрса, онда бір ғана көлем хлорлы сутек түзілу қажет және бұл мәлімет тәжірибеге қайшы келер еді. Ал, хлор және сутегі жеке-жеке алғанда екі атомнан тұратын болғандықтан түзілген хлорлы сутек көлемі екі есе көп, өйткені хлорлы сутектің өзі екі атомнан тұрады демек оның көлемі екі есе көп болуы шарт. Мұны тәжірибе де дәлелдеп отыр.
Авотадроның бірінші гипотезасы Авогадро заңы деген атпен кең танымал және осы заңнан маңызды екі салдар туындайды:
1. Қалыпты жагдайда (t = 0
0
C, р = 1, 033•10
5
Па) кез келген газдың бір
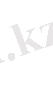 молі 22, 416 литрге тең көлем алады. Бұл шама газдың молярлы көлемі деп аталады.
молі 22, 416 литрге тең көлем алады. Бұл шама газдың молярлы көлемі деп аталады.
2. Бір газдың белгілі көлемінің массасының өзге бір газдың осындай көлемдегі массасына қатынасы бірінші газдың екінші газ бойынша тығыздығы деп аталады да «D» таңбасымен белгіленеді.
(Газдар бірдей жағдайда алынуы қажет) . Айтылғанды математика тілінде өрнектелік:
D=
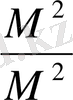
мұндағы D - 1 -газдың 2 -газ бойынша тығыздығы;
М 1 М 2 - 1 және 2 газдың молярлы массалары. Егер, газдың молекулалы массасы белгісіз болса, онда дәл сондай көлемдегі молекулалық массасы белгілі газ арқылы тығыздықты анықтап, газ молярлы массасын оңай анықтауға болады.
М (белгІсіз газ) = D•М (белгілі газ) .
Өрнектегі тығыздықты тәжірибе жүзінде анықтап алады. Есептеу барысында қысым, температура қалыпты жағдайдан өзгеше болғанда газ көлемін төменде келтірілген Менделеев Клапейрон теңдеуі арқылы анықтайды:
PV=
Equation. 3
мұндағы р - газ қысымы;
V - газ көлемі;
т - газ массасы;
М-газдың молярлы массасы;
К-универеалды газ тұрақтысы;
Т - термо динамикалық температура.
Көп жағдайда газдардың тығыздығы сутегі немесе ауа бойынша анықталада да, олардың молекулалы массасын есептеуде мына формулалар жиі пайдаланылады:
М (газ) = 2-DH 2 , мұндағы -2- сутегінің молярлы массасы. М (газ) = 29-D ауа , мұндағы -29- ауаның молярлы массасы.
Стехиометриялық заңдылықтарына құрам тұрақтылық заңы эквивалент заңы және еселік қатынас заңы жатады.
Құрам тұрақтылық заңы
Құрам тұрақтылық заңын алғаш ретфранцуз ғалымы Ж. Пруст (1808 ж) тұжырымдады. Оның айтуынша Оңтүстік пен Солтүстік жарты шарлардағы темір оксидінің арасында ешқандай айырмашылық жоқ. Сібірдегі малахиттің құрамы Испаниядағы малахиттің құрамымен бірдей. Жердің бір полюсімен екінші полюсіне дейінгі аралықтағы бірдей қосылыстардың құрамдары да, қасиеттері де бірдей болады.
Құрам тұрақтылық заңы төмендегіше түжырымдалады: алыну тәсілдеріне қарамастан кез келген таза заттың құрамы мен қасиеті тұрақы болады.
Әйтсе де ғылымның соңғы жаңалықтарын ескерсек, аталған заңдылық тек құрамы мен құрылымы молекулалық түрдегі қосылыстар үшін ғана орынды екендігі шығады. Демек, химиялық қосылыстар молекулалық түрден өзге түрде де бола алады деген сөз. Айтқанымыз түсінікті болу үшін бір валентті хлорлы мыс қосылысы СuСІ -ды қарастыралық. Аталған қосылысқа СuСІ -молекуласы тек бұл зат газ күйінде ғана болғанда сәйкес келеді, Ал қатты күйінде оның молекуласы полимер тектес - (СuС1) n -формуласымен өрнектеледі және СuСІ - формуласы заттың қаттты күйіндегі «қарапайым» формуласын сипаттайды. Газ күйіндегі СuСІ - молекуласы мен осы заттың қатты күйіндегі түрі құрылымы және қасиеті жөндерімен бір-бірінен өзгеше болып келеді.
Мысалы, кальций карбонатының молекуласының құрылыс формуласын деп жазамыз, және мұнда үшінші оттек атомы тек көміртегімен ғана байланысып тұр. Ал зерттеулерге сүйенсек, жеке дара СаСО 3 молекуласының жоқ екендігін және осы зат құрамындағы үш оттек атомының бәрі де кальций, көміртегімен бірдей жағдайда байланысқандығы шығады. Осы күнге дейін СаСО 3 формуласымен мраморды, әктасты (известняк) борды өрнектеп келдік, ал шындығында қарап отырсақ, олардың қасиеті бір-бірінен өзгеше және бұл қосылыс қасиеті олардың алыну жолдарына тікелей қатысты. Мысалы, екі валентті титан тотығын (оксидін) алу барысында оның құрамы оттегінің қысымы мен сол жүйенің температурасына тікелей тәуелді болып келеді де ТіО 0, 58-1, 33 формуласымен өрнектеледі. Тотықтағы оттегінің 0, 58 -1, 00 -ге дейінгі құрамы оттегінің стехиометриялық шамадағыдан кем, ал 1, 00-1, 33 дейінгісі артық екендігін айғақтайды.
Сонымен, молекулалық құрылым, құрамы тұрақты болып келген химиялық қосылыстарға тән. Қатты күйдегі бейорганикалық заттарға беймолекулалық, яғни молекулалық емес құрылым түрлері тән. Осы себепті заттардың молекулалық және молекулалық емес құрылым түрлерін ескере отырып, стехиометриялық заңдылықтарға түзетулер енгізуді талап етеді:
Құрам тұрақтылық заңы (Пруст Ж. ) . Молекулалың цурылымдағы қосылыс-тардың құрамы оның алыну жолына тәуелсіз тұрақты болып келеді. Ал молекулалың құрылымы жоқ қосылыстардың қарастырылып отырған агрегаттың күйдегі құрамы оның алыну жолына тәуелді.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz