Кремний тотығының микроқаттылығының температураға тәуелділігін зерттеу


ТАРАЗ МЕМЛЕКЕТТІК ПЕДАГОГИКАЛЫҚ ИНСТИТУТЫ
БЕККУЛИЕВА МАРЖАН АТАБЕКҚЫЗЫ
« Кремний қос тотығы микроқаттылығының температураға тәуелділігін зерттеу»
6М011000-«Физика»
Физика магистрі академиялық дәрежесіне диссертация
Ғылыми жетекші:
Қ. Тоғжігітов
Тараз 2012
Мазмұны
Кіріспе . . .
I Қатты денелер және микроқаттылық
1. 1. Кристалдық күйдің, негізгі ерекшеліктері . . .
1. 2. Кристалдарды сұрыптау . . .
1. 3. Кристалдық торлардың физикалық қасиеттері . . .
1. 4. Кристалдық және аморфтық денелердiң құрылысы. Анизотропия . . .
1. 5. Кремний. Кремнийдің отттекті қосылыстары
1. 6. Микроқаттылық
II Қаттылық және оны анықтау әдістері
2. 1. Қаттылықты анықтау әдістері . . .
2. 2. Микроқаттылықты өлшеу құралы мен әдісі . . .
2. 3. Зерттеу материалдарына сипаттама . . .
III Кремний қос тотығының микроқаттылықтылығын зерттеу
3. 1. Кремний қос тотығының температураға байланысты микроқаттылығын анықтау . . .
3. 2. Қоспа ендірілген кремний қос тотығының микроқаттылығының температураға байланыстылығы . . .
3. 3. Ғылыми зерттеу элементтері бар «Микроқаттылыққа сынау» тақырыбында лабораториялық жұмыс . . .
Қорытынды . . .
Пайдаланылған әдебиеттер . . .
КІРІСПЕ
Курстық жұмыс тақырыбының жалпы сипаттамасы
Атомдық өндірістің дамуына байланысты баса аударылып отырған назар органикалық сорбенттер ішінде силикагель ерекше орын алады.
Кәдімгі органикалық иониттермен салыстырғанда органикалық емес сорбенттердің радиацонды - химиялық және термиялық орнықтылығы жоғары, сондықтан оларды радтохимиялық өндірістерде жоғары белсенді ерітінділерді қайта өңдеу үшін қолдану өте тиімді. Органикалық емес ион алмастырғыш материалдардың қолданысы олардың минералды қышқылдарда химиялық орнықтылығы жеткіліксіздігінен шектеулі.
Қатты денелердің физикалық, химиялық қасиеттері температуралық қыздыруға, сәулелендіру дозасына және диформациялану шамасына байланысты. Олар осындай әсерлерге кездескенде микроқұрылымдық өзгерістерге ұшырайды. Көптеген Москва, Ташкент ғалымдары диффузия коэффициентінің. адсорбция, катализдік қасиеттерінің өзгерісін ол материалдардың ескіруінен немесе химиялық қасиеттерінен деп қарастырады.
Мұндай жағдайлар Алматының ядролық ғылыми зеттеу институтының «Радиациялық» лабораториясындағы зерттеу жұмыстар нәтижелерінде орын алған. Әртүрлі газдардың мысалы, сутегі, оттегі және тағы басқа газдардың силикагелдегі адсорбциясын тексергенде белгілі бір температураға, дозаға дейін адсобция артады да, одан ары кемитіндігі байқалған.
Осы материалдардағы мыстың, алтынның, темірдің диффузия коэффициенттерін анықтағанға жоғарыдағыдай өзгерістің болатындығы байқалған.
Бұл материалдың рентген құрылымдық өзгерісін зерттегенде, құрылғанда фазалық өзгерістер болатындығын анықтаған. Аморфты силикагель - 500 С асқанда поликристалға, - 800 0 С - 900 0 С шамасында монокристалға одан жоғары температура артқанда аморфты жүйеге өтеді. Олай болса адсорбцияның диффузиялық өзгеруі материялдың тікелей құрылымдық өзгерісіне байланысты.
Осы жағынан келгенде кремний тотығының температураға байланысты құрылымдық өзгерісін тексеру ғылыми, практикалық жағынан пайдалы.
Диссертациялық жұмыс тақырыбының өзектілігі: Силикагель мен кварцтың структурасының өзгеруіне әкелетін физикалық процестерді түсіну үшін маңызды жоғарыда айтылған мәселелер, сонымен бірге ғылым мен техниканың практикалық сұранысынан туындайды.
Кварц қос тотығын температуралық қыздыруға байланысты зерттеу, оның микроқаттылығын анықтау өте маңызды. Материалдардың микроқаттылығын анықтау әдісі, негізгі рентген структуралық әдістеріне қосымша ретінде пайдаланылады.
Заттардың структурасының сәулелендіру және температура әсерімен өзгерісі атомдардың орын ауыстыруы мен кристал торы структурасында ақаулар түзілуіне байланысты. Радиация кезінде кристалдың қайттан ұрылуын кристалдың матералдарда төмен температурада әртүрлі физико - химиялық процестер өтуіне байланысты болуы мүмкін. Сондықтан заттардың яғни кремний және кварцтың структурасының термиялық өңдеу және сәулелендіруде өзгерісі күрделі мәселе болып табылады.
Абсорбенттер мен катализаторларды қолданылуымен байланысты ғылым мен техника дамуына орай олардың қасиеттеріне қатаң талап қойылады. Сондықтан алдын - ала берілген қасиеттерімен материалдар жасау, соның ішінде силикагельдерді жасау өзекті мәселе болып табылады.
Диссертациялық жұмыс тақырыбының мақсаты мен міндеттері: Ғылыми - зерттеу барысында магистрант жартылай өткізгіштер мен диэлектриктердің микроқаттылығын анықтау үшін мына төмендегідей мәселелерді меңгеру қажет.
а) ПМТ - 3 микроқаттылықты анықтау құралында жұмыс істей білу.
б) Жүктеменің шамасын табу әдісін игеру.
в) Материалдардан үлгілер дайындау.
г) алынған зерттеу нәтижелерін физикалық тұрғыдан талқылай білу.
Диссертациялық жұмыс тақырыбының зерттеу нысандары: Силикагельден, кварцтан үлгілер дайындау. Оларды әртүрлі органикалық қоспалардан тазарту үшін вакуумдық 10
I Қатты денелер және микроқаттылық
1. 1Кристалдық күйдің, негізгі ерекшеліктері
Енді атомдық-молекулалық деңгейде заттың қатты және сұйық күйлерін қарастырайык Табиғатта кездесетін қатты денелердің басым көпшілігінің құрылымы кристалдық болады деуге болады (минералдар және металдар қатты күйде кристалдар болып табылады) .
Кристалдық күйді сүйық жөне газ күйінен ажырататын негізгі сипат оларда анизотропияның болатындығы: кристалдың кейбір физикалық (механикалық, жылулық, электрлік, оптикалық) қасиеттері бағытқа тәуелді болады.
Қасиеттері барлық бағыттарда бірдей болатын денелер изотропты деп аталады. Газдар және сұйықтармен қатар аморфтық қатты денелер изотропты болып табылады.
Кристаллдардың анизотроптығының себебі оларды түзетін бөлшектердің (атомдардың немесе молекулалардың) реттілікпен орналасуында. Бөлшек-тердің реттілікпен орналасуы кристалдардың сыртқы жақтарының дұрыс гео-метриялық пішінде болуынан-ақ көрінеді. /13/
Кристалл атомдардың реттілікпен орналасуы олардың геометриялық дұрыс пішіндегі кеңістіктік тордың түйіндерінде орналасуларының арқасында болады. Тұтас кристаллды элементар кристаллдық ұяшық деп аталатын бір ғана кұрылымдық элементі түрліше үш бағыттарда көп қайтара қайталау арқылы алуға болады . Кристалл ұяшығының а, Ь және с қабырғалары кристалдың периодтары деп аталады.
Кристалл ұяшығы дегеніміз модулдері кристалл периодтарына тең болатын а, Ь және с үш векторларына тұрғызылған параллелипед болып табыла
ды. Бұл параллелипипед а, Ь және с кабырғалармен қатар қабырғалар арасындағы а, β және γ бұрыштарымен де сипатталады а, Ь, с, а, Р, жөне ү шамалар эле-ментар ұяшықты бір мәнділікпен сипаттайды және де оның параметрлері деп аталады.
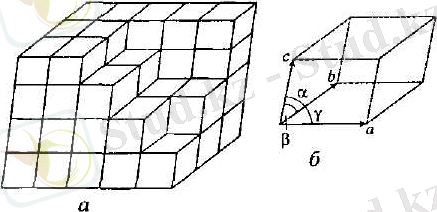
1. 1-сурет
Элементар ұяшықты түрліше тәсілдермен алуға болады. Мұны жазық құрылым мысалынан көруге болады. Қабырғаны ашық жөне күңгірт үш бұрыш плиткалармен кезектестіре жауып шығу үшін екі бағытта түрліше ұяшықтарды көптеп қайталап өтсе жеткілікті (мысалы 1, 2 жөне 3 үяшықтарды; сілтемелермен үяшықтардың қайталанып отыратын бағыттары көрсетілген) . 1 және 2 ұяшықтарға құрылымдық элементтердің максимал саны кіреді: бір ашық және бір күңгірт плиткалар. Кристалдық заттың химиялық құрамын сипаттайтын атомдардың мүмкін ең аз санынан тұратын кристалдық ұяшық (мысалы, мұз кристалы үшін бір оттегі атомы және екі сутегі атомы), примитивтік (қарапайым) ұяшық деп аталады. Бірақ көбіне симметриясы бүтін кристалдың симметриясындай болатын көптеген атомдардан түзілетін элементар ұяшықты таңдайды. Мәселен, 1. 1-суреттегі жазық құрылғы плитка-ның төбесі арқылы өтетін өзіне перпендикуляр кез-келген өстен 120°-қа бұрғанда өзімен-өзі бірдей түседі, 3 ұяшықтың да симметриясы дәл осындай. 1 және 2 ұяшықтардың симметрия дәрежесі бұдан төмен: олар өзді-өзімен тек 360°-қа бұрғанда ғана бірдей түседі. /13/
Ең аз санынан тұратын кристаллдық ұяшық (мысалы, мұз кристаллы үшін бір оттегі атом және екі сутегі атомы), примитивтік(қарапайым) ұяшық деп аталады. Бірақ көбіне симметриясы бүтін кристалдың симметриясындай болатын көптеген атомдардан түзілетін элементар ұяшықты таңдайды. Мәселен, 5. 2-сурет екі жазық құрылы м, плитканың төбесі арқылы өтетін өзіне перпендикуляр кез-келген осьтен 120°-қа бұрғанда өзімен-өзі бірдей түседі, 3 ұяшықтың да симметриясы дәл осындай. 1 және 2 ұяшықтардың симметрия дәрежесі бұдан төмен олар өзді-өзімен тек 360°-қа бұрғанда ғана бірдей түседі.
1. 2 Кристалдарды сұрыптау
Кристалдық тордың симметриясы түрліше болады. Кристалдык, тордың симметриясы деп тордың кейбір кеңістіктік орын ауыстырулар кезінде і өзі -өзімен бірдей түсу қасиеті аталады.
Кез-келген тордың ең әуелі трансляциялық симметриясы болады, яғни оны период шамасына орын ауыстыртқан кезде өзімен-өзі бірдей түседі. Симметри-яның басқа турлерінен ерекше айта кететініміз кейбір осьтерден бұрылуға сим-метрия және белгілі жазықтыктарға қатысты айналық шағылу симметриясы.
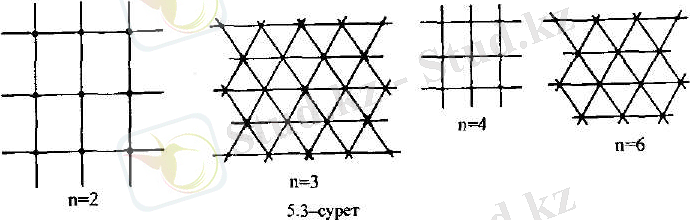
Егер тор кайсы бір оське қатысты 2л/ п бұрышқа бұрған кезде өзімен өзі бірдей түсетін болса ( демек, тор осьті толық бір рет айналып шыққанда, ол өзімен өзі п рет бірдей түседі), онда мүндай ось п~ реттік симметрия осьі деп аталады. Ең қарапайым 1-реттік осьпен қатар, 2-, 3-, 4-жөне 6-реттік осьтер болады. Осындай симметрия осьтері бар құрылымдардың сұлбасы 5. 3-суретте көрсетілген ( ақ, қара шеңбершелер және айқыштармен атомдардың түрліше түрлері белгіленген) .
Айналық шағылу кезінде тордың өзімен-өзі бірдей түсетін жазықтығы сим-метрия жазықтығы деп аталады. Симметрия жазықтығының мысалы 5. 3-суретте көрсетілген. Кристалдық тордың бір мезгілде бірнеше симметриялары болады. Барлық кристалдар элементар ұяшықтың пішініне қарай жеті кристаллографиялық жүйелерге бөлінеді, олардың әрбіреулеріне бірнеше симметрия түрлері кіреді.
Олар:
І. Триклиндік жүйе. Ол үшін а=Ь=с, β=α=γ.
Элементар ұяшық көлбеу параллелипед түрінде болады.
2. Моноклиндік жүйе. Екі бұрышы тік, ал үшінші бұрышы тік емес
(ол үшін р бұрышын алу келісілген) : а а=Ь=с,, а = β = 90°; β= 90°. Элементар ұяшық тік призма түрінде болады, оның табанында параллелограмм (яғни тік параллелепипед) түрінде болады.
З. Ромбикалық жүйе. Барлық бұрыштары тік, барлық қабырғалары түрліше: а^ЬФс, а~ (3 = у = 9Ъ° ■ Элементар ұяшық тік бұрышты параллелипипед түрінде.
4. Тетрогоналдық жүйе. Барлық бұрыштары тік, екі кабырғасы бірдей:
афЪ^с, а- р = ү = 90°. Элементар ұяшық табаны квадрат тік призма.
5. Ромбоэдр немесе тригоналдық жүйе. Барлық қабырғалары бірдей, барлық бұрыштары да бірдей, бірақ тік бұрыш емес: а = Ъ = с; а - В = / ^ 90°. Элементар ұяшық диагональ бойымен сығылған немесе
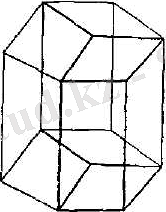
созылған куб түрінде болады.
6. Гексагоналдық жүйе. Қабырғалары мен олардың арасындағы бұрыштары мына шартты канағат-
тандырады: а = Ь*с; а = /? = 90°, у = 120°. Егер үш
элементар ұяшықтарды бірге 5. 4-суретте көрсетілгендей қосса, онда дұрыс алты жақтық призма шығады.
7. К у б т ы қ (текшелік) жүйе. Барлық қабырғалары-
бірдей, барлық бұрыштары тік: а = Ъ = с;а = Р = ү - 90°, . Элементар ұяшық куб (текше) түрінде. /14/
1. 3 Кристалдық торлардың физикалық қасиеттері
Кристалдық тордың түйіндерінде орналасқан бөлшектердің табиғатына және бөлшектердің арасындағы өзара әрекеттесу күштерінің сипатына байланысты кристалдық торларды төрт түрге бөледі және осыған сәйкес кристалдардың төрт түрі болады: иондык, атомдық, металдық және молекулалық.
І. Иондық кристалдар. Кристалдық тордың түйіндерінде түрліше таңбалы иондар орналасқан. Олардың арасындағы өзара өрекеттесу күштері негізінен электрлік (кулондык) болып табылады. Түрліше зарядталған ион-дардың арасындағы электростатикалық тартылыстан туатын байланыс г е -терополярлық (немесе иондық) деп аталады. Иондық тордың мысалына ас түзынын (МзС/) өрнектелген торын келтіруге болады. Бұл тор кубтық жүйеге жатады. Ак, шеңбершектер оң зарядталған натрий иондары да, ал қара шеңбершектер мен хлордын теріс иондары белгіленген. Иондық кристал моле-кулалардан емес, иондардан түрады. Тұтас кристалды аса зор бір молекула деп қарастыруға болады.
2. Атомдық кристалдар. Кристалдық тордың түйіндерінде бейтарап атомдар орналасқан. Кристалдағы бейтарап (сонымен бірге молекуладағы да) атомдарды байланыстыратын байланыс гомеополярлық (немесе коваленттік) деп аталады. Гомеополярлық байланыс күштері де электрлік сипатта болады (бірақ кулондык емес) . Ол күштерді тек кванттық механика негізінде ғана түсіндіруге болады.
3. Металдық кристалдар. Кристалдық тордың барлық түйіндерінде металдың оң иондары орналасқан. Олардың арасында газ молекулаларына ұқсас, иондар түзілген кезде атомдардан үзіліп қалған электрондар бей-
берекет қозғалып жүреді. Бүл электрондар оң иондарды шашыратпай ұстап тұратын ""цемент" ролін аткарады; басқаша болса, оң иондар арасындағы тебілу күштерінін әсерінен тор быт-шыт болған болар еді. Сонымен қатар иондар да электрондарды сыртқа шығармай тор ішінде ұстап тұрады.
4. Молекулалық кристалдар.
белгілі түрде бағдарланған молекулалар орналасады. Кристалдағы молекулалардың арасындағы байланыс күштерінің тегі де газдарды идеалдықтықтан ауытқытатын молекулалар арасындағы тартылыс күштерімен бірдей. Сол себептен оларды В а н-дер-в а л ь с т ы қ күштер деп атайды. Мысалы, мына
заттардың молекулалық торлары болады: Н 2 , М 2 , О 2 , СО 2 , Н 2 О. Сөйтіп, байырғы мұз да, құрғақ мұз да (қатты көмір қышқыл) молекулалық кристалдар болып табылады екен.
1. 4. Кристаллдық және аморфтық денелер
Физикалық қасиеттеріне және молекулалық құрылысына сәйкес барлық қатты денелер екі класқа - аморфтық және кристаллдық денелер болып бөлінеді. Аморфтық денелерге тән ерекшелік - бұл олардың изотроптығы , яғни барлық физикалық қасиеттерінің (механикалық. оптикалық) бағытынан тәуелсіздігі. Изотропты қатты денелердің молекулалары мен атомдары хаостық түрде, бірнеше бөлшектерді құрайтын шағын топтар құрайды. Структурасы бойынша аморфтық денелер сұйықтыққа ұқсас болып келеді. Аморфтық денелердің мысалы болып шыны, қатып қалған смола (янтарь), пластиктер табылады. Егер аморфтық денені қыздырса, ол біртіндеп жұмсарады, және сұйық түрге өтуі үлкен температураны қажет етеді.
Кристалл денелерде бөлшектер қатаң ретте, дененің бүкіл көлемінде қайталанып отыратын кеңістіктік структураларды құрайды. Осындай структуралардың көрнекі түсінігін алу үшін, кеңістіктер кристаллдық торлар қолданылады. Мұндай торлардың түйіндерінде атомдардың немесе молекулалардың центрлері орналасады. Көп жағдайда кристаллдық тор атом иондарынан тұрады. Мысалы аз тұзының торы NaCl молекулаларына қос-қостан бірікпеген Na + және Cl - иондарынан тұрады (1. 5-сурет) . Мұндай кристалдарды иондық деп атайды. /15/
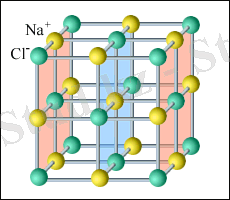
1. 5-сурет. Ас тұзының кристалдық торы.
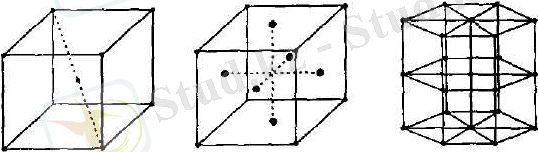
Әрбір тордан элементарлы ұяшық деп аталатын ең аз өлшемді структуралық элементті бөліп алуға болады. Бүкіл кристалдық тор элементарлық ұяшықты қандай да бір бағыт бойынша параллельдік көшіру ( трансляция ) арқылы тұрғызылады. Барлығы 230 әр түрлі кеңістіктік кристалдық структура болуы мүмкіндігі теория жүзінде дәлелденген. Олардың көпшілігі табиғатта анықталды немесе қолдан жасалынды. Металдардың кристалдық торы 6 қырлы призма тәріздес (цинк, магний), қыры центрленген куб тәріздес (мыс, алтын) немесе көлімдік центрленген куб тәріздес (темір) болады. Кристалдық денелер монокристалды немесе поликристалды болуы мүмкін. Поликристалдық денелер кристаллит деп аталатын хаосты біріккен көптеген кішкентай кристалдардан құралған. Үлкен монокристалдар табиғатта және техникада сирек кездеседі. Жиі кездесетін кристалдық денелерге поликристалдар жатады. Монокристалдарға қарағанда, поликристалдық денелер изотроты, яғни олардың қасиеттері барлық бағытта бірдей болады. Қатты дененің поликристалдық құрылысын микроскоптың көмегімен, ал кейде ол көзбен де (шойын) көрінеді. Көптеген заттар физикалық қасиеттерімен өзгешеленетін бірнеше кристалдық модификацияларда (фазаларда) болуы мүмкін. Бұл құбылыс полиморфизм деп аталады. Бір модификациядан екінші модификацияға өту полиморфты өту деп аталады. Полиморфты өтудің қызықты әрі маңызды мысалы - графиттің алмазға өтуі. Өндірісте жасанды алмаздардың мұндай өтуі 60-100 мың атмосферада және 1500-2000 К температурада жасалады. Кристалдық торлардың структуралары тәжірибелік жолмен монокристалдық және поликристалдық үлгілерде рентгендік сәуле шығарудың дифракциясы көмегімен зерттеледі. 2-суретте қарапайым кристалдық торлардың мысалдары келтірілген. Кристалдағы бөлшектер қатты жиналған, сондықтан олардың центрлерінің арасындағы ара қашықтық бөлшектердің өлшемдеріне тең болады.
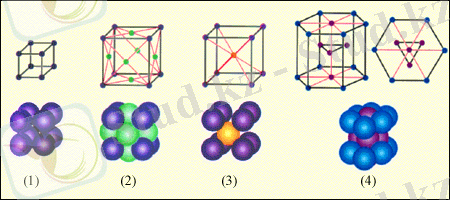
1. 6-сурет. Қарапайым кристалдық торлар:
1 - қарапайым кубтық тор, 2 - қыры центрленген кубтық тор,
3 - көлемі центрленген кубтық тор, 4 - гексагондық тор.
Қарапайым кубтық торда бөлшектер кубтың төбелерінде орналасады. Қыры центрленген торда бөлшектер кубтың төбелерінде ғана емес, оның әрқайсы қырында орналасады.
1. 5-суретінде ас тұзының торы бір-біріне салынған Na + и Cl - тұратын қыры центрленген торлардан құралған. Көлемі центрленген кубтық торда қосымша бөлшек әрбір элементар кубтық ұяшықтың центрінде орналасады. Металдардың кристалдық структураларының маңызды ерекшелігі бар. Кристалдық тор құрайтын металдың оң зарядталған иондары «еркін электрондық газымен» әрекеттесу күштерімен тепе-теңдік жағдайында орнайды
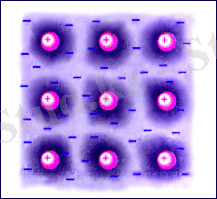
1. 7-сурет. Металдық кристалдың структурасы
Электрондық газ әрбір атом берген бір немесе бірнеше электрондардың есебінен құралады. Еркін электрондар бүкіл кристалл бойымен қозғалуы мүмкін.
Қатты денелер деп өзiнiң көлемi мен формасын сақтайтын денелердi айтады. Бөлшектердiң өзара тартылу күшi өте үлкен, оның әсерiнен молекулалар өзiне көршi орналасқан молекулалардан едәуiр ұзап кете алмайды. Олар кеңiстiкте тығыз, периодты турде қайталанатын ретпен орналасқан. Қатты денелердiң құрылымының негiзi, төбелерiнде бөлшектер - атомдар, молекулалар немесе иондар - орналасқан, дұрыс геометриялық формадағы элементар ұяшықтан тұрады. Бұл ұяшық, оның қабырғасына еселiк ұзындықтағы арақашықтықта қайталанатын, кристалдық торды құрайды. Қатты денелер бөлшектердiң алыс қатар (ретпен) орналасуымен сипатталады, яғни дененiң бүкiл көлемi бойында элементар ұяшық геометриясы бiрнеше (көп) рет қайталанады. Қатты денелердегi бөлшектердiң жылулық қозғалысы - олардың тепе-теңдiк жағдайына қатысты бейберекет тербелiсiн бередi. Кристаллды тордың байланыстары болады.
1. 5 Кристалдық және аморфтық денелердiң құрылысы. Анизотропия

Атомдары немесе молекулалары реттелiп орналасқан және периодты түрде қайталанып тұратын iшкi структурасын түзетiн қатты денелер кристаллдар деп аталады. Кристалдардың қырлары әрқашан жазық және дұрыс геометриялық пiшiндi болып келедi (1. 8, 1. 9 - суреттер) . Бөлшектердiң орналасуының салыстырмалы түрде орныққан скелетi кристалдық торлар деп аталады, ал сол торлардың орналасқан орындары түйiндер деп аталады (1. 10 - сурет) .

Кристалдардың сыртқы пiшiнiнiң дұрыстығы - олардың реттелген құрылысының бiр ғана салдары емес. Олардың ең басты ерекшелiгi кристалдың физикалық қасиеттерiнiң ондағы таңдалған бағытына байланыстылығында. Кристалдардың бұл қасиетi анизотропия деп аталады. Барлық кристалды денелер анизотропты болып келедi. Анизотропияның бiр себебi - кристалдық тор түйiндерiнiң тығыздығы әр түрлi бағытта әр түрлi болған жағдайдағы, бөлшектердiң дұрыс ретпен орналасуы. Осы бағыттардағы бөлшектердiң өзара әсерi де бiрдей болмайды. Бұдан, әр түрлi бағыттардағы кисталдардың механикалық берiктiгi әр түрлi екендiгi шығады. Көптеген кристалдар жылу мен электр тогын әр бағытта әр-түрлi өткiзедi. Кристаллдың оптикалық қасиеттерi де оның бағытына байланысты болуы мүмкiн.
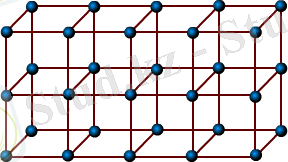
Белгiлi бiр температураға дейiн қыздырғанда (әр заттың өз температурасы бар ) зат қатты кристалдық күйден сұйық күйге өтедi. Осы процесс балқу деп аталады, ал балқуға ұшырататын температура балқу температурасы деп аталады.
Монокристалдар мен поликристалдар. Қатты денелердiң негiзгi түрiне металдар жатады. Олардың да кристалдық структурасы бар. Бiрақ, бiр қарағанда, олардың кристалдық құрылымы не сырт пiшiнiнен, не физикалық қасиеттерiнен байқалмайды. Металдар кәдiмгi күйде анизотропияны анықтай алмайды. Себебi металл көптеген өзара бiтiсiп кеткен кiшкентай кристаликтерден тұрады. Олардың әр қайсысының қасиеттерi бағытына байланысты, бiрақ олар бiр-бiрiне қарағанда ретсiз бағытталған. Сондықтан, көлемi жекелеген кристаликтердiң көлемiнен анағұрлым үлкен металл iшiндегi барлық бағыттар тең және оның қасиеттерi барлық бағытта бiрдей болады.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz