Радиобиология мен ядролық физикаға кіріспе: тарихы, радиоактивтік ыдыраулар және дозиметрия негіздері


Дәріс 1
КІРІСПЕ. ПӘННІҢ МАҚСАТЫ МЕН ҚЫСҚАША ДАМУ ТАРИХЫ.
- Радиобиология және ветеринарлық радиобиолог ия.
- Радиобиологияның қысқаша даму тарихы.
- Радиобиологияныңң дамуына ғалымдардың қосқан үлесі.
1896 жылдың 1 марты ғылым тарихына тағы да бір жаңалық әкелді. Францу физигі Анри Беккерель уран тұздарының белгісіз бір сәуле шығаратындығын байқады.
Беккерельдің бұл жаңалығы кездейсоқ емес еді. 1985 жылы неміс ғалымы Рентген белгісіз сәулелерді ашты. Ол оны Х-сәулелер деп атады. Бұл ХІХ ғасырдың аяғындағы ең ірі ғылыми жаңалықтардың бірі болды. Енді ғалымдар осы сәуленің тегін іздестіре бастады. Ол үшін көптеген әр алуан заттар зерттелді. Француз ғалымы А. Пуанкаре фосфоросцениялық (жарқырайтын) қасиеттері бар заттарды зерттеуді ұсынды. Олар алдын ала жарықта ұстағаннан кейін қараңғыда да біраз уақыт өзінен өзі жарық шығаратын. Енді осындай заттар рентген сәулелерін шығармас па екен деген болжамды анықтай түсу керек болды.
Анри Беккерель қараңғыда жарық шығару қасиеті күшті уран мен калийдің қос күкіртті қышқыл тұзын K 2 UO 2 (SO 4 ) 2 алады. Бірақ ауа райы бұлтты, тұманды болып, алдын ала күн жарығында ұстауға мүмкіндік болмағандықтан, оны фотопластикада салып, қара қағазға орап, столының тартпасына қояды. 1 март күні күн ашық болыпты. Беккерель тартпадағы уран тұзын алып, күн көзіне ұстамай тұрып, алдымен фотопластинканы Ғалымдар радиоактивтік сәулені мұқият зерттей бастады. Көп ұзамай-ақ Беккерель уран бөліп шығаратын сәле ауаны иондандыратынын анықтайды. Ол уран сәулесімен магнит өрісінде қисаяды деген болжал жасап, 1899 жылы тәжірбие арқылы шынында солай болатындығын және уран сәулелері қасиеттері жағынан катод сәулелеріне ұқсайтындығын дәлелдеді. Бірнеше жыл өткеннен кейін ағылшын физигі Э. Резерворд уран сәулелерінің үш түрге бөлінетінін дәлелдеп, олар а- (альфа), в-(бета) және у-(гамма) сәулелері деп аталады.
Бұл жаңа құбылысты зерттеуде Мария және Пьер Кюрилер еңбегінің маңызы зор болды. Олар Беккерельдің зерттеулерін, одан әрі жалғастырып, дамыта түсті, Сөйтіп, уранның табиғи минералды (мысалы, шала тотық - U 3 O 8 ) таза металл уранға қарағанда сәулені күштірек шығаратынын байқайды. Олар уранның табиғи қосылыстарында ураннан да активті зат бар деген болжал жасайды. Екі жылғы зерттеуден кейін 1898 жылы олар сәуле шығаратын жаңа элемент - полонийді және көмекшілер Ж-бемонмен бірге екінші активті элемент - радийді ашады. Мария Кюри-Склодовскаяның ұсынысты бойынша бұл жаңа құбылыс радиоактивтілік зерттеудегі сіңірген еңбектері үшін оларға және Анри Беккерельге Нобель сыйлығы, 1911 жылы радий элементін таза күйніде бөліп алғаны үшін Мария Кюриге екінші рет Нобель сыйлығын берілді.
Мария және Пьер Кюрилердің радиоактивтілікті зерттеулері бүкіл дүние жүзі ғалымдарының назарын аударды. Бұл мәселемен ағылшын физиктері Э. Резерфорд. Ф. Содди, Ф. Фаянс айналысты. Соның нәтижесінде радий мен ураннан басқа да бірқатар элементтердің радиактивтілігік қасиеті бар да бірқатар элементтердің радиоактивтілік қаиеті бар екендігін анықталды. Атап айтқанда, реттік номері 84-тен бастап 92-ге дейінгі элементтердің барлығы да радиоактивті екен. Ал 92-ші элемент уран -алғаш ашылған радиоактивті элемент.
Радиоактивті элементтердің көптеп ашылуы ғалымдарды тағы да бір тұйыққа тіреді. Істің мәнісі былай еді. Ол кезде бір элементтің радиоактивтілік қасиеті байқалса болды, ол жаңа элемент деп есептелетін. Сондықтан да 1910-1915 жылдардың өзінде-ақ олардың саны 30-дан асып, периодтық системада орын жетпеді.
Осы кезде, яғни 1911 жылы Э. Резерфорд атом құрлысының ядролық моделін ұсынды. Ол модель жүретін теріс зарядталған электрондардан тұрады. Элементтің химиялық қасиеттері сыртқы қабаттардағы электрондарға байланысты. Атом құрлысы жайлы Э. Резерфорд ұсынған модельге сұйене отырып, Ф. Содди атомдарының радиоактивтік қасиеті ядроға, ал химиялық қасиеттері электрондарға байланысты болады, сондықтан химиялық элементті құрайтын атомдардың бірдей болмауы мүмкін деген пікір айтты. Ф. Содди өзінің бұл теориясына дейін де кейбір жаңадан ашылған радиоактивті элементтердің химиялық, сондай-ақ физикалық қасиеттерінің өте ұқсас екендігін, тек радиоактивті қасиеттерінде ғана айырмашылық барлығын байқайды. Мәселен уран-Х1 радиоторий және ионий «элементтерін» бір-бірінен және бұрыннан белгілі болған торий элементінен бөліп алу мүмкін емес.
1910 жылы У. Марквальд пен Ф. Содди мезоторий-1 және радийдің химиялық қасиеттері негізінен ұқсас екендігін және олар химиялық радиакуаларда бірдей қасиет көрсеткендігін анықтайды. Әсіресе, венгер физигі Г. Хеваши мен Ф. Панеттің бұл жөніндегі зерттеу жұмыстары көңіл аударарлық болды. Олар радий-Д мен қорғасынды айырып, бөлу үшін әр түрлі 20-ға жуық әдіс қолданып, бірнеше жыл еңбек етті. Бірақ олардың бұл әрекетінен ешнәрсе шықпады. Осындай жұмыстардың нәтижесінен еліп бөлінбейтін элементтердің бірдейлігі туралы ой туды. Сөйтіп, осындай фактілердің негізінде Ф. Содди өзі ұсынған теориясын дамыта отырып, 1913 жылы К. Фаяс екеуі ғылымға радиоактивті элементтердің изотоптары жайлы ұғым енгізді.
Радиоактивтілік деген не?
Бұл сұраққа жауап беру үшін алдымен атомның ішкі құрылысынан біраз хабардар болуымыз керек. Атомның ішкі құрлысын анықтауда радиоактивтіліктің ашылуы шешуші роль атқарады.
1920 жылы Э. Резерфорд нейтрон бөлшектерінің бар екнедігін туралы болжау айтты. Резерфордтың шәкірті Дж. Чэвдик массасы 1-ге тең, электр заряды жоқ нейтрон бөлшектерінің шынында бар екендігін тәжірбие арқылы дәлелдеді. 1932 жылы совет ғалымдары Д. Иваненко мен Е. Гапон және неміс ғалымы В. Гейзенберг атом ядросының протон-нйтрондық моделбін ұсынды. Сонымен қазіргі кездегі ғылыми теория бойынша атом ядро мен оны айналып жүретін электрондардан, ал ядроның өзі протон мен нейрон бөлшектерінен құралады. Протонның ассасы 1-ге, электр заряды +1 ге тең, ал нейронның массасы 1-ге тең де, электр заряды болмайды. Протондар Р деп, ал Нейрон Т деп белгіленеді. Жоғары сан бөлшектің массасын, ал төменгісан электр зарядын көрсетеді.
Атомдардың шамасы өте кішкентай. Оның көлденеңі 10-8 см, демек, 1 см ұзындыққа 100 млн атомды қатарлап түзіуге болады. Ең жеңіл деген сутек атомның масасы 1, 67-10-24 . Атом масасының негізгі бөлігі (99, 95%) көлемі жағынан аса кішкентай ядроға жинақталған. Атомдағы электрондар саны тұрақты және периодтық системадағы элементтердің рет номерініне тең болады. Ядродағы протондар саны да элементтің реттік номеріне тең келеді. Электрондар мен протондардың саны өзара тең болғандықтан, атом тұтас алғанда электр түріне орналасады. Ең алыстау қабаттағы электрондардың ядромен байланысы әлсіз, сондықтан олар басқа атомдармен оңай әрекеттеседі. Осы сыртқы қабатағы электрондардың ядромен байланысы әлсіз, сондықтан олар басқа атомдармен оңай әрекеттеседі. Осы сыртқы қабаттағы электрондардың саны элементтердің химиялық қасиетін, яғни оның басқа элементтермен әрекеттесіп әр алуан химиялық қосылыстар түзу қасиетін белгілейді.
Радиоактивтіліктің сырын ашу жөнінде көптеген ғалымдар еңбек етті. Ең алдымен радиоактивтілікке әсер етуге болмайтындығын анықталды.
Дәріс 2.
ЯДРОЛЫҚ ФИЗИКА ЭЛЕМЕНТТЕРІ.
- Атомның құрылысы туралы осы заманғы түсінік.
- Атом құрамына кіретін элементарлы бөлшектердің физикалық сипаттамасы.
- Атомдардағы бөлшектердің байланыс энергиясы.
Аса жоғары температураға дейін қыздыру, өте салқындату, жоғары қысым мен сиретілген вакумм, түрлі химиялық реактивтермен әсер ету - міне, бұлардың ешқайсысы да радиоактивтілікті бәсеңдетіп, немесе оны жылдамдата алған жоқ. Сонымен қатар кез келген адиоактивті заттың сәуле шығару интенсивтігі уақыт өткен сайын белгілі бір заңдылық бойынша өздігінен азаятындығы байқалды. Әрбір радиоактивті затқа жартылай ыдырау кезеңі тура келеді. Жартылай ыдырау кезеңі дегеніміз -сәуле шығару интенсивтігі екі есе азаятын уақыт мөлшері. Бұл уақыт ішінде радиоактивті атомдардың жартысы ыдырайды. Мысалы радийдің жартылай ыдырау кезеңі -1620 жыл, полонийдікі -138 күн, урандікі -4, 5 млрд жыл және т. с. с.
Радиоактивті заттың мөлшерін бір уақыт бірлігінде ыдырау санымен өлшейді. Радиоактивтіліктің өлшем бірлігі ретінде кюри алынған. Бір кюри -1 секундта 3, 7 10 10 ыдырауға тең. Бір грамм радийдің радиоактивтігі бір кюриге де жиі қолданылады: мкюри (милликюри) және мюкюри (микрокюри) ; 1 мкюри - 0, 001 кюриге, 1 мккюри - 0, 001 мкюриге немесе 0, 000 001 кюриге тең. Ядролық сәуленің энергиясын электронвольтпен (эв) өлшейді. Бұл -масасы мен заряды электрондікіне тең бөлшектің потенциалдар айырмасы 1 вольтті (в) өткенде алатын энергиясы. 1 эв - 1, 6- 10 -12 эрг.
Ядролық әуленің энергиясы кез келген элементтің сыртқы электрон қабаттарындағы электрондардың байланыс энергиясынан әлдеқайда көп. Заттың қабатынан өткенде ядролық сәуле оның атомдарын иондандырып, ал өзі энергиясын біртіндеп жоғалтады. Осының нәтижесінде бос электрондар пайда болады да, атомның қалған бөліктері оң зарядталған иондарға айналады. Осыған байланысты кейде ядролық сәулені онын иондандыру қасиетімен, яғни иондандырушы бөлшектіңкі емесе кванттың (электромагниттік сәуленің) жүріп өткен бір см жолында түзілген нондардың жұбымен сипаттайды. Ғалымдар ұзақ жылдар бойғы зерттеу жұмыстарының нәтижесінде радиоактивтік өзгерістердің бірнеше түрі болатындығын анықтады.
Радиоактивтік өзгерістің бірінші түрі альфа ыдырау деп аталады. Ол кысқаша а-ыдырау деп жазылады (а - грек алфавитінің бірінші әрпі - альфа) . Альфа-ыдырау кезінде радиоактивті элементтер альфа-бөлшек-терін бөліп шығарады. Альфа-белшектерінің құрамында 2 протон және 2 нейтрон бар, массасы 4-ке, ал заряды + 2-ге тең. Бұлар- гелий атомдарының ядролары. Альфа-ыдырау нәтижесінде бастапқы ядроның заряды 2-ге, ал массасы 4-ке кемиді.
Сондықтан жаңадан пайда болған элементтің ядросы периодтық системада бастапқы элементке карағанда 2 клетка солға тамаи орналасқан элементке жатады. Бұған мысал ретінде торий элементінің радиоактивті ыдырауын келтіруге болады:
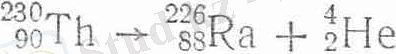
Қабылданған ереже бойынша ядролық реакция теңдеуінде алдымен реакцияға катысатын элементтің немесе бөлшектің таңбасы одан соң таңбаның жоғарғы сол жағына элементтің (белшектің) массасы, төменгі сол жағына заряды жазылады. Теңдеудің он жағына (стрел-кадан кейін) реакцпя нәтижесінде пайда болған элементтер (бөлшектер) де осы тәртіппен жазылады. Кейде ядролық реакция нәтижесінде түзілетін жаңа бөлшектер стрелканың үстінде болады. Мысалы:

Ал ядролық физикада реакция теңдеуін бұдаи да қысқартып жазады. Атап айтқанда, алдымен өзгеріске ұшырайтын ядро таңбасы, одан кейін жақшаның ішіне ядролық реакцияны тудыратын белшектің, оның қатары-на реакция нәтижесінде түзілетін бөлшектің таңбалары, ал жақшадан кейін жаңадан пайда болатын ядроның таңбасы жазылады. Мысал ретінде азот атомдарын альфа-бөлшектерімен атқылау реакциясын келтірелік:
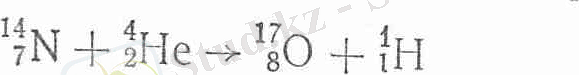
Қысқартып жазғанда былай болады:
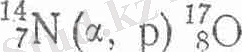
Біз бұдан былай ядролық реакцияларды жазудың толық түрін ғана колданамыз.
Альфа-ыдырау табиғатта кеңінен таралған деуге болады. Қазіргі кезде белгілі радиоактивті изотоптардың 10%-ке жуығы альфа-белшектерін бөле отырып ыдырайды. Изотоптар таблицасында 160-қа жуық альфа-активті изотоптар бар. Олардың көбісі периодтық системаның сонғы жағына орналасқан (2>82) элементтердікі.
Альфа-бөлшектерінің иондандыру қасиеті өте жоғары: альфа-бөлшегінің ауадағы 1 см жолында 3 жүп ион тузіледі. Алайда, заряды мен массасы аса үлкен болғандықтан альфа-бөлшектерінің өткіштігі азғантай. Қалцийдығы 0, 1 мм қағаз қабаты альфа-бөлшектерін толық сініре алады.
Радиоактивтіліктіқ ең көп тараған түрі - бета-ыдырау ((3-ыдырау) . Бета-активті ыдырау кезінде элемент ядросы электрондар бөліп шығарады. Бета-активті изотоптық массасы өзгермейді, тек ядро зарядының мөлшері 1-ге артып, периодтық системада бір клетка оңға та-ман орналасқан элементтің ядросына айналады.
Бета-активті ыдырау табиғатта кеңінен таралған. Қазіргі кездегі ғылымға белгілі изотоптардың 46%-і электрон ыдырайды.
Бета-ыдыраудың әте күрделі құбылыс екендігі анықталды. Біріншіден, бета-активті ыдыраудың бірнеше түрлері болатындығы ашылды. Олар мыналар: бета-минус - ыдырау (р-ыдырау), бета-плюс-ыдырау (й+-ыдырау) Тәжіс орбиталық ( электрондық) қармап алу.
Бета-минусыдырау кезінде электрон бөлініп шығады да, нәтижесінде бастапқы ядроға қарағанда, периодтық снстемада реттік номері бір клетка оңға орналасқан элементтің ядросы түзіледі. Мысалы, талий элементі изотопының ыдырауын алайық:
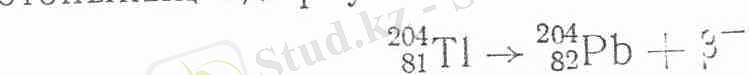
Енді бета-минус-ыдырауды түсіну үшін 1931 жылы американ ғалымы К- Андерсон ашқан позитрон бөлшегін еске түсіруіміз керек. Позитронның массасы мен заряд шамасы электрондікіне тең де, бірақ заряды қарама-қарсы, яғни оң. Позитрон ашылғаннан кейін үш жыл өткеннен соц ерлі-зайыпты Фредерик және Ирен Жолио-Кюрилер жасанды радиоактивтілікті ашты.
Дәріс 3.
ИОНДАУШЫ СӘУЛЕЛЕРДІ РАДИОМЕТРИЯЛАУ ЖӘНЕ ДОЗИМЕТРИЯЛАУ.
- Радиометрия және дозиметрия туралы түсінік, оның мақсаты мен міндеті.
- Иондаушы сәулелерді табу және тіркеу құралдары мен әдістері.
- Ионизациялық әдіс.
Осының негізінде ғалымдар кейбір жасанды радиоактпвті нзотоптардың позитрон беліп ыдырантындығын байқады. Радиоактивтіліктің жаңа түрі - позитрондық радиоактивтілік (немесе бета-плюс-ыдырау) осылай ашылды. Позитрон бөліп шығарған ядроның заряды 1-ге кемиді. Соның нәтижесінде периодтық системада бір клетка солға қарай орналасқан жаңа элемент түзіледі.
Бұл радиоактивтік ыдыраудың жаңа түрі тек жасанды радиоактивті изотоптарға ғана тән болып шықты. Табиғатта позитрон бөліп ыдырайтын элемент ядросы кезең дескен жоқ. Радиоактнвті изотоптардың 11%-і ғана по-І зитрон бөліп ыдырайды. Соның өзінде бүл бета-плюс- ыдырау периодтық системаның алғашқы жартысында орналасқан жеңіл элементтердің изотоптарында ғана кездеседі. Позитрондық ыдырауға мысал ретінде натрий изотоның неонға айналып ыдырауын келтіруге болады:
Енді бета-ыдыраудың үшінші түріне тоқталамыз. 1935 жылы американ физигі Л. Альварец атом ядролары кейбір жағдайларда жақын орналасқан электрон қабаттарынан электрондарды тартып алатындығын дәлелдеді. Бұл жағдайда электрон тартып алған ядроның заряды 1-ге кемиді. Бұл құбылыс орбиталық (немесе электрондық) қармап алу деп аталады. Радиоактивті ядролардың шамамен төрттен бірі осындай электрондық қармап алудың нәтижесінде өзгеріске ұшырайды. Орбиталық (электрондық) қармап алу көбінесе периодтық системаның екінші жартысында орналасқан элементтердің изотоптарында кездеседі. Өйткені олардың атомдарында бірінші электрон кабаттары ядроға жақындау орналасқандықтан оның электронды тартып алуы оңайлайды. Егер ядро өзіне ен таяу орналасқан К электрон қабатындағы электронды тартып алса, оны К - қармап алу, 2 қабатынан тартып алса, 2 - қармап алу деп атайды. Кейде бір ядроның өзі К - қармап алу жолымен де немесе позитрондық ыдырау жолымен де өзгеруі мүмкін. Біз бұл жерде радиоактивті «айырмен» кездесіп отырмыз. Мысалы, прометий-142 изотопы осьшдай екі жолмен бір мезгілде ыдырайды. Кейбір изотоптарда электрондық қармап алу да, бета-минус-ыдырау да кездеседі. Мыса-лы, кеңінен таралған калий-40 изотопы ядроларының 89%-і электрон бәліп ыдырайды да, ал қалғандары К қармап алу жолымен өзгереді. Ал марганец-52 нзотопы ядроларының 33%-і бета-плюс-ыдырау, ал 67%-і К қармап алу жолымен хром-52 изотопына айналады. Тіпті бір мезгілде бета-ыдыраудың үш түрі арқылы езгеретін ядролар да кездеседі. Мыс-64 изотопы ядроларының 40%-і орбиталық қармап алу, ал 20%-і позитрондық ыдырау (бета-плюс-ыдырау) жолымен өзгеріске ұшырайды.
Сөйтіп, бета-ыдырау деген атпен радноактивтік ыдыраудың жеке-жеке үш түрі біріктірілген: бета-минус-ыдырау (электрон шығару), бета-плюс-ыдырау (позинтрон шығару) және орбиталық (электрондық) қармап алу. Радиоактивті нзотоптардың оннан тоғызы дерлік осы үш түрлі жолдың бірімен өзгеріске ұшырайды.
Енді біздің алдымызда тағы да бірнеше сұрақ туады. Біріншіден, ядро протон мен нейтрондардан ғана кұралған деген теория бойынша, оның құрамында электрон да, позитрон да болмауы тиіс. Алайда іс жүзінде радиоактивтік ыдырау кезінде электрон да, позитрон да ядродан ұшып шығып жатады. Олар кайдан пайда болады? Екіншіден, кез келген бета-активті, зат беліп шығарған іэлектроңнын энергиясы тұрақты емес, ол нольден бастап ; белгілі бір жоғары шамаға дейін езгеріп отырады. Бұл құбылыс энергия сақталу заңына қайшы келетін тәрізді. Үшіншіден, неге кейбір ядро - электрон, екіншілері по-знтрон бөліп шығарады, ал үшіншілері электронды тартып алады?
Бұл жерде неміс физигі В. Паули болжап айтқан нейтрон бөлшегінің бета-активтік процесіндегі роліне тоқталу керек. Нейтрино дегеніміз - электр заряды жоқ, нейтраль әрі тыныштық массасы болмайтын бөлшек, реитрино жайлы ұғым арқылы радиоактивтік ыдырау кезінде бөлініп шығатын бета-бөлшектері энергиясының неге тұрақсыз болатындығына түсінік берілді. Оның қысқаша мазмұны мынадай: ядродағы протондар мен нейтрон бөлшектерінің ішкі құрлысы күрделі, сондықтан олар бір біріне яғни протон нейтронға (немесе керісінше) айнала алады. Сонда оң зарядты бета-бөлшегі (пазитрон) бөлініп шығады. Нейтрон мен протонның бір-біріне айналуы кезінде бұл аталған бөлшектермен қоса нейтронно пен антинейтронно бөлшектері түзіледі. Бета-ыдырау кезінде бөлінетін энергия ос бөлшектердің арасында таралады.
Енді ядродағы протонның нейронға айналуын былай жазуға болады:

Ал кері процесті, яғни нейронның протонға айналуын былайша жазамыз:

Мұндағы V - нейтринно -антинейтрино.
Электрондық қармап алудың механизмі былай өрнектеледі:
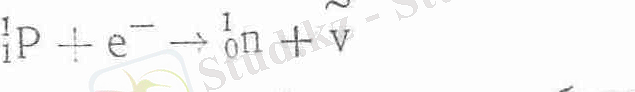
Әр түрлі изотоптардың түрліше жолмен бета-активті ыдырауы атом ядросының құрамына байланысты болады. Ядроның протондар тұрақтылығы оны құрайтын протондар мен нейтрондардың ара қатынасына тәуелді. Ол шама ядро нейтрондардың ара қатынасына тәуелді. Ол шама ядро нейтрондарының санын протондардың санына яғни элементтің реттік номеріне бөлгеннен шығатын санмен өрнектеледі. Элементтің реттік номері, яғни массасы артқан сайын ядроағы нейтрондар көбейе түседі. Ядролары тұрақты элементтердегі ядро заряды Z мен оның массалық саны А арасындағы байланыс мына қаарпайым формуламен белгіленеді.
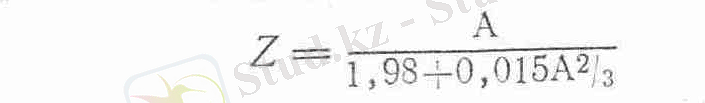
Осы формулаға сәйкес келетін протондар мен нейтрондардың ара қатынасы бұзылған ядролар тұрақсыз яғни радиоактивті болады. Ондай ядролар радиоактивтік ыдырау арқылы тұрақты ядроға айналуға бейім тұрады.
Егер ядрода нейтрондар саны артық болса, ол электрон бөліп шығарып, айналады. Керісінше, ядрода протондар артық болса, ол позитрон бөліп шығарып, нйетронға айналады. Альфа-бөлшектеріне қарағанда бета-сәулелерінің иондандыру қасиеті әлдеқайда төмен: энергиясы 1 мэв (миллион электрон вольт ) бета бөлшегі ауадағы 1 см жолында 53 жұп ион түзеді. Оның есесіне бұл бөлшектердің жүру жолы едәуір үлкен: ол ауада бірнеше ондаған метрге, ал тығыз заттарда милиметрдің бірнеше үлгісіне жетеді. Сондай-ақ бета-бөлшектерінің өткіштік қасиеті де едәуір жоғары. Мысалы, энергиясы 2, 5 Мэв бета-сәулесі қалыңдығы 1, 5 мм темір немесе мың қабатынан, қалыңдығы 4, 5 мм алюминий қабатынан өтіп кетеді.
Альфа-және бета-бөлшектерінің бөлінуін кейде альфа-және бета-сәле шығару деп те атайды. Шынына, бұлар сәуле емес, материалдық бөлшектер ағыны болып табылады.
Ал гамма -сәулелер олай емес. Олардың рентген сәулелерімен ұқсастығы көп. Екеуі де электромагниттік сәулелерге жатады. Тек гамма-сәулелер толқындарының ұзындығы өте кішкентай. Әзір толқындары гамма-сәулелеріне қарағанда қысқа келетін сәулелер табылған жоқ.
Дәріс 4.
РАДИОМЕТРИЯ, ДОЗИМЕТРИЯ ТУРАЛЫ ТҮСІНІК.
- Радиометриялық, дозиметриялық аспаптарды жіктеу құрылысы және қолданылуы.
- Радиоактивтілікті өлшеудің негізгі әдістері: салыстырмалы, абсолютті және есептеу
- Сәуле мөлшері, оның түрі мен қуаты.
Иондаушы сәулелердің қарқындылығы. Ионды сәуле тасқынының тығыздығы 1 сек. Ішінде 1 м2 түскен квантпен есептелінеді. Мысалы: в-бөлшегі , V - квант, в-бөлшегі ', V -квант .
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz