Су буының құрғақ, ылғалды және аса ысытылған күйлерінің термодинамикалық параметрлері және есептеу әдістері


Құрғақ қаныққан бу.
Құрғақ қаныққан будың күйі оның қысымымен және теппературасымен анықталады. XIII және XV кестелер бойынша будың қысымын (және барлық басқа параметрлерін) температура арқылы анықтауға болады. Ал XIII және XVI кестелер
47 сурет 48 сурет
бойынша - будың температурасын (және оның басқа барлық параметрлерін) қысым арқылы анықтауға болады. Су буы үшін P=f (tv), υ”= f (p) және тәуелділіктері 47 және 48 суреттерде келтірілген.
Ылғалды қаныққан бу.
Ылғалды қаныққан будың күйі оның қысымымен немесе температурасымен және құрғақтық дәрежесімен х анықталады.
Х=0 мәні судың қайнау кезіндегі күйіне сәйкес ал Х= 0 - құрғақ қаныққан буға сәйкес екендігі айқын (анық)
Ылғалды будың температурасы тек қысымның ғана функциясы және құрғақ будың температурасын анықтағандай XIII және XV кестелерден анықталады. ылғалды будың меншікті көлемі қысым мен құрғақтық дәрежесіне тәуелді және төмендегі теңдеуі бойынша анықталады.
υ х = υ х n + (1-x) υ 1 (7. 1)
Бұл теңдеуден х мәнін аламыз:
X=
(7. 2)
30 барға дейінгі қысымдар үшін және кезде 71 теңдіктің соңғы мүшесін ескермеуге болады. Сонда ылғал қаныққан будың меншікті көлемі төмендегіше жазады.
Vx =
 (7. 3)
(7. 3)
Үлкен қысымдар және аз х мәндері үшін (71) теңдеуді пайдалану керек.
Ылғалды будың тығыздығы келесі теңдіктен анықталады.
 ρ
x
=
ρ
x
=
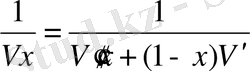 (7. 4)
(7. 4)
немесе жуық түрде ρ
x
=
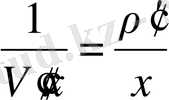 (7. 5)
(7. 5)
Аса ысытылған бу.
Құрғақ қаныққан будың температурсымен t салыстырғанда, сол қысымдағы аса ысытылған будың температурасы t жоғары болады.
Сәйкесінше белгілі қысымдағы аса ысытылған будың қаныққан будан өзгешелігі - оның әр түрлі температураға ие болу мүмкіндігі.
Аса ысытылған будың күйін сипаттау үшін оның екі параметрін білу керек. Мысалы: қысым мент температураны. Бірдей қысымдардағы аса ысытылған бумен қаныққан будың температураларының айырмасы будың тым ысытылуы деп аталады .
Жылутехникалық есептеулерде бу түзілу процесінің жекелеген сатыларына жұмсалған жылу мөлшері мен ішкі энергия өзгерісін анықтау өте маңызды болып табылады.
Қысым тұрақты кезде сұйықтықты 0 0 С -тан қайнау температурсына дейін қыздыруға жұмсалған жылудың мөлшерін сұйықтық жылуы деп атайды.
Оның қайнау күйіндегі сұйықтықтың энтальпиясының айырмасы мен анықтауға болады. Яғни
q p = Һ 2 - Һ 1 = Һ 1 -Һ 0 1 (7. 6)
Жоғары емес қысымды Һ 0 1 -ді техникалық есептеулер үшін жетерліктегі дәрежеде нольге тең деп санауға болады онда
q p =Һ 0 1 (7. 7)
Сұйықтықтың ішкі энергиясының мәнін жалпы тәуелділіктен есептеуге болады.
Һ = U+ ρV (7. 8)
Сонда
U 1 = Һ 1 - ρV 1 (7. 9)
ρV 1 шамасы аз болғандықтан жоғары емес қысымдарды төмендегідей қабылдауға болады.
U 1 = Һ 1 (7. 10)
Яғни сұйықтық ішкі энергиясы, сұйықтықтың энталпиясына тең А мәні оған сәйкес и мәніде қаныққан бу кестелерінде келтіріледі.
Тұрақты қысымда, 1 кг қайнайтын сұйықтықты құрғақ қаныққан буға өткізу үшін қажетті жылудың мөлшерін бу түзілу жылуы деп атайды және r әріпімен белгілейді.
Бұл жылу мөлшері ұлғаю жұмысы (ψ) мен сұйықтықтың молекулаларының арасындағы ілінісу көштерін d жеңумен байланысқан ішкі энергияның өзгерісіне шығындалады.
d шамасын бу түзілудің ішкі жылжуы деп атайды, ал шамасы - бу түзілудің сыртқы жылуы деп аталады.
Ψ= Р (
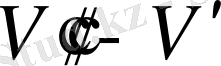 ) (7. 11)
) (7. 11)
және
r = d+ Ψ (7. 12)
екендігі анық.
r мәндері қаныққан будың кестелерінде келтіріледі.
Құрғақ қаныққан будың энтальпиясы Һn келесі теңдеу бойынша анықталады.
h
11
= h
1
+r (7. 13)
1кг сұйықтық кезде, құрғақ қаныққан будың алынуы кезіндегі ішкі энергия өзгерісі - келесі өрнектен анықталады.
u 11 = h 11 - PV 11 (7. 14)
Ылғалды қаныққан бу үшін келесі байланыстарды аламыз:
hx =h 1 +rx (7. 15)
және
ux=hx-PVx (7. 16)
мұндағы Һх - ылғалды қаныққан будың энталопиясы
ux- ылғалды қаныққан будың ішкі энергиясы.
Тұрақты қысым кезінде 1кг құрғақ қаныққан буды аса ысытылған буға өткізу үшін қажетті жылу мөлшерін аса ысытылу жылу деп атайды.
q
n
=
 th
t
Cp dt (7. 17)
th
t
Cp dt (7. 17)
мұндағы, Ср - тұрақты қысымдағы аса ысытылған будың нақты массалық жылушымдылығы. мұхият зеттеулердің нәтижесінде, аса ысытылған булардың жылу сиымдылықтары Ср температурамен қысымға тәуелді екендігі анықталған және аналитикалық тәуелділік табылған
Cp = f (P, t) (7. 18)
Бірақ бұл тәуелділіктің күнделігі мен рабайсыздығы салдарынан, оны пайдалану қолайсыз. Су буының кестелеріне аса ысытылған будың энтальпиясының һ мәндері келтіруі себепті есептеулер елеулі жеңілдейді (XIV және XVII кестелерді қара ) Сондықтан аса ысытылу жылуы келесі өрнектен анықталады.
q n = h-h 11 (7. 19)
Будың энтрoпиясы.
Су буының энторпиясын шартты нольден бастап есептейді.
Шартты ноль ретінде судың 0, 01 С - тағы және қанығу судың қысымындағы және температурадағы сәйкес келетін қысымдағы 0, 006108 бар (0, 006228 ат ) энтрoпиясы қабылданады
Сұйықтықтың энтрoпиясы S 1
S
1
= c ln
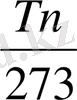 (7. 20)
(7. 20)
өрнегімен анықталады.
мұндағы, с- судың жылу сиымдылығы
Тқ - қанығу температурасы К
Су үшін жылу сиымдылықтың мәнін едәуір дәлдәкпен 4, 19 (кг град) деп санауға болады. сәйкесінше,
S
1
=ln
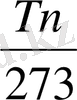 ккал (кг, град) (7. 21)
ккал (кг, град) (7. 21)
Немесе
S
1
=4, 19 ln
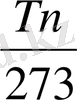 кдж (кг, град) (7. 22)
кдж (кг, град) (7. 22)
Егер сұйықтықты қыздыру қайнау температурасына дейін немесе еркін алынған Т дейін жүргізілсе онда (722) теңдеудегі Тқ орнына осы еркін температураны қою қажет.
Құрғақ қаныққан будың энторпиясы S төмендегі теңдеуден анықталады
S
11
=S
1
+
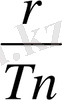 . (7. 23)
. (7. 23)
Мұндағы r - бу түзілу жылуы.
Ылғал қаныққан будың энторпиясы
Sx
0
= S
1
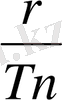 x (7. 24)
x (7. 24)
Немесе 724 теңдеуді негізге алып,
Sx = S 1 + (S 11 -S 1 ) х (7. 25)
Мұндағы х- будың құрғақтық дәрежесі.
S
1
және S
11
энтропияларының мәндері қаныққан бу кестелерінде келтірілген
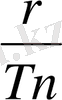 мәндерін осы кестелерден S
11
S
1
айырмасы ретінде алуға болады.
мәндерін осы кестелерден S
11
S
1
айырмасы ретінде алуға болады.
Аса ысытылған будың энтропиясы келесі теңдеуден анықталуы мүмкін .
S = S
11
+
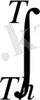 Cp
Cp
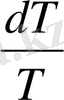 (7. 26)
(7. 26)
S мәндері аса ысытылған будың кестелерінде келтіріледі (XIV және
XVIIкестелерді қараңыздар)
Берілген параметрлерден буының күйін анықтау кезінде, төмендігілерді негізге алу керек:
Аса ысытылған және құрғақ қаныққан бу үшін бірдей қысымды
V>V 11 және P>Pn
Аса ысытылған және құрғақ қаныққан будың температуралары бірдей кезде
V>V 11 және P>Pn
Су буының кестесінің көмегімен және осы байланыстардың көмегімен бу күйін анықтау оңай.
7. 1есеп.
Қаныққан құрғақ будың Р= 10 бар қысымдағы температурасын, меншікті көлемін тығыздығын энтальпиясын және энтропиясын және энторпиясын анықтау керек.
Шешуі:
XIII кестеден табатынымыз: tn = 179, 88 0 C V 11 = 0, 1946 м 3 /кг;
Ρ 11 =5, 139 м 3 /кг, Һ 11 = 2778 кдж/кг; S 11 = 6, 587 кдж//кг град/
7. 2 есеп.
Құрғақ қаныққан бу Р = 14 бар қысымға ие . Будың қалған барлық параметрлерін анықтау керек.
Жауабы:
tn - 195, 04 0 С; V 11 = 0, 1408м 3 / кг
Ρ 11 = 7, 103 м 3 /кг, Һ 11 = 2790 кдж/кг;
U 11 = 2593 кдж/кг; S 11 = 6, 469 кдж//кг град/
7. 3есеп 15 бар қысым болғандағы су 190 С - қа дейін қыздырылды. Қайнау болдыма ?
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz