Жылутехника мен техникалық термодинамика: мұнай саласындағы рөлі, идеал газдар және термодинамиканың бірінші заңы


Дәріс №№1-2 Тақырыбы: Кіріспе. Жылу қондырғылары және олардың
еліміздің мұнай саласындағы ролі.
«Жылутехника» пәні және оның мұнай және газ
бакалаврларын дайындаудағы орны мен ролі.
Дәрістің мақсаты: Студеттерге энергияның халық шаруашылығындағы ерекше ролін және Республикадағы жағармайлық теңдіктің өзгеру бағыттары жөнінен хабардар ету.
Дәрістің жоспары :
1. Жылу қондырғылары.
2. Жылутехника пәні
3. Жылу жүйесіндегі факторлар
Жылу қондырғылары. Жылутехника (термодинамика) пәні.
Жылу құбылыстарын, жылу алу жолдарын, оның өзгерісін, жылу алмасуын, қолданылуын және оның іс - әрекеті мен құрылымдық ерекшеліктеріне байланысты жылу және бугенераторларын, жылу машиналарын, аппараттар мен қондырғыларды зерттейтін ғылым - жылутехника деп аталады. Жылутехника ғылымын дамытуда көп еңбек сіңірген орыстың ғалымдары мен инженерлері. Осы салада алғаш рет өзінің ғылыми жұмыстарын ұсынған орыстың ғұлама ғалымы - М. В. Ломоносов болды. Ол теориялық зерттеулері мен экспериментальдық жұмыстарының нәтижесінде заттың молекула - кинетикалық теориясының негіздерін, молекула арасындағы жылулық және механикалық энергияның сақталу және өзгеру заңдылықтарының бір бөлігі деп түсінген.
Д. И. Менделеев өзінің осы салада терең жұмыстар жүргізуінің арқасында, ғылымға алғаш рет жер асты жағармайдың газдандырылуына байланысты туатын сұрақтарды ашық талқыға салды. Сонымен қатар, ол әр заттың белгілі бір кризистік температурасы болатынын, одан әрі бұл зат қандай да болмасын жоғары қысымда да сұйыққа айнала алмайтындығын дәлелдеп, кризистік температура таблицасын құрастырады.
К. Е. Циолковский, К. В. Кирш, А. А. Радцг, В. И. Гриневецкий және тағы да басқа орыс инженерлері мен ғалымдарының еңбектерінің арқасында 19 ғасырдың аяғымен 20 ғасырдың басында жылу агрегаттарының ғылыми жобалары жасақталды (пештер, жылу двигательдері, ракеталар және т. б. ) .
Жылудың рационалды түрде толық пайдаланылуы үшін, жылу қондырғылардағы процестердің жұмысын анализ арқылы үнемдеп, мейлінше ұтымды ауыстырып және жаңасын тауып, теплотехниканың теориялық негізін тереңдеп дамыту керек. Мұнсыз, қуатты бу және газ турбиналарын жасап шығаруға, реактивті двигательдерді, континет аралық аса дәл ракеталарды және т. б. күрделі жылулық қондырғыларды ойлап табу мүмкін емес.
Жылудың принципті түрде 2 бағытта қолданылатынын естен шығармаған абзал.
- Энергетикалық;
- Техникалық;
Жылуды энергетикалық бағытта қолданған кезде, ол механикалық жұмысқа айналады. Егер, жылуды техникалық ортада қолданатын болсақ, ол әр түрлі заттардың қасиеттерін өзгерту үшін қолданылатынын көреміз. Мысалы: дененің температурасын өзгерту арқылы, оларды балқытуға, қатайтуға, құрылысын өзгеруіге, механикалық, химиялық, физикалық қасиеттерін өзгертуге болады.
Қазіргі энергетикалық салалардың басты жұмыс бағдары, жылудың механикалық жұмысқа толық трансформациялануы. Осының салдарынан генераторда алыс жолға тасымалдауға қолайлы энергия пайда болады. Реакцияға қажетті жылуды - жағармайды пештерде немесе іштен жану двигательдерінде жағу арқылы өндіреді.
Құрылыс индрустриясында құрал-жабдықтарды өндіру кезінде техникалық жылулық принцип қолданылады. Бірақ, жұмыста қолданылған бужасағыш, кептіргіш, жанғыш қондырылар толығымен термодинамика заңдарына сәйкес анықталады.
Жылу жүйесіндегі факторлар.
Сонымен қатар, жылуды пайдалана отырып, жылу жүйесін үнемді қолдану проблемасы туындайды, ол өз кезегінде, жағармай үнемділігін қажет етеді, Ж. Э. Р. 2 фактор бойынша реттеледі.
- Экономикалық фактор;
- Экологиялық фактор;
Экономикалық фактор.
Экономикалық фактор әлемде болып жатқан жағдайларға және дүние жүзіндегі жағармайдың қымбаттауына байланысты, меншікті шығынның көлемін азайтуды және жағармай өндіру дәрежесін арттыруды талап етіп отыр.
Көптеген технологиялық процестердің энергетикалық нәтижелігі өте нашар. Мысалы: біздің елде 1 т. цемент өндіру үшін жұмсалатын меншікті жылу мөлшері 210 кг/т, ал осы кезде энергияны үнемдейтін технологиялардың нәтижесінде АҚШ-тағы өндірісте жұмсалатын жылу мөлшерінің көрсеткіші 150 кг/т, ал Японияда бұл көрсеткіш тіпті төмен 110 кг/т болып келеді.
Қазіргі таңда қаражатты жағармай өнімділігін арттыру үшін салған тиімсіз, оданда жағармайды пайдалану (жұмсау) дәрежесін азайтуға, технологиялық процестердегі отынды тиімді үнемдей отырып пайдалануға ат салысқан жөн. Қазіргі кезде, энергетикалық - жағармай өндірісін дамытуға әлемнің 23 елі қаражат құяды. 1985 жылға шейін еліміздің жағармайлық теңдікте - мұнай мен газдың ролі өсті. 1985 жылдан бастап мұнай мен газ өндіру тұрақталды. Енді мұнайды тереңірек өңдеу салдарынан мазут пен пештік жанармайдың көлемі азаяды да моторлық жанармайдың көлемі артады.
Егер 1983 жылы еліміздің электр станцияларында мазуттың максимальды көрсеткіш - 120 млн. т., жұмсалса, соңғы жылдары мазуттың энергетика саласында пайдалану көрсеткіші күрт төмендеді. Ірі энергетикалық компаниялар, қазір қатты отын түрлерін және табиғи газды пайдалануға құлшыныс танытып жатыр. Осыған орай мұнай мен газ өндіру дәрежесі алдағы уақытта артпаса, азаятыны екі талай.
Экологиялық фактор.
Алдағы уақытта өтетініміздей, жағармайды жағу кезінде шығатын өнімнің бірі көмірсутек диоксиді - Co 2 . Бұл газ, жердің атмосферасының құрамында кездеседі. Ол жерді салқындатуға, космосқа саулелену арқылы кері әсерін тигізеді. Соңғы жылдары бүкіл елдің ғалымдары атмосферадағы көмірсутек диоксидінің концентрациясы көбейіп кетті деп дабыл қағуда. Егер бұл жорамал расталса, адамзатқа алдағы уақытта құрамында көмірсутек диоксиді бар жанармайды қолданудан бас тартуымыз қажет.
Сонымен қатар, жылу-электр және жағармай жағу қондырғылары бөлетін қалдықтар жергілікті экологияны ластап, (ақаба сулар мен газдар) химиялық (күкірт оксиді мен азот) күл мен түтін бөледі, олардың мөлшері өнеркәсіптің өнімділігі артқан сайын өсіп, күрделі қиындықтарды тудырып отыр. Бұл қалдықтарды түбегейлі жоюға немесе атмосфераға тарайтын зиянды заттардың санын мейлінше азайту үшін ең алдымен жағармай қолданатын қондырғылардың жұмысын, ондағы ағып жатқан процестерді тереңірек зерттеу керек. Нақты айтқанда қазір, экология, адамзатты толығымен қалдықсыз технология өндірісін пайдалануға мәжбірлеп отыр.
Негізі адамзаттың пайдаланып отырған пайдалы қазбаларының 90 % органикалық отын көзі болып табылады. Бұл теплотехника ролін анықтайды - жалпы инженерлік мамандықта, жылу құбылыстарын, жылу алу жолдарын, оның өзгерісін, жылу алмасуын, қолданылуын және осыған сәйкес аппараттардың жұмысын зерттейді.
Теплотехниканың теориялық бөлімі - жағармайлық энергияның қасиетін, температураның таралу процесін және өзгеру заңдылықтарын зерттейтін бөлімдерге бөлінеді:
1) Техникалық термодинамика
2) Жылу алмасу теориясы
Студенттердің өзін-өзі бақылауға арналған сұрақтар:
- Энергия мен жылу техникасының халық шаруашылығындағы орны?
- «Жылутехника» нені зерттейді?
- Орыс және кеңес одағы ғалымдарының жылу техника мен энергетика
саласына қосқан үлесі қандай?
- Жағармайлық тепе-теңдік неге және қалай өзгереді?
- Энергетикалық және техникалық жылу дегеніміз не?
- Халық шаруашылығында жылуды қайда қолданылатынын атап өтіңіз?
Әдебиеттер: [2] §1; 4-6 беттер;
[3] §14-5 беттер.
Дәріс №№ 3-4 Тақырыбы: Техникалық термодинамика.
Мінсіз(идеал) газдар және олардың қоспалары
Дәрістің мақсаты : Анықтамалар кешенімен студенттерді таныстыру және техникалық термодинамика ұғымдарының, базадағы келесі тақырыптарды таныстырып, олардың ұғымдарды айқын меңгеруіне көз жеткізу.
Дәрістің жоспары:
1. Техникалық термодинамика пәні.
2. Термодинамикалық жүйе.
3. Термодинамикалық күй көрсеткіштерінің негізгі теңдеуі.
4. Күй көрсеткішінің теңдігі.
5. Термодинамикалық процесс.
Техникалық термодинамика пәні.
Термодинамика - әр түрлі энергияның бір-біріне айналу процесстерін зерттейтін ғылым. Бұл ғылым табиғат құбылыстарының сан алуандығын, ондағы химиялық, механикалық, физико-химиялық құбылыстарын зерттейді. термодинамиканың үш бөлімінің бірін техникалық термодинамика деп атайды, ол жылудың толықтай жұмысқа айналу заңдылықтарын қарастырады.
Басқаша айтқанда, техникалық термодинамика жылулық және механикалық энергияның айналу заңдылықтарын, айналу процессіне қатысатын денелердің қасиетін зерттейді. Ол жылулық, механикалық және химиялық процестердің арасында өзара байланыс орнатады, бұл байланыс жылулық және салқындатқыш қондырғыларда іске асады. Сонымен қатар газдар мен буларда жүретін процесстерді, ондағы денелердің қасиетін әр түрлі физикалық ортада зертейді.
Жылуалмасу мен техникалық термодинамикалардың теориясы жылу-техникасының басты іргетасы болып табылады. Осының негізінде есептеулер және барлық жылу қозғалтқыштардың жобалауын жүдзеге асырады, сонымен қатар технологиялық жабдықтау да жоспарлайды.
Термодинамика пәні негізгі екі заңға сүйене отырып жасақталған.
Термодинамиканың бірінші заңы - табиғат заңдылықтарына байланысты жылулық құбылыстарына негізделген - энергияның өзгеру мен сақталу заңын ұсынады.
Термодинамиканың екінші заңы жүйедегі макроскопиялық денелердің ағып өтуін және процестердің бағыттарының алғы шарттарын зерттейді.
Термодинамикада зерттеудің екі әдісі қолданылады.
- Тұйық (айналмалы) процесстік әдіс;
- Термодинамикалық функциялар мен геометриялық құраушылардың әдісі болып бөлінеді.
Термодинамикалық жүйе
Барлық табиғат құбылыстарына бір-бірімен өзара байланысқан бір немесе бірнеше денелер жиынтығы қатысады. Термодинамикалық құбылыстарды зерттеу кезінде тәжірбие обьектісі ретінде бір немесе бірнеше дене, кей жағдайда сол дененің бір бөлшегі ғана алынады. Зерттелу обьектісі - термодинамикалық жүйе, ал оның шекарасында жатқан денелер - қоршаған орта деп аталады.
Термодинамикалық жүйе деп - макроскопиялық денелер жиынтығынан тұратын, өзара бір-бірімен және қоршаған ортамен энергия алмасатын жүйені айтады.
Жүйе мен қоршаған ортаны айырып тұратын бақылау қабықшасы (бақылау беті) .
Термодинамикалық жүйенің ең қарапайым түрі ретінде цилиндрде піспектің астында сығылған газды алуға болады. Мұндағы қоршаған ортаның рөлін - қоршап тұрған кәдімгі ауа, ал бақылау қабықшасы ретінде цилиндрдің қабырғалары мен поршень алынады.
Егер термодинамикалық жүйенің қоршаған ортамен еш байланысы болмаса, ондай жүйені жылу оқшауланған жүйе деп атайды. Бірақ, жүйе қоршаған ортамен затпен де, энергиямен де алмаспайды.
Адиабаттық қабықшамен қоршалған, қоршаған ортамен жылу алмасу процессін мүлдем өткізбейтін жүйені жылу оқшауланған немесе адиабаттық жүйе деп атайды. Бұған мысал ретінде, қабырғалары жылу алмасудан мықтап оқшауланған, қоршаған ортамен жылу алмаспайтын шыны ішіндегі газды алынады.
Термодинамикалық жүйедегі механикалық және жылу алмасу процесстері бақылау қабықшасы арқылы жүзеге асады. Механикалық әрекеттесу кезінде жүйенің өзімен немесе жүйенің үстінен жұмыс жасалады. Біздің қарапайым мысалымыздың негізінде механикалық жұмыс поршеннің орын ауыстыруымен, көлемінің өзгеруімен жалғасады.
Жылу алмасу негіздері жылудың бөлек бөлшектердің арасында орын ауыстыру мен жылу жүйесімен және қоршаған ортамен әрекеттесуіне байланысты. Қарастырылып отырған мысалда жылу газдан цилиндрдің қабырғалары арқылы алынады. Жалпы жағдайда жүйе ортамен және затпен алмаса алады (масса алмасу әрекетті) . Мұндай жүйе - ашық жүйе деп аталады. Турбиналар мен құбырлардағы газ бен будың ағындары - ашық жүйенің негізі болып табылады.
Ал, келешекте біз жабық жүйені қарастырамыз. Жұмыс денесі қарапайым термодинамикалық жүйе болып табылады, ол жылудың жұмысқа айналуын жүзеге асырады. Іштен жанатын двигательдерде (ІЖД) мысалы, жұмыс денесі ретінде құрамында ауа мен бензин буы бар карбюратордағы жанғыш қоспа алынады.
Термодинамикалық жүйедегі негізгі күй көрсеткіштері.
Техникалық термодинамика пәні жылу машиналарындағы процестердің жылу мен жұмыстың өзара өзгеру әрекетін зерттейді. Жылу машиналарында жылудың жұмысқа айналу процессі жұмыс денесінің негізінде жүздеге асады.
Мысалы: ІЖД, ГТҚ қондырғыларында қарастырылған процестерде жұмыс денесі ретінде газ алынған. Парлы двигательдерде жұмыс денесі - су буы болып табылады.
Жұмыс денесінің физикалық жағдайы (немесе термодинамикалық жүйеде) бірнеше өлшем бірліктермен анықталып, оның күй жағдайын, термодинамикалық күй жағдайын анықтайды. Біркелкі дененің күй жағдайы негізгі үш параметр бойынша анықталады:
υ - меншікті көлем;
Р - қысым;
Т - температура.
Меншікті көлем - біркелкі зат - өлшем, көлем мен массаның қатынасына тең.
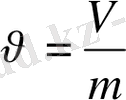 (1)
(1)
Мұндағы: v - заттың меншікті көлемі; м 3 /кг;
V - белгілі бір заттың көлемі; м 3 ;
m - сол заттың массасы; кг;
Меншікті көлемге қарама - қарсы өлшем заттың тығыздығы деп аталады да, ол мына қатынаспен анықталады
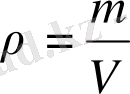 (2)
(2)
Мұндығы: р - заттың тығыздығы; кг/м 3 ;
V - көлем; м 3
m - масса; кг;
Қысым.
Молекула кинетикалық теорияның негізінде қысым газ молекулаларының орташа соққысының салдарынан пайда болып, үздіксіз қозғалысының нәтижесінде шыны ыдыстың бойында тұрған газ ыдыстың қабырғасына соғып, күштің ауданға қатынасын көрсетеді.
Р=
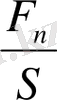 (3)
(3)
Мұндағы: P - қысым, Па;
F - күш, Н;
S - ауданы, м 2 ;
Халықаралық (СИ) жүйесіндегі өлшем бірлік бойынша қысым Паскальмен өрнектелінеді. Бұл өлшем бірлік аз болғандықтан
1кПа =10 3 Па және 1 МПа = 10 6 Па қолданған тиімдірек.
Көбінесе қысым бармен өлшенеді (СИ жүйесінен бөлек) 1бар=10 5 Па. Әдетте қысым Паскальмен өлшенетінін естен шығармаған абзал. Қысымды барометр, манометр, вакуумметр аспаптары аққылы өлшейді. Манометр артықтық қысымды өлшейді Р арт .
Термодинамикалық параметрлердің бірі - абсолюттік қысым мынаған тең.
Р = Р арт + Р атм (4)
Мұндағы: Р атм - атмосфералық қысым, барометрмен өлшенеді.
Атмосфералық қысымнан төмен қысым вакуумдық қысым деп аталады, ол вакуумметрмен өлшенеді.
Егер ыдыста вакуум болса, онда абсолюттік қысым мынаған тең.
Р=Р атм -Р вак (5)
Температура - дененің қызу дәрежесін көрсететін физикалық шама.
Ол жылулық тепе-теңдіктегі изоляцияланған жүйенің молекулаларының жылулық қозғалысының интенсивтілігін сипаттайтын және молекулалардың іргерлемелі қозғалысының орташа кинетикалық энергиясына тура пропорционал скаляр шаманы айтамыз.
Егер орташа кинетикалық энергиясы әр түрлі екі дененің молекулалық қозғалысын әкеліп әрекеттестірсек, онда орташа кинетикалық молекуласының энергиясы үлкен дене (үлкен температурамен) өзінің бойындағы энергияны орташа кинетикалық молекулалық энергиясы аз денеге береді (аз температурамен) және бұл процесс екі дененің орташа кинетикалық энергиясы теңеспегенше, яғни олардың температулары бір - біріне сай болмағанша жүре береді. Екі дененің бұл жағдайы жылулық тепе - теңдік деп аталады.
Халықаралық (СИ) жүйесіндегі өлшем бірлік бойынша температура кельвинмен (К) өлшенеді. Практикада көбіне градус Цельсия ( 0 С) қолданылады. Абсолют температура мен температураның арасындағы қарым - қатынас, Цельсия ( 0 С) градус мынадай түрде өрнектеледі.
Т = t + 273, 15;
Өндірісте және лабораторияларда температураны сұйықтық термометрдің, пирометрдің, термопардың және де басқа да құралдардың көмегімен өлшейді.
Күй теңдеуі.
Егер термодинамикалық күй көрсеткіштері уақыт өте келе тұрақты бастапқы қалпында сақталатын болса, онда мұндай жүйені бірқалыпты деп атайды.
Егер жүйедегі параметрлер әр түрлі нүктеде t, Р әр түрлі болса, онда мұндай жүйені бірқалыпсыз деп аталады.
Бірқалыпты термодинамикалық жүйеде параметрлі күй көрсеткіштерінің арасында функцианальдық байланыс болады, ол күй теңдеуі деп аталады.
Тәжірбиелер көрсеткендей, қарапайым жүйедегі негізгі күй көрсеткіштердің (Р,
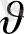 , T), немесе біркелкі дененің жағдайы бір біріне байланысты және олар бір матаматикалық теңдікпен өзара байланған f(Р, v, T) = 0
, T), немесе біркелкі дененің жағдайы бір біріне байланысты және олар бір матаматикалық теңдікпен өзара байланған f(Р, v, T) = 0
Күй теңдеуін басқа түрге келтіруге болады.
Р= f
(
, Т) ;
= f
(Р, Т) ; Т= f
(Р,
) .
Бұл теңдеу, жүйенің күй жағдайын анықтаушы негізгі үш параметрдің тек қана екеуі ғана тәуелсіз болып келетінін көрсетті. Тапсырманы термодинамикалық әдіспен шешу үшін, күй теңдеуін дырыс меңгеру керек.
Идеал газ деп газ молекулаларының материалдық нүкте ретінде қарастыруға болатын және олардың бір - бірімен әсерлесуі жоқ, тек қана серпімді соқтығысумен әсерлесетін, малекуларының көлемі газдың көлемін бірнеше есе кіші болып келетін газды айтамыз. Нақты газдардың көпшілігі жоғары температурада және төменгі қысымда идеал газдармен қасиеті жағынан шамалас болып келеді. 1 кг идеал газ үшін күй теңдеуі мынадай математикалық өрнекпен өрнектеледі.
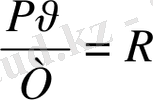 немесе
немесе
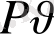 =
RT
(6) Мұндағы : тұрақты бірлікті - газ тұрақтысы деп атайды. Өлшем бірлігі
- Дж/кг* К;
=
RT
(6) Мұндағы : тұрақты бірлікті - газ тұрақтысы деп атайды. Өлшем бірлігі
- Дж/кг* К;
Бұл теңдеу - идеал газдың термиялық күй теңдеу немесе сипаттайтын теңдеу деп атайды. Бұл теңдеуді француз ғалымы Клайперон 1834 жылы ашты, қазір бұл теңдеу сол ғалымның атымен аталады.
Газдың әр түрлі саны үшін массасы m (кг) (6) -шы теңдеу мына түрге келеді.
РV=mRТ (7)
Клайперон теңдеуін мынадай уневерсалды түрге келтіруге болады.
РV
=
(8)
Мұндағы: V- газдың киломольдік көлемі;
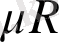 =
R
=
R
 - универсал газ тұрақтысы деп аталады. Авогадро заңының негізінде (итальян ғалымы 1811 ж. ) 1 кг газдың киломольдік көлемі әр түрлі жағдайларда, барлық идеал газ үшін, қалыпты физикалық жағдайда (қысым 101325 Па және температура 273, 15 К) тұрақты 22, 4136 м
3
болады, сондықтан:
- универсал газ тұрақтысы деп аталады. Авогадро заңының негізінде (итальян ғалымы 1811 ж. ) 1 кг газдың киломольдік көлемі әр түрлі жағдайларда, барлық идеал газ үшін, қалыпты физикалық жағдайда (қысым 101325 Па және температура 273, 15 К) тұрақты 22, 4136 м
3
болады, сондықтан:
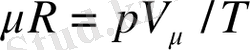 =101325*22, 4136/273, 15 = 8314 Дж/(кмоль·К)
=101325*22, 4136/273, 15 = 8314 Дж/(кмоль·К)
1 кг газ тұрақтысы мынаған тең.
R =8314/μ (9)
Термодинамикалық процесс.
Жоғырыда айтып кеткеніміздей, егер күй теңдеуі белгілі болса, онда қарапайым жүйедегі -уақыт өте келе мәндері тұрақты біркелкі болатын, массасын да, құрамын да негізгі үш параметрдің екеуі ғана белгілі болса, күй көрсеткіштерін анықтауға болады.
Р= f
(
, Т) ;
= f
(Р, Т) ; Т= f
(
, Р) .
Термодинамикалық жүйені қоршап тұрған сыртқы орта өзгеретін болса, онда жүйенің ішкі жағдайыда өзгереді.
Термодинамикалық жүйенің күй жағдайының бір тұрақты ортадан, екінші ортаға өзгеру жиынтығы - термодинамикалық процес деп аталады.
Немесе, термодинамикалық жүйенің уақыт өте келе өзгеру жағдайын - термодинамикалық жүйе деп атайды. Жүйенің өзгеру процессі бірқалыпты және бірқалыпсыз болып екіге бөлінеді. Егер термодинамикалық жүйе бірқалыпты күй көрсеткіштерімен өтіп жатса, онда мұндай жүйені бірқалыпты деп атайды. Қорыта келгенде, бірқалыпты процесс толассыз қатардағы жүйелілердің тепе-теңдік күй-жағдайы. Сондықтан термодинамикадық жүйедегі оның барлық нүктелерін оның жұмыс денесінің күй теңдеуі деп сипаттауға болады. Сондықтан классикалық термодинамикалық зеттеу негіздері бірқалыпты жүйеге сүйене отырып жасақталған.
Термодинамикалық жүйедегі бірқалыпты процесті график арқылы бейнелеуге болады. Техникалық термодинамикада бірқалыпты процесті бейнелеу үшін екі жүйелі координаталар қолданылады РV. Мұндағы абсциссаны меншікті көлем, ал ординатаны қысым өлшейді. Термодинамикалық жүйедегі, РV - координаталарында тұрақты көлемдігі процесс - изохора вертикальтүрінде, ал тұрақты қысымдағы процесс - изобара горизонталь түрінде, тұрақты температурадағы процесс - изотерма гипербола түрінде бейнеленеді ( 1-сурет) .
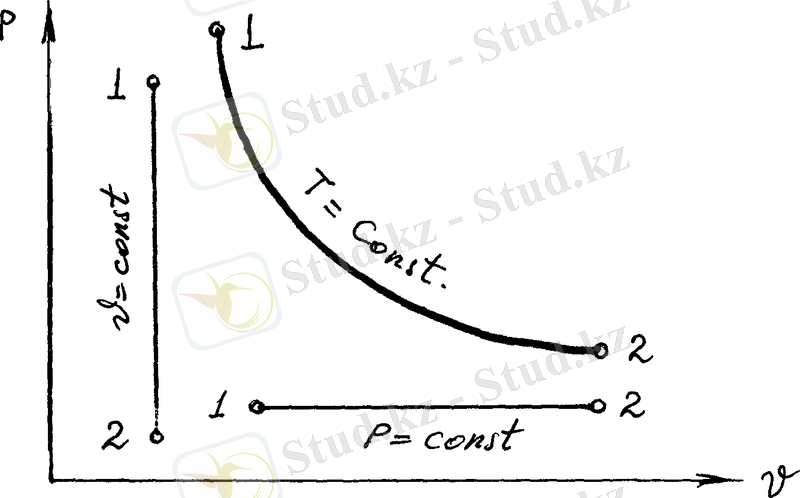
1 - сурет
Термодидинамикалық процестерді зерттеген кезде ерекше мағынаны - тұйық (айналмалы) процестерге көп көңіл бөледі. Бұл жағдай да жүйе бірнеше айналмалы әрекеттер қатарын жасап, бастапқы алғашқы күйіне (жағдайына) келеді.
Студенттердің өзін-өзі тексеруге арналған бақылау сұрақтары:
1. Термодинамикалық жүйе дегеніміз не?
2. Жұмыс денесі дегеніміз не?
3. Термодинамиканың негізгі параметрлерін және олардың өлшем бірліктерін атаңыз?
4. Қандай процесс термодинамикалық деп аталады?
5. Бірқалыпты және бірқалыпсыз жағдай мен процесс дегеніміз не?
6. Айнылмалы тұйық процесс дегеніміз не?
7. Идеал газ дегеніміз не?
8. Идеал газдың қандай күй теңдеулері бар?
Әдебиеттер: [2] §1. 1. 2. -1. 6. ; 6-14 беттер;
[3] §1 1. 2. -1. 6. ; 6-12 беттер;
Дәріс №№ 5-6. Тақырыбы: «Термодинамиканың бірінші заңы»
Дәрістің мақсаты: Студентерді ғылымның екі алғашқы бастамалары «Жылутехника» пәнімен таныстырып, жұмыс денесінің ішкі энергиясының жұмыс пен жылудан айырмашылығын анықтау.
Дәрістің жоспары:
1. Ішкі энергия;
2. Жұмыстың ұлғаюы;
3. Жылу;
4. Термодинамиканың бірінші заңының аналитикалық өрнегі.
Ішкі энергия.
Ішкі энергия деп, молекула мен атомдардың бей-берекетсіз қозғалысының салдарынан пайда болатын; өз бойына мынадай қасиеттерді қосатын:
─ Кинетикалық энергияның берілмелі, айнымалы және тербелмелі қозғалыстары;
─ Молекулалардың арасындағы күштің потенциалдық энергиясы.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz