Көмірсутектер: қаныққан, қанықпаған және ароматты қосылыстардың құрылымы мен химиялық қасиеттері


Жоспар:
1) Көмірсутектер
2) Қанықпаған көмірсутектер
3) Ароматты көмірсутектер
4) Қаныққан көмірсутектер
Пайдаланылған әдебиеттер
1) Көмірсутектер
Көмірсутектер - молекулалары көміртек пен сутек атомдарынан тұратын органикалық қосылыстар.
Құрамына байланысты көмірсутектер ациклды, алициклды және ароматты қосылыстарға бөлінеді. Химикалық қасиеттері мен құрылысы ұқсас, ал молекулалар құрамы бойынша айырмашылығы бір не бірнеше CH2 тобы болатын қосылыстарды гомологтар деп атайды, олар гомологтық қатар түзеді. Мысалы, қаныққан көмірсутектердің гомологтық қатары. Бұл қатардың бірінші мүшесі - метан, одан соңғылары - бір-бірінен айырмашылығы CH2 тобы болатын гомологтық қатар мүшелері. Қалыпты жағдайда 1-ден 4-ке дейін көміртек атомдары бар қаныққан көмірсутектер - газдар, 5-тен 17-ге дейін сұйықтар, ал көміртек атомдарының саны 17-ден көптері - қатты заттар. Көмірсутектердің көбі түссіз. Оның негізгі табиғи қоры - мұнай. Мұнай құрамында 23 - 63%-ға дейін парафиндер, 29, 72% шамасында нафтендер, 2 - 16%-ға дейін ароматты көмірсутектер болады. Төменгі алкандар (негізінен, метан) - метан, этан, пропан - табиғи газдар құрамында болады.
Көмірсутектер, негізінен, мұнай айдау процесі кезінде алынады, сондай-ақ көміртек оксиді мен сутекті катализатор қатысында қыздырғанда қалыпты парафиндер мен тармақталған парафиндер қоспасы түзіледі. Қаныққан көмірсутектер жанар май, жағар май алу үшін шикізат ретінде қолданылады. Кокстік химия өндірісінде алынатын ароматты көмірсутектер дәрі-дәрмек, хош иісті заттар алуда, ал қанықпаған көмірсутектер спирт, ацетон, жасанды каучук алуда пайдаланылады.
2) Қанықпаған көмірсутектер
Қанықпаған қосылыстар көмірсутектер арасында кең тараған, практикалық маңызы зор топты құрайды. Қаныққан көмірсутектер қатарының метаннан басталатыны тәрізді, қанықпаған көмірсутектері үлкен тобының қарапайым өкілі этилен болып табылады.
Этилен - ауадан біраз жеңілдеу, иісі жоққа тән, түссіз газ.
Оның молекулалық формуласын анықтап көрейік. Қалыпты жағдайдағы этиленнің тығыздығы - 1, 25 г/л. Демек газдың мольдік массасы 1, 25 г/л * 22, 4л/моль=28г/моль болады. Сонда бұдан этиленнің салыстырмалы молекулалық массасы - 28, сонда этиленнің формуласы - С 2 Н 4 болады.
Этилен молекуласы симметриалы болып келеді. Яғни мұндағы көміртегінің атомы әрбір атомы сутегінің екі атомынымен байланысады. Н 2 С=СН 2
Этиленнің молекуласында барлық атомдардың ядролары бір жазықтың бойында орналасып, молекуладағы валенттік бұрыш 109°28` болмай, 120° болатыны физикалық әдістерімен зерттеу арқылы анықтайды. Қанықпаған көмірсутектерде sp 2 - гибридтену, және П байланысы болады. Этилен - молекулаларында көміртегі атомдары арасында қос байланыс болатын заттардың гомологтық қатарындағы бірінші мүше. Этиленнің ең жақын гомологы: пропилен СН 2 = СН - СН 3 , бутилен СН 2 = СН - СН 2 - СН 3 . Этилен қатарындағы көмірсутектердің атауына -илен жұрнағы жалғанады. Қазіргі кезде мұндай номенклатура мен қатар, жүйелеу(халықаралық) номенклатурасы жиі қолданылады, ол номенклатура бойынша бұл көмірсутектер атауы -ен жұрнағымен аяқталады(этен, пропен, бутен, т. б. ) . Этилен қатарындағы көмірсутектердің жалпы формуласы - С n H 2n .
Этилен қатарындағы көмірсутектердің жеке атаулары былай құралады:
- құрылымдық формуладан қос байланысы бар көміртегі атомдарының ең ұзың тізбегін бөліп алады, оларды қос байланыс ең жақын орналасқан шеттен бастап нөмірлейді.
- атаудың алдында көміртегі атомының қайсысына орын басушы топ(радикал) орналасқанын цифрмен көрсетеді.
- егер орын басушы топ бірнешеу болса, цифрмен оның әрқайсысын көрсетеді.
- атаудың соңына қос байланыстың орнын көрсетеді, оны қос байланыс басталатын көміртегі атомының нөмірімен белгілейді.
CH 2 = CH - CH 2 - CH 3 СН 3 - СН = СН - СН 3
Бутен - 1 Бутен - 2
Химиялық қасиеттері.
1. Этилен көмірсутектер қаныққан көмірсутектердегідей химиялық элементтерден(көміртегі және сутегінен) құралатын болғандықтан, бұлардың қасиеттері де бірдей - жанғыш болып келеді. Мысалы, этиленді жаққанда ауада су және көміртегі(IV) оксидін түзе жанады.
С 2 Н 4 + 3О 2 → 2СО 2 + 2Н 2 О + Q
2. Гидрлеу реакциясы: (затқа сутегі қосыла жүретін реакциялар - гидрлену немесе гидрогендену деп аталады)
С 3 Н 6 + Н 2 →С 3 Н 8
3. Галогенденуі:
Н 2 С = СН 2 + Br 2 →BrH 2 C - CH 2 Br
1, 2 - дибромэтан
Тізбек сызықшалы макромолекулалардың ("макрос" - грекше үлкен, ұзын деген мағынаны білдіреді) құралған үлкен молекулалы зат түзіледі. Бірдей молекулалардың ірі молекула болып, бірігіп қосылу процессін полимерлену реакциясы, оның өнімін полимердеп атайды. Полиэтилен дегеніміз - полимер, оның молекулалық массасы бірнеше жүздеген мыңға жетеді. Этиленнің полимерлену реакциясы теңдеуін қысқаша түрде мынадай етіп көрсетуге болады:
nCH 2 = CH 2 → (-СН 2 - СН 2 -) n
3) АРОМАТТЫ КӨМІРСУТЕКТЕР.
1. Бензол құрылысы
Ароматты көмірсутектердің басты өкілі-бензол. Оны 1825 ж. М. Фарадей жарық газын зерттей отырып, соның құрамынан тапқан, ал Э. Митчерлих 1834 ж. бензой қышқылын құрғақ айдау арқылы алған.
Кекуле 1865 ж. бензолдың циклді формуласын ұсынды. Кекуле бойынша бензол молекуласы қосыаланған үш байланысы бар циклогексатриенді тұйық жүйе:
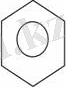
Бұл формуланы қазіргі күнге дейін қолданып жүр.
Бензол және оның туындыларының өздеріне тән ерекше қасиеттері бар.
1. Ароматты көмірсутектердің молекуласында алты π-электрондардың біртұтас тұйық электрондық система құруы-ароматикалық қасиеттің басты белгісі. Бұл бензол және оның гомологтарының физикалық және химиялық қасиеттерін анықтайды.
2. Ароматты көмірсутектер тотықтырғыштардың әрекетіне тұрақты.
3. Ароматты көмірсутектер қосылу реакциясына қиын түседі, ал электрофильді орынбасу реакциясына оңай түседі.
2. Алу жолдары және табиғи көздері
Ароматты көмірсутектерді негізінен тас көмірді құрғақ айдау арқылы алады. Ол үшін тас көмірді 900-1000 0 С ауа қатыстырмай қыздырады. Нәтижесінде құрғақ қалдық кокс, газдар мен тас көмір смоласы алынады. 1м 3 газдың құрамында 30 г. бензол және 10 г. толуол болады. Смола құрамында бензол, толуол, ксилол, фенолдар, көп ядролы ароматты көмірсутектер және гетероциклді қосылыстар болады.
Бензол молекуласын алудың көптеген синтетикалық жолдары бар:
1. Алкандар оксидті катализатордың қатысуында циклдену және дегидрогендеу реакцияларына түсіп, арендер түзеді:
А) H
3
C-(CH
2
)
5
-CH
3
 C
6
H
5
-CH
3
+4H
2
(Cr
2
O
3
кат. қатысында)
C
6
H
5
-CH
3
+4H
2
(Cr
2
O
3
кат. қатысында)
B) H
3
C-(CH
2
)
6
-CH
3
 (о-) C
6
H
4
CH
3
CH
3
(Cr
2
O
3
кат. қатысында)
(о-) C
6
H
4
CH
3
CH
3
(Cr
2
O
3
кат. қатысында)
2. Ацетилен және оның гомологтары металлорганикалық катализатордың қатысуында циклотримерлену реакциясына түсіп, бензол және оның гомологтарын түзеді:
3CH
3
-C≡CH
 (1, 3, 5) C
6
H
3
(CH
3
)
3
(1, 3, 5) C
6
H
3
(CH
3
)
3
3. Циклоалкандар жоғары темтературада және катализатордың қатысуында дегидрогенделіп, арендерге айналады.
4. Бензой қышқылының тұздары сілтімен қосып айдау арқылы бензол алады:
C
6
H
5
COONa+NaOH
 C
6
H
6
+Na
2
CO
3
C
6
H
6
+Na
2
CO
3
5. Бензол гомологтарын галоген туындылардан Вюрц-Фиттиг (1864) реакциясы бойынша жеңіл алады:
C 6 H 5 Br+2Na+BrC 2 H 5 →C 6 H 5 -C 2 H 5 +2NaBr
6. Бензол гомологтарын алудың маңызды әдісі Фридель-Крафтс-Густавсон реакциясы (1877) :
C 6 H 5 -CO-CH 3 +2H 2 →C 6 H 5 -C 2 H 5 +H 2 O
Тотықсыздану реакциясы қышқылдық ортада мырыш амальгамасының қатысуында жүреді.
3. Бензолдың физикалық қасиеті
Бензолдың гомлогтық қатарының төменгі өкілдері, негізінен сұйықтық болады. Оның молекулалық массасы өскен сайын қайнау температурасы да, артады, орта-изомерлер, әдетте, пара-изомерлерге қарағанда жоғары температурада қайнайды.
Бензолдың қайнау температурасы (80, 1 0 С) гексанның қайнау температурасынан (68, 8 0 С) жоғары.
Симметриялы құрылысты изомерлердің балқу температурасы жоғарырақ болып келеді. Екі орынбасарлары изомерлердің ішінде-пара-изомер ең жоғары температурада балқиды.
Май қатары мен алициклді қатар көмірсутектерден тығыздығы және жарық сындыру көрсеткіштері анағұрлым жоғары.
Бензол қатарындағы ароматты көмірсутектер судан жеңіл, суда ерімейді, ал көптеген органикалық еріткіштерде жақсы ериді. Олардың буымен ұзақ уақыт тыныс алғанда адам уланады.
Ароматикалық көмірсутектердің физикалық қасиеттері

4. Химиялық қасиеттері
Қосылу реакциялары. Ароматты көмірсутектер кәдімгі жағдайда қосылу реакциясына түспейді, яғни олар борм суын, калий перманганатының ерітіндісін түссіздендірмейді. Бірақ ерекше жағдайларда қосылу реакциясына түсіруге болады.
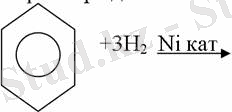
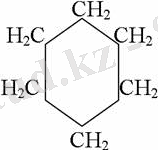
1. Катализатордың қатысуында және жоғары температурада ароматты көмірсутектер сутекті қосып алып, циклогексан және оның гомологтарын түзеді.
1 2. Ультракүлгін сәуленің әсерінен арендер хлор мен бромды қосып алып, гексагалогенидтер түзеді.
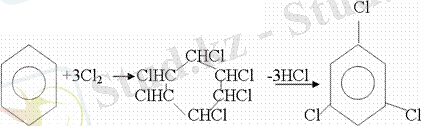
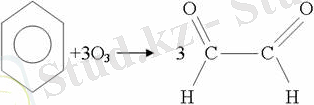
3. Бензол мен оның гомологтары қанықпаған көмірсутектер секілді озонды қосып алып, өте қопарылғыш зат-үш озонидтер түзеді. Бұл озонидтер сумен гидролизденіп, дикарбонильді қосылыстар (глиоксаль) түзеді.
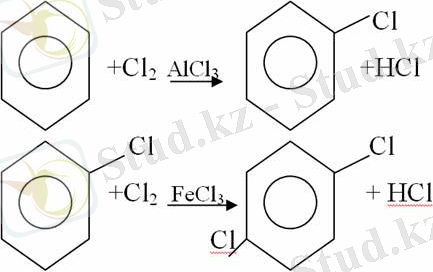
Орынбасу реакциялары. Бензол мен оның гомологтары галогендермен (катализатордың қатысуымен), азот және күкірт қышқылдарымен басқаша әрекеттеседі. Барлық жағдайда да атомдар мен қалдықтар бензол ядросы сутектерінің орнын басады.
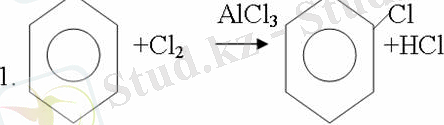
1. Катализатордың, мысалы, темірдің қатысуымен хлор немесе бром бензолмен әрекеттестіргенде галоген сутек атомдарының орнын басады, әрі бағытталу ережесі сақталады: хлор бензолдан көбінесе дихлор бензолдардың пара-изомері алынады:
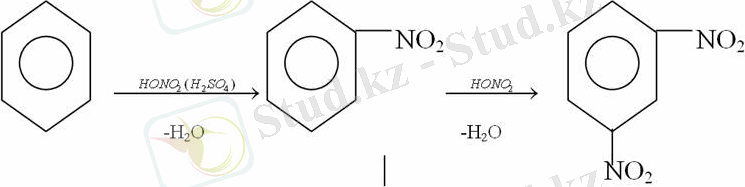
2. Бензолға нитрлегіш қоспамен (азот және күкірт қышқылдарының қоспасы) әсер еткенде сутек атомдарының орнын нитротоп басады. Нитрлеу әрі қарай жүргенде де орнын басу ережесі сақталады: нитробензолдан динитробензолдың мета-изомері алынады.
5. Бензолдың қолданылуы.
Бензол-кең түрде қолданылатын арен. Бензолды еріткіш ретінде көп қолданады. Ол майларды, каучукті, полимерлерді, лактарды, мұнай өнімдерін жақсы ерітеді. Бензол суда нашар ериді, сумен азеотропты қоспа түзеді. Химиялық өнеркәсіпте нитробензол, хлорбензол, анилин, фенол, стирол және т. б. өнімді алу үшін шикізат ретінде қолданады.
4) Алкандар
Алкандар - молекула құрамындағы көміртек атомдары өзара тек дара σ-байланыстар арқылы байланысқан жалпы формуласы C n H 2n+2 болатын алифатты қаныққан көмірсутектер.
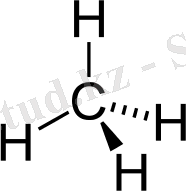
Ең қарапайым алкан - метанның құырылымы
Алкандардың молекуласындағы әр көміртек атомының барлық төрт валенттігі толығымен, яғни шетіне дейін сутек және көміртек атомдарымен қаныққан. Сондықтан алкандар қаныққан (шектелген) көмірсутектерге жатады.
Алкандардың изомерлері мен атаулары
Изомерленудің бірнеше себебі болатынын өткен тақырыптардан білесіңдер. Алкандарға құрылымдық (көміртек қаңқасының) изомерлену тән. Ол молекуладағы көміртек атомдарының өзара орналасуынан болады. Тармақталмаған көміртек тізбегі нормалді изомер деп аталады.
Алкандардың изомерленуі бутаннан (С 4 Н 10 ) басталады. Бутанның молекуласында барлық көміртек атомдары тізбектеліп орналасады (н-бутан) . Ал изобутанда көміртек атомдары тармақталып байланысады, негізгі көміртек тізбегі үш атомнан тұрады да, 4-көміртек атомы үзіліп, бүйірінен 2-көміртекпен байланысады.
Тармақталған изомерлерде радикалдар әр түрлі орналасуы мүмкін.
Қосылыс құрамындағы көміртек атомдарының сандары өскен сайын изомерлердің сандары да көбейе береді
Алкандардың бастапқы төрт көмірсутегі тривиальді аттармен аталады: метан, этан, пропан, бутан. Ал бесінші көмірсутек- пентаннан бастап грек сандарына -ан жұрнағы жалғанып аталады.
Рационалды атау бойынша көмірсутектер бір немесе бірнеше сутек атомдары радикалдарға алмасқан метанның туындылары ретінде қарастырылады. Егер формулаларда бірдей радикалдар қайталанса, грекше ди-, три-, тетра-, т. б. сандармен көрсетіледі. Метан көміртегінің негізі етіп ең көп тармақталған көміртек атомы алынады
Физикалық қасиеттері
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz