Томсон мен Резерфорд атом модельдері және олардың эксперименттік негіздері


Кіріспе3
1. Томсонның және Резерфордтың атом моделі5
2. Екінші модель - Э. Резерфордтың планетарлық моделі. 12
Қорытынды14
Пайдаланған әдебиеттер16
КіріспеXIX ғасырдың аяғына дейін атом заттың бөлінбейтін өзгермейтін бөлшегі деп саналып келді. XIX ғасырдың аяғы мен ХХ- ғасырдың бас кезіндегі ғылыми жаңалықтар (радиоактивтік құбылыс жəне рентген сəулелерінің ашылуы, электронның табылуы т. б. ) негізінен атомның күрделі бөлшек екендігін сипаттады. Сонымен атом құрамында электронның болатындығы белгілі болды. Электронның массасы m e = 9. 1 · 10 -31 кг , ал заряды e = 1. 6·10 - 19 Кл , болатын теріс зарядты элементар бөлшек. Бірақ қалыпты жағдайда атом заряды білінбейді, сондықтан да атом бейтарап бөлшек, оның оң зарядты бөлшектерінің шамасы электрондардың зарядына тең болуға тиіс, сонда ғана атом бейтарап бола алады.
ХХ ғасырдың бас кезінде атомның күрделі бөлшек екендігі анықталды, олай болса атомның оң жəне теріс зарядты бөлшектері болады. Осы оң зарядты иеленуші қандай бөлшек жəне электронның қозғалысының себебі неден, олардың орналасуы қалай болатындығы жəне атомның құрылысы қандай екендігі белгісіз болды.
ХХ ғасырдың бас кезінде осы атомның құрылысы жөнінде бірқатар көзқарастар (пікірлер) айтылып, атомның екі моделі ұсынылды:
Қазіргі кезде біз атомның оң зарядталған ядродан және сол ядроны айнала қозғалатын теріс зарядталған электроннан тұратынын жақсы білеміз. Электрон теріс зарядталған бөлшек. Ядроның заряды оң. Ол +eZ-ке тең, мұндағы е-электрон зарядының шамасы, z- Менделеев кестесіндегі элементтің (реттік) атомдық нөмірі.
Барлық заттар бөлiнбейтiн аса ұсақ бөлшектерден - атомдардан тұрады деген ұғым ерте қалыптасқан болатын. Егер атом шындығында заттың бөлiнбейтiн алғашқы кiрпiштерi болса табиғаттағы кездесетiн сан алуан заттарға сан алуан атомдар сәйкес қойылуы тиiс. Бұлай болуы бiр жағынан күмән туғызады.
Физика ғылымының дамуы барысында ХIХ ғасырдың аяғына қарата атомның қасиеттерiне байланысты жаңа тәжiрибелiк деректер жинала бастады. Мысалы М. Фарадей 1833 жылы электролиз құбылысын зерттеу барысында электролит ертiндiлерiндегi ток иондардың реттелген қозғалысы екенiн анықтады. Ал 1897 жылы Дж. Томсон сиретiлген газдардағы электр разрядын зерттеу барысында қыздырылған немесе ультракүлгiн жарықпен сәулелендiрiлген кез-келген химиялық элементтiң атомы өзiнен терiс зарядталған бөлшектердi шығатынын анықтады. Осылай алғашқы элементар бөлшек - электрон ашылды. Атом құрлысының күрделiлiгiне нұсқайтын тағы бiр бұлтартпас факт 1869 жылы орыс ғалымы Д. И. Менделеев ашқан химиядық элементтердiң периодтылық заңы. Атомдық масса өскен кезде элементтердiң қасиеттерiнiң қайталануын атомның құрамына кiретiн бөлшектердiң саны өскен кезде оның iшкi құрылымының қандай да бiр ерекшелiгiнiң қайталануымен түсiндiруге болатындай.
1. Томсонның және Резерфордтың атом моделіДжозеф Джон Томсон
Ағылшын физигі. Ол электронның ашылуына көп үлес қосты. Сондықтан осы ғалым электронды ашты деп есептелінеді. Он тоғызыншы ғасырдың соңында Кембридж университетінде жұмыс істеді. 1906 жылы Томсон тоқтың газ бойымен өтуі бойынша теориялық және тәжірибелік зерттеулеріндегі еңбегі үшін Нобель сыйлығына ие болды. Ол сонымен қатар бірінші массалық спектрометрді жасап шығарды.
Эрнест Резерфорд
Ағылшын физигі. Ол радиоактивтік негіздерін және атом құрылысын анықтады. Сонымен қатар, ол альфа, бета және гамма сәулеленулерінің арасында айырмашылықтар бар екенін дәлелдеді. Ол радиоактивті ыдырау теориясын жасап, 1908 жылы химия бойынша радиоактивтілікке жүргізген зерттеулері үшін Нобель сыйлығына ие болды. Оның жүргізген зерттеулері 1911 жылы атомның планетарлық моделі деген атпен белгілі атом моделінің пайда болуына негіз болды.
Ядро және атом
Атомның өлшемі шамамен 10 -10 м-ді құрайды. Ал оның ядросының өлшемі шамамен 10 -15 м-ді құрайды. Алайда атомның шамамен барлық массасы оның ядросында шоғырланған. Осы сөйлемнің соңындағы нүкте шамамен бір біріне жақын орналасқан 2, 5 миллион атомнан құралған. Ядроның тығыздығы өте жоғары болып келеді. Ол шамамен 10 17 кг/м 3 -ті құрайды. Осындый материалдан жасалған милиметр куб шамамен 100 000 тоннаны құрайды.
Спектрлік анализ
Егер біз газдың жарықтануын туғызып, газды саңылау арқылы өткізіп, содан кейін оны дифракциялық тор арқылы өткізетін болсақ, біз сызықтық спектр деп аталатын жүйелі сызықшаларды аламыз. Әр элемент газ күйінде болған кезде, оның жарықтануы кезінде белгілі бір сәуле шығарады. Алынған спектрдегі әрбір жолақ белгілі бір жиіліктегі шығарылған сәулеге сәйкес келеді. Сәулелену спектрі туралы ғылым, спектрлік анализ, бізге атомдардың құрылымы туралы мәлімет береді.
Жұлдыздар
Жұлдыздардың сәулесіне жасалынған спектрлік анализ бізге оларды құрайтын элементтер туралы мәлімет береді. Осы тәсіл арқылы алғаш рет гелий, 1868 жылы, Күнде анықталды, ал кейінрек 1895 жылы ол жерден табылды.
Атомның алғашқы үлгілерінің бірін Дж. Томсон ұсынды. Бұл үлгіде атом радиусы ~10 −10 К) м оң зарядталған шар ретінде қарастырылады. Шардың ішінде тепе-теңдікжағдайының маңында электрондар тербеліп тұрады. Электрондардың теріс зарядтарының қосындысы шарға біркелкі таралған оң зарядты теңестіреді, сондықтан тұтас алғанда атом электрлік бейтарап бөлшек болады. Кейінгі зерттеулер бұл модельдің дұрыс емес екенін көрсетті, сондықтан Томсон моделі қазір тек тарихи тұрғыдан қарастырылады.
Атомның ішінде электр зарядтарының орналасу тәртібін анықтау үшін 1911 жылы Резерфорд өзінің шекірттері Г. Гейгер және Э . Марсденмен бірге альфа-бөлшектершоғын өте жұқа алтын фольгадан өткізіп, бірнеше тәжірибелер жасады. Осы тәжірибелерді зерделеу нәтижесінде атомның ядролық, басқаша айтсақ, планетарлық моделі өмірге келді.
Тәжірибенің нәтижесінде альфа-бөлшектердің басым көпшілігі фольгадан өткенде алғашқы бағыттан aуытқымайтыны (φ≈1-2°) анықталды. Бұл нәтиже, негізінен, Томсон моделіне сүйеніп жасалған есептеулермен дәл келді. Бірақ, альфа- бөлшектердің мардымсыз аз бөлігі 90°-тан артық бұрышқа ауытқитыны, яғни олар фольгаға соғылып, кері бағытта ұшатыны таңдандырды. Сегіз мыңға жуық бөлшектердің біреуі ғана осындай үлкен бұрышқа ауытқиды екен! Мұны Томсон моделі негізінде түсіндіру тіпті мүмкін болмады.
Тәжірибеде алынған нәтижелерді зерделей отырып Резерфорд өз моделін ұсынды. Ол атомның оң заряды оның ортасында орналасқан радиусы шамамен 10 −15 м өте аз көлемге жинақталған деген қорытындыға келді. Бұл орталық бөлшекті Резерфорд ядро деп атады. Атомның массасы түгел дерлік ядрода шоғырланған. Ядроныайнала әр түрлі орбиталармен электрондар қозғалып жүреді. Ең шеткі электрон орбитасының радиусы атомның радиусына тең, R a ≈10 −10 м. Бұл үлгі Күн жүйесініңқұрылымына ұқсайтын болғандықтан, оны атомның планетарлық моделі деп те атайды. Модель бойынша атом көлемінің басым көпшілік бөлігі "бос" болып шығады, ядроның радиусы атомның радиусынан 100 000 есе кіші. Орбиталардағы электрондардың теріс зарядтарының қосындысы ядроның оң зарядына тең, атом электрлік бейтарап.
Атомның ішіндегі бос кеңістік "өте үлкен". Сондықтан, фольга арқылы өткенде альфа-бөлшектерінің көбі ядродан алыс өтеді де, шашырамайды. Электрондар альфа-бөлшектен 8 мың еседей жеңіл болғандықтан, оның қозғалыс траекториясын өзгерте алмайды. Тек ядроға тікелей қарсы келіп қалған альфа-бөлшектер ғана онымен әсерлесіп, кері ұшады. Мұндай бөлшектер саны ядро радиусының атом радиусына қатынасымен анықталады.
Жоғарыда біз тәжірибеге тек сапалық талдау жүргіздік. Резерфорд сонымен қатар өз моделінің және Томсон моделінің негізшде есептеу жұмыстарын жүргізді, олардың нәтижесі Резерфорд үлгісінің дұрыстығын көрсетті. Бірақ классикалық физика тұрғысынан мұндай атомның орнықты болуы мүмкін емес. Бұдан бұрын айтылғандай, зарядталған бөлшек үдемелі қозғалса, міндетті түрде сәулеленуі (электромагниттік толқындар шығаруы) керек. Бұл сәулеленудің жиілігі электронның ядро маңында айналу жиілігіне тең болуы тиіс. Электрон ядроны айнала дөңгелек орбитамен қозғалса, оның центрге тартқыш үдеуі бар. Олай болса, электрон сәуле шығара отырып, өз энергиясын азайтуы тиіс. Энергияның (орбиталық жылдамдықтың) азаюы электронның ядроға кулон күшінің әсерінен біртіндеп жақындап, ақыры оған құлап түсуіне әкеп соғады. Бұған бар болғаны 10 −8 с-ка тең уақыт кетеді екен және классикалық теория бойынша мұндай атомның сәулелену спектрі тұтас болу керек, ал шын мәнінде атомдық спектрдің сызықтық болатынын алдыңғы тақырыпта айтып кеттік.
Сайып келгенде, бұл жерде классикалық физиканың заңдары жүрмейтін болып шықты. Тіпті жоғарыда әңгіме болған атомның планетарлық моделі, дәл айтқанда ол бар болғаны нағыз атомның механикалық үлгісі екеніне біртіндеп көзіміз жетеді.
20 ғасырдың бас кезінде атомның шын бар екендігі ешқандай күмәнсіз жалпылай мойындалды. Атом моделін ұсынған ағылшын физигі Дж. Томсон (1902-1904жж) болды.
Бұл атомның күрделі құрамы белгілі ғылыми деректерге сүйеніп ұсыналған атомның алғашқы физикалық моделі. Бірақ бұл модель тікелей тәжірибеге негізделмегендіктен болжау ғана еді. осы модельге сәйкес атомның оң заряды сфера тәрізді атомды біркелкі толтырып тұруға тиіс. Ал оның ішінде нүктелік теріс зарядтар -электрондар атом бүтіндей бейтарап болатындай мөлшерде сфераның әр жеріне орналасқан болады.
Томсон моделі тәжірибеге қайшы келді. тұтасынан алғанда томсон моделі көптеген күдік туғызды. томсон моделінің кемшілігін ағылшын физигі Резерфорд көрсетті. Э. Резерфорд және оның шәкірті Э. Марсден, Г. Гейгер тәжірибелері нәтижесіне сүйене атомның жаңа ядролық моделін ұсынды. Резерфорд α бөлшектер көмегімен тәжірибе жасады. α бөлшектер шапшаң қозғалатын ауыр бөлшектер, затпен әсерлескенде, зат атомдарына енуі мүмкін. Тәжірибе нәтижесінде келесі ұйғарымға келеді: атом өте кішкентай, бірақ ауыр, оң зарядталған ядродан және осы қайсібір қашықтықта қоршаған электрондардан тұрады. Электрондар ядросы айналып қозғалуы тиіс болды. өйткені егер олар тыныштықта болса, онда электрлік кулондық тарту әсерінен ядроға құлаған болар еді. Резерфордтың бағалауы бойынша ядро мөлшерінің реттік шамасы 10 -15 -10 -14 м болуға тиіс. Резерфорд атомының құрылысы планеталар жүйесіне ұқсас деген жорамал ұсынды. Күннің айналасында үлкен қашықтықтарда планеталар қалай айналып жүретін болса, дәл солай атомның ішінде электрондар ядроны айналып жүреді. Атом құрылысының осындай моделі планетарлық немесе ядролық модель деп аталады.
Ағылшынның физигі Д. Д. Томсонның (1903 ж. ) болжауы бойынша, атом дегеніміз оң жəне теріс электронмен бірқалыпты зарядталған сфера, теріс зарядты электрондар осы сфераның ішкі жағына орналасқан. Сфера ішіндегі барлық электрондардың зарядының мөлшері, оның оң зарядына тең, сондықтан атом бейтарап. Электрон қозғалғанда оған квазисерпімді күш
(1. 1. 1)
əсер етіп, ол гармониялық тербеліске келеді. Атомның бұл моделіне сүйеніп, тербелген атомдардың жарық шығаруын түсіндіруге болады, бірақ атом спектрінде болатын
заңдылықтарды жəне басқа құбылыстарды түсіндіруге келмейді. Томсон моделі бойынша атом ішіндегі оң жəне теріс зарядтар туралы айтылған пікір тəжірибеге негізделмеген, сондықтан да бұл модель сəтсіз болды. Томсон ұсынысы бойынша оң-теріс бөлшектер электр күші арқылы байланысып тұрады.
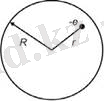
Д. Д. Томсон моделінің негізгі кемшілігі атомдағы, оң жəне теріс зарядтарды араласып жатуында. Томсон моделін тамшылық модель дейміз (1. 1-сурет) .
сы бірқалыпты зарядталған сфера ішінде заряд тығыздығы:
(1. 1. 2)

өріс кернеулігі мына формуламен анықталады:
мұндағы, е - сфера заряды, R - сфера радиусы немесе атом радиусы. +
Тепе-теңдік қалыптан r қашықтықтағы электронға əсер ететін күш:
(1) мен (4) теңдікті теңестірсек
1 e 2 r kx r x ;
4 0 R 3

 kr m
2
r
kr m
2
r
0 0
1. 1-сурет
 сонда атом радусы
сонда атом радусы
1/ 3
R e 2 2 (1. 1. 6)

4 0 m 0 0
осы формуладағы ω0 орнына сутегі атомының сызықтық жиілігін (ω=3·10 15 Гц) қойып, атом радиусын тапсақ, 3·10 м болып шығады.
2. Екінші модель - Э. Резерфордтың планетарлық моделі. Радиоактивтік құбылыс ашылғаннан (1896 ж. ) кейін атом құрылысының күрделі екендігі анықталды.
1906 жылы Э. Резерфорд атом құрылысын зерттеу үшін іргелі тəжірибелер жасап, ол - бөлшегімен азот атомын атқылау нəтижесінде, ауыр - бөлшегінің шашырайтындығын байқады. Тəжірибелер нəтижесінде - бөлшектерінің көпшілігі заттан өткенде өзінің бастапқы бағытын сақтап, қалатындығы, ал аздаған бөлігі бағытын өзгертіп бастапқы қалпынан өте үлкен шамаға дейін ауытқитындығын анықтады. Резерфордпен оның шəкірттері Гейгер жə не Марсден -бөлшегінің іздерін фотопластинкаға түсіріп, ауытқу бұрыштарын анықтады. Ол үшін синтилляциялық əдісті қолданды. Осы əдіс бойынша металл фалгадан шашырап, бастапқы бағытынан ауытқыған - бөлшегінің саны, төрт дəрежеленген шашырау бұрышының жартысының синусына кері пропорционал болатындығын анықтады, яғни
Осыларды қорыта келіп Резерфорд мынадай қорытындыға келді:
~ 15 ~
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz