Қышқылдар, сілтілер, тұздар және оксидтердің химиялық қасиеттері, алынуы, жіктелуі және бейорганикалық қосылыстардың генетикалық байланыстары


Қышқылдар, сілтілер, тұздар мен оксидтердің химиялық қасиеттері, алынуы, классификациясы . Бейорганикалық қосылыстардың арасындағы генетикалық байланыстар.

Негіздік оксидтерге негіздер сәйкес, негіздік окситердің металл төменгі тотығу дәрежесін ТД көрсетеді (+1, +2) .
Мысалы:
K 2 O - калий оксиді, KOH - калий гидроксиді
CaO - кальций оксиді, Ca(OH) 2 - кальций гидроксиді
FeO - темір (ІІ) оксиді, Fe(OH) 2 - темір (ІІ) гидроксиді
CrO - хром (ІІ) оксиді, Cr(OH) 2 - хром (ІІ) гидроксиді.
Екідайлы оксидтерде металдар жоғары тотығу дәрежелерді көрсетеді: +2, +3, +4.
Мысалы:
Al 2 O 3 - алюминий оксиді (ТД(Al) = +3, топ нөмеріне сәйкес)
Fe 2 O 3 - темір (ІІІ) оксиді
Cr 2 O 3 - хром (ІІІ) оксиді
ZnO - мырыш оксиді (ТД(Zn) = +2, топ нөмеріне сәйкес)
Қышқылдық оксидтер қышқылдарға сәйкес, құрамында бейметалдар:
CO 2 - көміртек (IV) оксиді; H 2 CO 3 - көміртек қышқылы
SO 2 - күкірт (IV) оксиді; H 2 SO 3 - күкіртті қышқыл
SO 3 - күкірт (VI) оксиді; H 2 SO 4 - күкірт қышқылы
P 2 O 5 - фосфор (V) оксиді; H 3 PO 4 - фосфор қышқылы
және жоғары тотығу дәрежелерін көрсететін (+5, +6, +7) металдар болады:
Cr 2 O 3 - хром (VI) оксиді, хром ангидриді; H 2 Cr 2 O 7 - дихром және HCrO 4 хром қышқылдары сәйкес
Mn 2 O 7 - марганец (VІІ) оксиді, HMnO 4 - марганец қышқылы.
Оксидтердің алу жолдары
1. Жай және күрделі заттарды оттекпен тотықтыру арқылы:
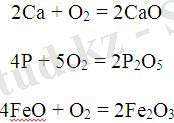
2. Негіздерді, қышқылдарды, тұздарды термиялық ыдырау:
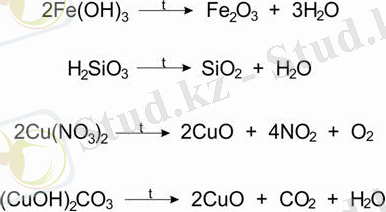
Оксидтердің химиялық қасиеттері:
1. Сумен әрекеттесуі:
а) негіздік оксид + су = сілті
CaO + H 2 O = Ca(OH) 2
б) қышқылдық оксид + су = қышқыл
SO 3 + H 2 O = H 2 SO 4
2. оксидтермен әрекеттесуі:
а) қышқылдық оксид + негіздік оксид = тұз
CO 2 + CaO = CaCO 3
б) қышқылдық оксид + екідайлы оксид = тұз
3SO 3 + Al 2 O 3 = Al 2 (SO 4 ) 3
в) негіздік оксид + екідайлы оксид = тұз
Na 2 O + ZnO = Na 2 ZnO 2
3. Қышқылдармен және негіздермен әрекеттесуі:
а) негіздік оксид + қышқыл = тұз + Н 2 О
MgO + 2HCl = MgCl 2 + H 2 O
б) қышқылдық оксид + негіз = тұз + Н 2 О
CO 2 + 2NaOH = Na 2 CO 3 + H 2 O
в) екідайлы оксид + негіз = тұз + Н 2 О
Al 2 O 3 + 6HCl = 2AlCl 3 + 3H 2 O
г) екідайлы оксид + негіз = тұз + Н 2 О
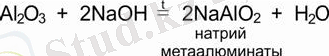
Негіздердің судағы ерігіштігі бойынша суда еритін негіздер (сілтілер) мен суда ерімейтін негіздер деп жіктейді. Екідайлы негіздер қышқылдар мен негіздермен әрекеттеседі.
Негіздердің алынуы:
1) сумен әрекеттесуі:
активті метал + су = сілті + сутек
2Na + 2H 2 O = 2NaOH + H 2
сілтілік және сілтілікжер метал оксидтері + су = сілті
CaO + H 2 O = Ca(OH) 2
2) ерімтал тұз + сілті = ерімейтін негіз + су
FeSO 4 + 2NaOH = Fe(OH) 2 ↓ + Na 2 SO 4
K 2 CO 3 + Ba(OH) 2 = 2KOH + BaCO 3 ↓
3) тұздардың сулы ерітінділерінің электролизі:
2NaCl + 2H 2 O = 2NaOH + H 2 ↑ + Cl 2 ↑
Негіздердің химиялық қасиеттері:
1. Бейтараптану реакция
а) негіз + қышқыл = тұз + Н 2 О
3NaOH + H 3 PO 4 = Na 3 PO 4 + 3H 2 O
Cu(OH) 2 + 2HCl = CuCl 2 + 2H 2 O
б) негіз + қышқылдық тұз = орта тұз + су
Ca(OH) 2 + Ca(HCO 3 ) 2 = CaCO 3 ↓ + 3H 2 O
2. қышқылдық оксид + негіз = тұз + су
SO 2 + 2KOH = K 2 CO 3 + H 2 O
3. термиялық ыдырау:

Қышқылдардың жіктелуі
1) қышқыл қалдығының табиғаты бойынша:
а) оттексіз қышқылдар:
HCl -хлорсутек қышқылы, тұз қышқылы
H 2 S - күкіртсутек қышқылы
б) оттекті қышқылдар:
H 2 SO 4 - күкірт қышқылы
HClO 4 - хлор қышқылы
2) қышқыл құрамындағы металл атомдарымен орынбасу сутек атом сандары бойынша;
а) бірнегізді қышқылдар:
HNO 3 - азот қышқылы
HBr - бромсутек қышқылы
б) көпнегізді қышқылдар:
H 2 S (екінегізді),
H 3 BO 3 (үшнегізді) - бор қышқылы.
Қышқылдардың алу жолдары
1. қышқылдық оксид + су = қышқыл
P 2 O 5 + 3H 2 O = 2H 3 PO 4
2. әлсіз қышқылдық тұз + күшті қышқыл = тұз + қышқыл
Na 2 SiO 3 + 2HCl = H 2 SiO 3 ↓ + 2KCl
3. қатты тұз + концентрлі күкірт қышқылы = ұшқыш қышқыл + тұз
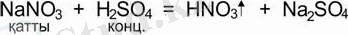
Қышқылдардың химиялық қасиеттері:
1. металл + қышқыл = тұз + сутек
(металдардың электрохимиялық кернеу қатарында сутекке дейін орналасқан металдар)
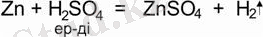
2. негіздік оксид + қышқыл = тұз + Н 2 О
CuO + 2HCl = CuCl 2 + H 2 O
3. негіз + қышқыл = тұз + Н 2 О
Ba(OH) 2 + H 2 SO 4 = BaSO 4 + 2H 2 O
4. тұз + қышқыл = жаңа тұз + жаңа қышқыл
Күшті қышқыл әлсіз қышқылдарды тұздарынан ығыстырады.
CH 3 COONa + HCl = CH 3 COOH + NaCl
Тұздардың жіктелуі
1) орта тұздар - қышқыл құрамындағы сутек атомдары толығымен металл атомдарына алмасқан. Мысалы: Na 2 SO 4 , Na 3 PO 4 , K 2 CO 3
2) қышқылдық тұздар - қышқыл құрамындағы сутек атомдары толық металл атомдарына алмаспаған. Мысалы:
KH 2 PO 4 - калий дигидрофосфаты
NaHCO 3 - натрий гидрокарбонаты
3) негіздік тұздар - негіз құрамындағы гидроксид топтары толық қышқыл қалдықтарына алмаспаған. MgOHCl - магний хлоридінің негіздік тұзы, магнийдің гидроксохлориді.
4) кешенді тұздар - олардың құрамындағы күрделі катион немесе анион кешен түзуші метал мен лигандлардан тұрады. Мысалы:

K 3 [Fe(CN) 6 ] - калийдің гексацианоферрат (ІІІ) (қызыл қан тұзы)
5) Қос тұздар - екі катиондар мен анионның арасында түзіледі, KAl(SO 4 ) 2
6) Аралас тұздар - бір катионмен екі аниондардан арасында пайда болады: CaOCl 2 кальций гипохлориті-хлориді
Орта тұздардың алынуы
1) Қышқылдардың металдармен, негіздік және екідайлы оксидтермен және негіздермен әрекеттесуі:
Zn + 2HCl = ZnCl 2 + H 2 ↑
MgO + H 2 SO 4 = MgSO 4 + H 2 O
ZnO + 2HNO 3 = Zn(NO 3 ) 2 + H 2 O
3NaOH + H 3 PO 4 = Na 3 PO 4 + 3H 2 O
2) Негіздердің қышқылдық және екідайлы оксидтермен және қышқылдармен әрекеттесуі:
2KOH + CO 2 = K 2 CO 3 + H 2 O
2KOH + ZnO = K 2 ZnO 2 + H 2 O
2KOH + H 2 SO 4 = K 2 SO 4 + 2H 2 O
3) Қышқылдық және негіздік оксидтердің әрекеттесуі:
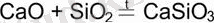
4) Алмасу реакция нәтижесінде:
тұз + тұз = жаңа тұз↓ + жаңа тұз
Ba(NO 3 ) 2 + Na 2 SO 4 = BaSO 4 ↓ + 2NaNO 3
қышқыл + тұз = жаңа тұз↓ + жаңа қышқыл
HCl + AgNO 3 = AgCl + HNO 3 .
Орта тұздардың қасиеттері:
1. Оттекті қышқылдар мен аммоний тұздарының термиялық айырылуы:
NH 4 NO 3 = N 2 O + 2H 2 O
NH 4 Cl = NH 3 ↑+ HCl
CaCO 3 = CaO + CO 2 ↑
2Pb(NO 3 ) 2 = 2PbO + 4NO 2 + O 2
2. Гидролизға ұшырайды:
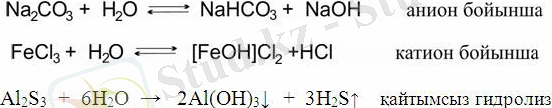
3. Қышқылдармен, негіздермен және тұздармен әрекеттесуі:
AgNO 3 + HCl = AgCl↓ + HNO 3
Al 2 (SO 4 ) 3 + 6KOH = 2Al(OH) 3 ↓ + 3K 2 SO 4
Ca(NO 3 ) 2 + Na 2 CO 3 = CaCO 3 ↓ + 2NaNO 3
Қышқылдық тұздардың алынуы:
1. Қышқыл (артық) + негіз = қышқылдық тұз + су
H 2 SO 4 + KOH = KHSO 4 + H 2 O
2. Қышқылдық оксид + негіз = қышқылдық тұз
(артық мөлшерде
алынған кезде)
2CO 2 + Ca(OH) 2 = Ca(HCO 3 ) 2
3. Орта тұз + қышқыл = қышқылдық тұз
CaSO 4 + H 2 SO 4 = Ca(HSO 4 ) 2
Қышқылдық тұздардың химиялық қасиеттері:
1) Қыздырғанда айырылады:
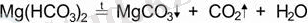
2) Бейтараптану реакцияға қатысады:
Mg(HCO 3 ) 2 + NaOH = MgCO 3 ↓ + NaHCO 3 + H 2 O
Негіздік тұздардың алынуы:
1) Орта тұздардың ерітінділеріне сілтінің аз мөлшерін қоссақ:
Al 2 (SO 4 ) 3 + 2NaOH = 2[AlOH] SO 4 + Na 2 SO 4
2) Әлсіз қышқылдардың тұздары орта тұздарға әсер еткенде:
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz