Титан және оның негізгі қосылыстары: таралуы, физика-химиялық қасиеттері, алынуы және қолданылуы


Титан және оның ең маңызды қосылыстары, олардың физикалық және химиялық қасиеттері, алынуы және қолданылуы
TiO 2 -ні бір-бірінен тәуелсіз ағылшын У. Грегор мен неміс химигі М. Г. Клапрот ашты. Ал титанның металл үлгісін 1825 жылы Й. Я. Берцелиус ашты
Титан табиғатта таралуы жағынан 10 -орында тұр. Жер қыртысында оны массасы- 0, 57 % құраса, теңіз суында - 0, 001 мг/л құрайды. Жер қыртысында титан үнемі төрт валентті және тек оттекпен қосылысы түрінде кездеседі. 30 %-ға дейін TiO 2 салмағы бойынша кейбір саздарда болады. Титан құрамына кіретін 100 деген минералдар табиғатта белгілі. Олардың ішінде маңыздылары:рутил TiO 2 , ильменит FeTiO 3 , титаномагнетит FeTiO 3 + Fe 3 O 4 , перовскит CaTiO 3 , титанит CaTiSiO 5 . Титанның кен орындары БАӘ, Ресей, Қытай, Жапония, Австралия, Индия, Цейлон, Бразилия, Оңтүстік Корея аумақтарында кездеседі. Титан кендері Қостанайда, Көкшетауда, Ақмола мен Ақтөбе облыстарында барланған. Ұлытау, Оңтүстік Алтайда және Жезқазған облысындағы қоры белгілі.
Титан өндірісі үшін және оның қосылыстары үшін негізгі бастапқы материал титан диоксиді болып табылады. Титан кендерінің концентратын күкірт қышқылымен немесе пиррометаллургиялық жолмен өңдейді. Пиррометаллургиялық өңдеуде титан диоксидінің ұнтағын кокспен пісіріп, хлормен өңдейді. Нтәижесінде төрхлорлы титан хлориді алынады:
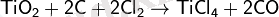
Түзілген TiCl 4 буларын 850 °C температурада магниймен тотықтырады:
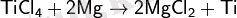
Алынған титанды қайта балқытып, тазартады.
Физикалық қасиеттері: Титан - жеңіл күміс тестес ақ металл. Екі түрлі кристалдық модификацияда болады: α-Ti гексагональді, β-Ti кубтық . Титан қиын балқитын металл болып табылады. Ұзақ уақыт бойы оны 1800 0 С-та балқиды деп есептелініп келсе, 50-жылдардың ортасына қарай агылшын ғалымдары таза титаннның балқу температурасын анықтады. Ол . 1668±3° С болды. Ол қиын балқитын металдардың арасында тек кейбір металдарға ғана орын береді. Олар: вольфрам, тантал, ниобий, рений, молибден, платиноиды, цирконий. Титанның маңызды физика-химиялық қаситеі : тығыздығыныңы төмен болуы, жоғары беріктік, қаттылығы. Бұл қасиеттерінің барлығы жоғары температура кезінде де сақталады. Оның тығыздығы 0° С кезінде 4, 517 г/см8 құраса, ал 100° С - 4, 506 г/см3 болады. Титан 1, 5 есе алюминийге қарағанда ауырырақ, және темірге қарағанда 1, 5 есе жеңілірек. Оның тағы бір маңызды көрсеткіші аққыштығының шектілігі. Бұл көрсеткіштің мәні жоғары болған сайын оның ауырлық қүшін көтеру дәрежесі жоғарылай береді. Титандағы аққыштықтың шегі алюминийге қарағанда 18 есе артық. Титан қорытпанларының меншікті беріктілігі 1, 5-2 есеге дейін артық болады. Оның механикалық беріктілігі жүздеген градустарда да жақсы сақталады.
Химиялық қасиеттері:
Титаннның коррозияға берік болуының себебі оның бетінде оксидтік қабатының пайда болуында. Титан сұйытылған сілті мен қышқылдардың әсеріне (HF, H3PO4 және конц. H2SO4 басқа) . тұрақты. Комплекстүзгіштердің қатысында әлсіз қышқылдармен де әрекеттесіп кетеді. Мысалы фторсутекпен
[TiF 6 ] 2− анионының қатысында әрекеттеседі. 1200 0 С-қа дейін ауада қыздырғанда ашық жалынмен жанып, қараяды. Титан тұздарының ерітінділерінң ішінде TiO(OH) 2 ·xH 2 O ғана тұнады, қыздыру нәтижесінде титан оксидін алады.
TiO
2
күкірт қышқылымен ұзақ уақыт қайнату нәтижесінде алынады. Содамен және Na
2
CO
3
поташпен K
2
CO
3
қыздыру нәтижесінде титан оксиді TiO
2
титанаттар түзеді:
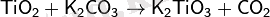
Қыздырған жағдайда титан галогеендермен әрекеттеседі. Төртхлорлы титан-қалыпты жағдайда түссіз сұйықтық, ауада түтінденеді. TiCl 4 -ті әртүрлі (күкірт, алюминий, кремний) тотықсыздандыру нәтижесінде үшхлорлы, екіхлорлы титан сияқты қатты заттар алынады. Олардың тотықсыздану қасиеттері жоғары болып, хлор, бром элементтерімен әрекеттеседі.
Азотпен титан 400 градустан жоғары температурада титан нитридін TiN x (x=0, 58-1, 00) түзеді.
Титанды қорытпалар -құрамына алюминий, молибден, ванадий, қалайы, темір, т. б. элементтер қосылған титан негізді қорытпалар. Титан болат пен басқа қорытпаларға қосылатын лигерлеуіш элемент ретінде пайдаланылады. Химиялық активтілігі жоғары болғандықтан титан балқымасы ауадан оттек, азот, сутек, т. б. элементтерді қарқынды жұтады. Осының салдарынан өнеркәсіптік деңгейде таза титанды өндіру қиындық туғызады. 20 ғасырдың 50-жылдары таза (99, 9%) титан өндіру тәсілдері пайда болды. Таза титан механикалық қасиеттері бойынша темірмен шамалас, бірақ меншікті салмағы одан екі еседей жеңіл және жегі орталарға төзімді келеді. Мұндай қасиеттер титанды қорытпаларда да сақталған. Титанды қорытпалардың беріктілігі жоғары, тығыздығы төмен. Сондықтан өнеркәсіпте көбінесе титанның қорытпалары пайдаланылады. Титанды қорытпалардың механикалық және физикалық қасиеттері әр түрлі болады. Ыстыққа төзімділігі жағынан титанды қорытпалар алюминийлі қорытпалар мен тоттанбайтын болат аралығында болады. Олар белгілі бір температураларда қатты күйден фазалық ауысуға ұшырайды. Бұл титанды қорытпаларды болаттар секілді терм. өңдеуге және қасиеттерін жан-жақты өзгертуге мүмкіндік туғызады. Титанды қорытпалар 300 - 500°С аралығында жұмыс істейтін реактивті қозғалтқыштар мен ядролық реакторлардың кейбір тетіктерін жасауға, авиация мен ракета жасау салаларында, энергетикалық машиналар мен кеме жасауға, химиялық өнеркәсіпте, тұрмыстық бұйымдардың кейбір бөліктерін жасауға, т. б. пайдаланылады. Қазақстанда титанды қорытпалардың едәуір бөлігі Өскемен титан-магний комбинатында шығарылады
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz