Ароматты көмірсутектердің галоген туындылары: изомериясы, химиялық қасиеттері және алу әдістері


М. Өтемісов атындағы Батыс Қазақстан мемлекеттік университеті
КУРСТЫҚ ЖҰМЫС
Тақырыбы:
«Ароматты көмірсутектердің галоген туындылары»
Орындаған: Сартаева А. Р.
Тексерген:
Орал, 2017ж.
Мазмұны
Кіріспе . . . 3
1. Ароматты көмірсутектер (арендер)
1. 1 Көмірсутектердің галогентуындыларының изомерлері мен атаулары . . . 5
1. 2 Бензолдың жалпы формуласы. Гомологтық қатары . . . 8
1. 3 Химиялық қасиеттері . . . 10
1. 4 Бензол сақинасындағы бағытталу ережесі . . . 13
2. Көмірсутектердің галоген туындылары.
2. 1 Изомериясы. Номенклатурасы. Физикалық қасиеттері . . . 15
2. 2 Көмірсутектердің галоген туындыларын алу . . . 19
Қорытынды . . . 21
Әдебиеттер тізімі . . . 23
Кіріспе
Ароматты көмірсутектердің басты өкілі-бензол. Оны 1825 ж. М. Фарадей жарық газын зерттей отырып, соның құрамынан тапқан, ал Э. Митчерлих 1834 ж. бензой қышқылын құрғақ айдау арқылы алған.
Кекуле 1865 ж. бензолдың циклді формуласын ұсынды. Кекуле бойынша бензол молекуласы қосыаланған үш байланысы бар циклогексатриенді тұйық жүйе.
Органикалық қосылыстардың негізі етіп көмірсутекті алады да, қалған қосылыстарды, олардың туындылары ретінде қарайды. Көміртек тізбегінің құрылысына қарай органикалық қосылыстар ашық тізбекті (алифаттық) және циклді (тұйық) қосылыстарға бөлінеді.
Тұйық тізбекті қосылыстар екіге бөлінеді : карбоциклді және гетероциклді.
Карбоциклді қосылыстардың тұйық тізбегі тек көміртегі атомынан тұрады және сонымен бірге алициклді және ароматты болып екіге бөлінеді.
Гетероциклді қосылыстардың тұйық тізбегі көміртегі мен сутегі атомдарымен қоса басқа да атомдардан құралады. Гетероциклді қосылыстар түзуге көбінесе азот, күкірт, оттегі атомдары қатысады.
Органикалық қосылыстар құрамы мен құрылысына байланысты кластарға бөлінеді.
Ароматты қатардың ең қарапайым өкілдері - көмірсутектер.
Егер көмірсутектердегі сутегі атомдарын басқа атомдарға не атомдар топтарына - функциональды топтарға - ауыстырса, сол қатардың басқа кластары пайда болады.
Органикалық қосылыстар кластарының химиялық өзгерістері бағытын орын басқан атомдар мен функцинальды топтар анықтайды.
Орын басқан атомдары не функциональды топтары бірдей көмірсутектер және олардың туындылары гомологтық қатар түзеді. Сонымен, гомологтық қатарға құрылысы ұқсас, сондықтан химиялық қасиеттері де ұқсас, бір-бірінен СН 2 (метилен тобы - гомологтық айырмашылық) тобына айырымы бар заттар қатары жатады.
Органикалық қосылыстардың негізгі кластары:
1. Ароматты көмірсутектер (Ar - H) ;
2. Ароматты галогентуындылар (Ar - Hal) ;
3. Фенолдар және ароматты спирттер (Ar - OH) ;
4. Ароматты карбонильді қосылыстар - альдегидтер мен кетондар (Ar - CHO; Ar - CO - R) ;
5. Ароматты карбон қышқылдары (Ar - COOH) ;
6. Ароматты аминдер (Ar - NH 2 )
7. Ароматты нитроқосылыстар (Ar - NO 2 ) ;
8. Ароматты сульфоқосылыстар (Ar - SO 3 H) ;
Ароматты көмірсутектерге бір немесе бірнеше бензол сақинасы бар қосылыстар жатады. Бензол сақинасының саңына байланысты бірядролы (моноциклді) және көпядролы (полициклдер) деп бөлінеді.
Зерттеу жұмысының мақсаты: ароматты көмірсутектердің галоген туындыларын алу әдістермен танысу.
Зерттеу жұмысының міндетітері:
- ароматты көмірсутектердің галоген туындыларын алу әдістері туралы түсінік беру;
- Ароматты көмірсутектер қосылыстарының химиялық қасиеттеріне сипаттама беру.
Зерттеу құрылымы: кіріспеден, екі бөлімнен және қорытынды мен пайдаланылған әдебиеттер тізімінен тұрады.
1. АРОМАТТЫ КӨМІРСУТЕКТЕР (АРЕНДЕР)
1. 1 Көмірсутектердің галогентуындыларының изомерлері мен атаулары
Көмірсутектердің галогентуындылары - көмірсутек молекуласындағы бір немесе бірнеше сутек атомдарының орнын галоген атомдарына алмастырғанда түзілетін қосылыстар екендігімен таныссыңдар. Химиялық белсенді болғандықтан, галогеналкандар органикалық синтезде кең қолданылады. Галогенді қосылыс құрамындағы көміртек пен сутек арасындағы С - Н байланыс энергиясы көміртек пен галоген С - Гал (фтордан басқа) байланысының энергиясынан едәуір жоғары.
Көмірсутектердің химиялық байланыстардың энергиялары
Халықаралық атаулар жүйесі бойынша галогеналкандарды атау үшін көмірсутек тізбегі галоген жақын орналасқан жағынан бастап нөмірленеді. Галоген байланысып тұрған көміртектің нөмірі, галоген және көмірсутек аталады. Рационалды атау бойынша галогеналкилдердің аты көмірсутек радикалы мен галогеннен тұрады:
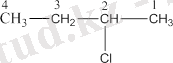
Галогеналкандардың изомерленуі көміртек қаңқасының құрылысы мен галогеннің орнына байланысты болады. Сондықтан бұлардың изомерлерінің саны сәйкес көмірсутектердің изомерлерінен көп болады. Изомерлену алкандарда С4 - бутаннан басталса, галогеналкилдердің изомерленуі С3-тен басталатынын келтірілген мысалдан көрдіңдер. Бромбутанның төрт изомері болады.
Галогеналкандардың физикалық қасиеттерінің өзгеру заңдылықтары алкандардың физикалық қасиеттерінің заңдылықтарына ұксас. Алкил радикал мен галогеннің массасы өскенде, галогеналкилдердің қайнау температуралары артады. Сан өзгерісінің сапа өзгерісіне ауысатындығына тағы да көз жеткіздіңдер. Галогеналкандардың бастапқы мүшелері газ тектес, ортаңғылары сұйық заттар. Өздеріне тән тәттілеу иістері болады. Галогеналкилдер суда нашар, органикалық еріткіштерде жақсы ериді.
Галогеналкилдер орынбасу, айырылу, тотығу реакцияларына түсе алады. Галогеналкилдердің галоген атомдарын басқа атом топтарына ауыстыруы, олардың маңызды реакциясы болып табылады. Осы реакциялар арқылы органикалық қосылыстардың басқа кластарына өтуге болады. Галогеналкил сілтінің судағы ерітіндісімен әрекеттескенде спирт түзіледі:
С2Н5Сl + NaOH --> С2Н5ОН + NaCl
Айырылу (ыдырау) реакциялары. Галогеналкилдерге сілтілердің спирттегі ерітінділерімен әсер еткенде, галогенсутек бөлініп, қанықпаған көмірсутектер түзіледі:
а) егер галогеналкилдің құрамында галогеннің бір атомы болса, алкен түзіледі. Бұл реакция теңдеуін алкеннен галогеналкилдерді алу әдісімен салыстырып, реакцияның қайтымдылығы жөнінде қорытынды жасаңдар. Қандай жағдайлар тепе-теңдікті этиленнің түзілу жағына карай ығыстыратынын айтыңдар. Мысалы:
Н3С - СН2Сl + NaOH -спирт-> Н2С=СН2 + NaCl + Н2O
ә) егер сілтінің спирттегі ерітіндісімен дигалогентуындылар әрекеттеесе, ацетилен қатарының көмірсутектері түзіледі:
СНСl2 - CH3 + 2КОН -спирт-> НС=СН + 2KCl + 2Н2O
Вюрц реакциясы металл натрий қатысында жүреді, реакция нәтижесінде алкандардың көміртек саны көбірек гомологтарын алуға болады.
Галогеналкилдер жоғарғы алкандарды, қанықпаған көмірсутектерді және спирттерді алғанда, аралық заттар ретінде кеңінен қолданылады.
Органикалық заттардың хлортуындылары улы химикаттар болып табылады. Өсімдіктер мен жануарлар зиянкестерімен күресуге қолданылатын заттарды пестицидтер деп атайды. Олардың ішінде инсектицидтер деп өсімдіктерді зиянкес жәндіктерден қорғайтын заттарды, гербицидтер деп арамшөптермен күресте қолданылатын заттарды, ал фунгицидтер деп саңырауқұлақ ауруларымен күресетін заттарды атайды. Мысалы, гексахлорбензол С6Н6Сl6 дәнді дақылдарды зиянкестерден қорғауға пайдаланылады.
Кейбір хлорорганикалық заттар коршаған ортада ондаған жылдар бойы бұзылмай сақталуы мүмкін. Олар сумен араласып, қоршаған ортаға таралады. Суда нашар ерігенмен, майда жақсы еритіндіктен, жануарлар (балық, құс, т. б. ) организмдеріне жиналады
1. 2 Бензолдың жалпы формуласы. Гомологтық қатары.
Бензол және оның туындыларының өздеріне тән ерекше қасиеттері бар.
1. Ароматты көмірсутектердің молекуласында алты π-электрондардың біртұтас тұйық электрондық система құруы-ароматикалық қасиеттің басты белгісі. Бұл бензол және оның гомологтарының физикалық және химиялық қасиеттерін анықтайды.
2. Ароматты көмірсутектер тотықтырғыштардың әрекетіне тұрақты.
3. Ароматты көмірсутектер қосылу реакциясына қиын түседі, ал электрофильді орынбасу реакциясына оңай түседі.
Ароматты көмірсутектер (арендер) деп - молекуласында циклогексатриендік цикл бар, физикалық және химиялық қасиеттерімен ерекшеленетін көмірсутектерді атайды. Ароматты қосылыстардың барлығына циклдік құрылыс және жоғары қанықпаушылық тән. Жалпы формуласы: С n H 2n-6 . Ароматты көмірсутектердің қарапайым өкілі - бензол- С 6 Н 6 . Бензол молекуласында көміртек пен сутек атомдары бір жазықтықтың бойында орналасқан. Көміртек атомдар арасындағы барлық байланыстардың ұзындығы бірдей - 1, 4 А 0 , байланыстар арасындағы бұрыш 120 0 тең болады. Бензол молекуласы С 6 Н 6 . Бензолдың қарапайым моноорынбасқан туындыларын атау үшін, «бензол» деген сөздің алдында орынбасарды атайды.
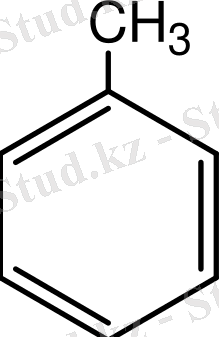
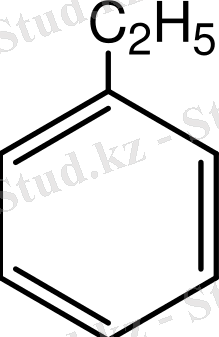
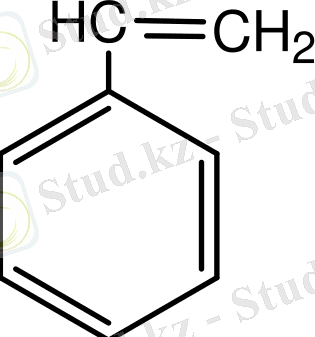
Бензолдың кейбір орынбасарлы туындыларын тривиалдық атаулармен атайды. Мысалы: метилбензол - толуол С 6 Н 5 СН 3 ; аминобензол - анилин С 6 Н 5 NH 2 , винилбензол стирол С 6 Н 5 С 2 Н 3
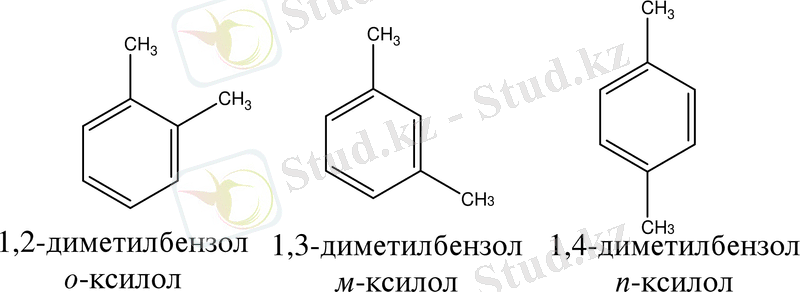
Екі орынбасарлы бензолдар. Бензол сақинасында екі орынбасар болса, оларды атағанда, орынбасардың тұрған орнын да көрсету қажет. Үш мүмкін изомерлерді орто- мета-, пара- (қысқаша о-, м-, n-) деп белгілейді.
Егер екі орынбасар көрші көміртегі атомдарында қатар орналасса, ондай изомерді орто- о-изомер дейді.
Егер орынбасар бір көміртегі атомынан кейін орналасса, ондай изомерді мета- м-изомер дейді.
Егер орныбасар екі көміртегі атомынан кейін орналасса, ондай изомерді пара- n-изомер дейді.
1. 3 Химиялық қасиеттері
Барлық ароматты көмірсутектер орынбасу реакциясына бейімді, ал қосып алу реакциясына өте қиын түседі. Арендер галогендеу, нитрлеу, сульфирлеу реакцияларына, ал гомологтары тотығу реакциясына қатысады. Бензол сақинасында π-электрон бұлттары бір келкі таралғандықтан нуклеофильдік реакциялар қиын, ал электрофильдік орынбасу реакциялары оңай жүреді.
1. Нитрлеу реакциясын жүргізу үшін, концентрлі азот пен күкірт қышқылдарының қоспасын алады. Бұл нитрлейтін агент нитроний ионын NO 2 + береді.
НО - NO 2 + 2H 2 SO 4 ↔︎ NO 2 + + H 3 O + + 2HSO 4 -
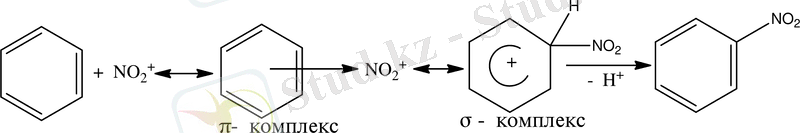
Электрофильдік орын басу реакциясы екі сатыда жүреді. Алдымен электрофильдік топ бензол сақинасының π- орбитальдарын шабуылдап, π- комплекс түзеді. Екінші сатыда π- комплекс, тұрақсыз σ- комплекске өтеді. Содан кейін пайда болған тұрақсыз карбокатионнан протон бөлініп, нитробензол түзіледі.
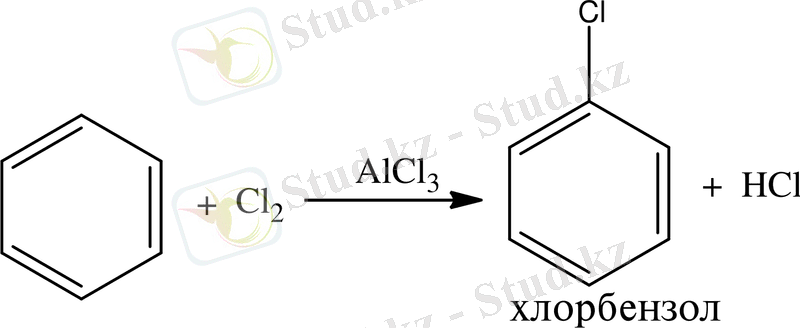
2. Галогендеу реакциясы. Бензол және оның гамологтары хлорланады, бромданады, иодталады. Реакция жүру үшін галогенді полярлайтын катализатор қажет: темір немесе алюминий галогенидтері.
3. Сульфирлеу реакциясы (күкірт қышқылын қосу) :
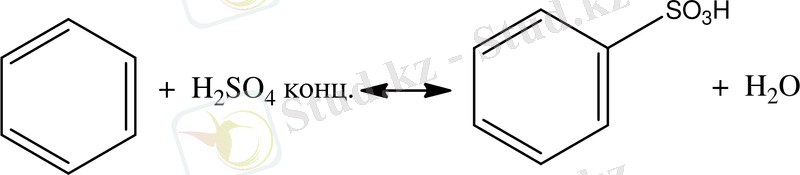
бензолсульфоқышқыл
4. Алкилдеу реакциясы. Бензол сақинасына алкил тобын енгізу үшін бензолды галогеналкандармен әрекеттестіреді.
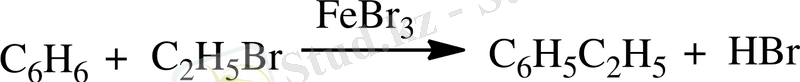
этилбензол
Реакция тек катализатор қатысында жүреді. Катализатор ретінде алюминий хлориді немесе темір (III) бромиді қолданылады. Бұл катализатордың тиімділігін бірінші рет Фридель мен Дж. Крафтс ашқандықтан, мұндай реакцияларды Фридель-Крафтс реакциялары деп атайды.
5. Фридель - Крафтс реакциясы бойынша ацилирлеу - молекулаға ацил тобын енгізу. Ацилирлеу процесін Льюис қышқылы қатысында карбон қышқылдарының жүргізеді.
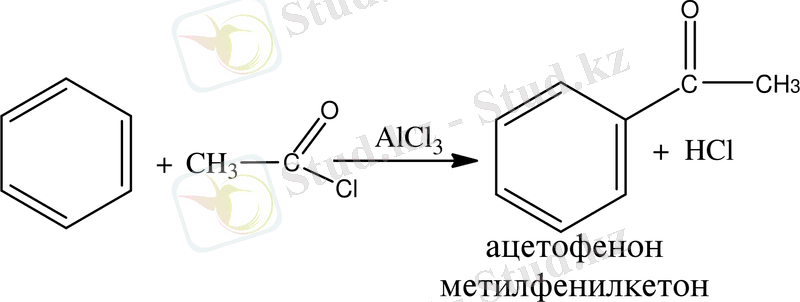
6. Тотығу реакциясы. Қалыпты жағдайда мына тотықтырғыштар - азот қышқылы, хром қоспасы, калий перманганаты, сутегі пероксиді - бензолға әсер етпейді. Тек жоғары температурада, ванадий (V) оксиді қатысында бензол ауамен малеин ангидридіне дейін тотығады.
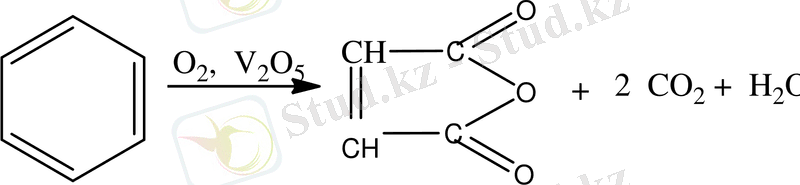
малеин ангидриді
Бензол гомологтарын катализатор (КМnO 4 , К 2 Сr 2 О 7 ) қатысында тотықтырса, ароматты қышқылға айналады.
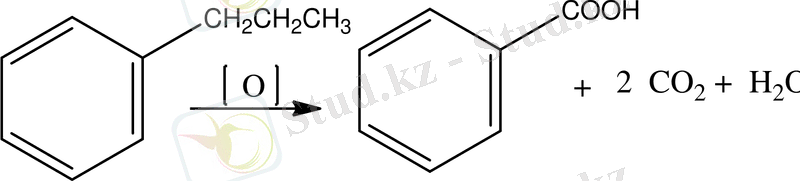
пропилбензол бензой қышқылы
Бензол молекуласы озонды қосып алып, алдымен триозонид түзеді, ол су әсерінен бұзылып, глиоксаль-диальдегид түзеді, сосын дикарбон қышқылы түзіледі.
.
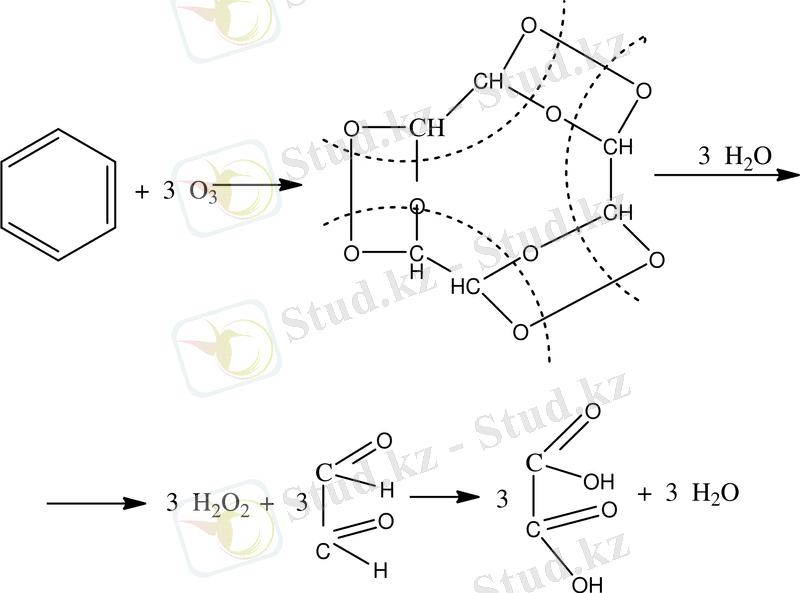
глиоксаль қымыздық қышқылы
1. 4 Бензол сақинасындағы бағытталу ережесі
Бензол сақинасындағы барлық көміртегі атомдары бір - бірімен тең, сондықтан электрофильді агенттер сақинадағы кез келген көміртегі атомын шабуылдайды. Егер бензол сақинасында бір орынбасар болса, онда келесі жаңа орынбасар белгілі орынға ие болады. Бензол қатарындағы көмірсутектердің электрофильдік орын басу реакциялары орынбасардың химиялық табиғаты және бағыттаушы қабілеті бойынша екі топқа бөлінеді.
1. о-, n- бағыттаушы орынбасарлар бірінші текті орынбасарлар (ориентанттар) деп аталады. Олар электрон беруге (электрондонорлар) бейім топтар: алкил ( -СН3, -СН2R), галогендер жатады, тағы - ОН, -NH2, - NHR, - NR2, -ОН, OR, - NHCOR, -OCOR, -SH.
2. м- бағыттаушы орынбасарлар екінші текті орынбасарлар (ориентанттар) деп аталады. Олар электрон қабылдауға (электрон акцепторлы) бейім топтар: - CF3, - NO2, - SO3H, - COOH, - CN, -COR, -COOR, -CCl3 жатады.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz