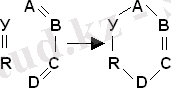
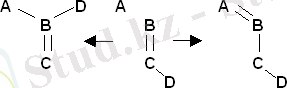
Ерітінді түзілуінің термодинамикасы мен молекулалы-кинетикасы: орынбасушы әсерлері және Гаммет-Тафт кореляциялық теңдеулері


Ерітіндінің алынуының термодинамикалық және молекулалы- кинетикалық жағдайы.
Компоненттерден алынған ерітінді - өзіндік деп аталады. Ол барлық өзіндік процестер сияқты екі сыртқы жағдайға сүйенеді (Р және Т), ∆G<0. Термодинамикалық процесс арқылы ерітінді түзілгенге Гиббс энергиясы шөгеді. Мұндай процесс өзінен өзі жүре береді, толық теңдік орнамағанша: ерітілген компонент (m, ж, г) ↔︎еритін компонент (ерітінді) ∆G=0 шамасында. Толық ерітінділер ғана бұл процеске кірмейді. Термодинамикалық заңдылық бойынша толық ерітінді деп - таза ерітіндінің химиялық потенциалы сол ерітіндінің еріген зат құрамындағы химиялық потенциалына тең шамасын айтамыз.
Егер сұйық ерітінді қатты заттың еруінен алынса, онда кинетика заңы бойынша ерітінді толық болады. Мына жағдайда: егер қатты заттың бетінен балқытылғанда алынған жылдамдық еріген заттың жылдамдығына тең болған жағдайда. Молекулалы-кинетикалық жағдай диффузия құбылысы арқылы жүзеге асады. Осы құбылысқа байланысты ерітінділерде мынадай қасиеттер байқалады: электроөткізгіштік, созылыңқылық, жылуөткізгіштік және тағы басқалары.
Бөліктердің ерітінді ішінде әртүрлі ауқымды ауысуына энергия өте қажет, энергия алғашқы күйден жаңа күйге ауысу үшін таптырмас қайнар көз. Қандай да болмасын ерітінді пайда болу үшін ерітінді құрылымы өзгеруі тиіс.
Кей сұйық ерітінділерді кристалды құрылым болады. кәдімгі сұйық су үшін ең көп тараған құрылым мұзтектес модель жатады, оны бізге О. Я. Сомайлов ұсынған. Бұл модельге қарасақ, су жылудан бұзылатын мұзтектес каркастан тұрады, оның бас құрамы су молекуласы бос құрам ішінде немесе мұзтектес каркас түйінінде энергетика жағынан біртектес емес. Сұйық судың молекуласы үздіксіз қозғалыста болады, ал қозғалыс мұзтектес каркастың бұзылуына және молекуланың су ішінде өзгеруіне әкеліп соғады. Сұйық ерітінді пайда болғанда, яғни таза ерітіндіге еритін зат қосылғанда, жаңа құрылымдық бөлік пайда болады. Бұл кезде молекулааралық күш те өзгеріске ұшырайды.
Органикалық қосылыстардың арасындағы құрылымдық байланыспен реакциялық бейімдеушілік.
Корреляциялық теңдіктер.
Осы тақырыпқа байланысты сұрақ теориялық химияның ең негізгі сұрақтары болып келеді. Реакциялық бейімдеушілік жылдамдық коснтантымен және теңдік константымен, сонымен қатар қышқылдық коснтантымен өрнектеледі. Қышқылдық константы органикалық қышқылдықтың құрылымына тәуелді болып келеді және олар әртүрлі қышқылдыққа құйылған заттармен де өрнектеледі. Негізінен жиірек констант қышқылдары карбон қышқылының функциональды реакцияның бейімдеушілігін бағалау үшін қолданады.
Гаммет теңдігі. Гамметтің бақылауы бойынша, белгілі бір қышқылдықтың қышқылдық шамасын арттырғанда жылдамдық константы күрделі алхимерді эфирлерде артады.
Реакциясы RCOOCH 3 + (CH 3 ) 3 N→RCOO - (CH 3 ) 4 N + 1935 жылы Гаммет, константы реакциялы бейімдеушілік м және n-бензой қышқылының арасында байланыс бар екенін табады. Бұл байланыс мына теңдік арқылы өрнектеледі (1937) .
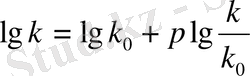
мұндағы, к-бензой қышқылындағы бензой цикліндегі қышқылдық констант. k-бензолдың константты реакциялық бейімдеушілігі. k
0
, k
0
- орын алмаған байланыс константтары, р-реакциялы бөлімнің константы
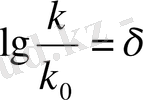 белгісінде Гаммет теңдігін аламыз.
белгісінде Гаммет теңдігін аламыз.
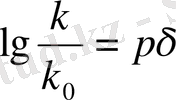 .
.
Бұл теңдік біртипті байланыста вариациалы өтуде биіктік өзгерісін lgk - lgk
0
(немесе
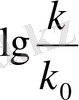 ) көрсетеді.
) көрсетеді.
Гаммет константы. Гаммет теңдігі екі үлкен шама көрсетеді - р және σ. Реакцияның константы сол реакцияны көрсетеді, реакция түрі сондықтан константты реакция бөлімі деп аталады.
Констант σ молекула құрылымының жерін көрсетеді - топтау немесе орынбасу жерін көрсетеді. σ - орынбасу константы болып табылады, сондықтан оны Гаммет константы деп атаймыз. Гаммет теңдігін қолдану үшін, стандартты биіктік шамасын таңдау қажет. Стандартты шама үшін, σ нолге тең болғанда Гаммет сутегі атомын таңдады. Бензой қышқылдарының ионизация реакциясында р=1. Осыдан келе σ-констант орынбасуының бірінші шкаласы алынды. lg k және σ кәдімгі күйдегі тәуелділігі графикалық координатада
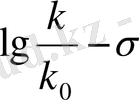 түрінде беріледі. Түзудің тангенс бұрышы, эксперименталь нүктелері арқылы жүргізілген, р константына сәйкес келеді. Орынбасушылар үшін 0=, m- және n-констант Гамметте әртүрлі сандық мәндерді және белгілерді білдіреді. Мысалы, OH
σM
=+0. 12, σ
n
=-0. 37, NH
2σM
=-0. 16, σ
n
=-0. 66, NO
2σM
=+0. 71, σ
n
=+0. 78 топтарына тең.
түрінде беріледі. Түзудің тангенс бұрышы, эксперименталь нүктелері арқылы жүргізілген, р константына сәйкес келеді. Орынбасушылар үшін 0=, m- және n-констант Гамметте әртүрлі сандық мәндерді және белгілерді білдіреді. Мысалы, OH
σM
=+0. 12, σ
n
=-0. 37, NH
2σM
=-0. 16, σ
n
=-0. 66, NO
2σM
=+0. 71, σ
n
=+0. 78 топтарына тең.
Гаммет коснтантында қолданылған «+» таңбасы орынбасушылардың электронды акцептораралық әсерлермен көрсетеді. Сандық таңбалар орынбасушылардың электронды әсерлерін көрсету үшін қолданылады.
Гаммет константы орынбасушылардың сандық электронды әсерлерін көрсетеді.
0=, M= және n - бұл көрсеткіштердің әсерлері әртүрлі. σ 0 константы бар жерлерді есепке ала отырып, олардың біз практикалық түрде қолданылуын сирек көреміз, себебі кеңістіктегі орта эффект әсері бір реакциядан екінші реакцияға өткенде ауысады.
σ M негізінен индуктивті әсердің санын және мезомерлі әсерін көрсетеді. Индуктивті әсер мен мезомерлі әсер бір-біріне бағыттары бойынша қарама-қарсы болулары мүмкін. Ол σ - констант топтарын OH және NH 2 М- және n- үшін нақты көрсетіледі.
Реакциялы бөлімдердің константы реакциялы бөлімдердің константтары р оңды және теріс нәтижелі көрсетулері мүмкін, теріс нәтижелері көбінесе -4-тен +4-ке дейінгі интервалда болады. Констант таңбасы электронды әсердің реакция болуын көрсетеді. Егер р>0, . онда реакцияны электронакцепторлы әсерлер жылдамдатады, ал егер р<0 реакцияға электрондонорлы әсерлер түседі.
Гаммет константы шектеулі қолданыста болады, себебі олар әсерлердің индуктивтік және мезомерлі қасиеттерін көрсетеді, ал реакция әсеріне бұл құбылыстар әр түрлі әсер етеді, әсіресе n-кезінде.
Гаммет - Браун константы мезомерлі әсері бар реакциялар өте қатты реакциялар болып табылады, сондықтан оларға жай σ n константы жарамсыз келеді.
Бұған мысал, n-тектес фенол ионизациясы бола алады.
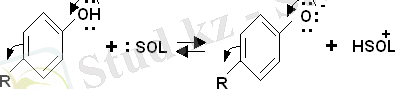
(мұнда R=NO 2 , COR + , C=N, N 2 + )
Бұл кезде R-ң жаңа үлкейтілген константын қолдану керек, тікелей полярлы констант түрін σ-ны қолдану керек.
Электронжонордың орынбасушысының тікелей полярлы қасиеті арқылы реакция ортасына карбкатиондар мысал бола алады.
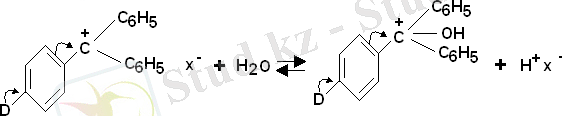
(мұнда D=OR, SR, NR 2 )
Электрондонорлы орынбасушысының тікелей полярлы D ¨- сы σ + болып белгіленген. σ - және σ + константтарын экспериментальды дәлелдеп ұсынған Браун Окомото (1957 ж) .
Абсолюттік шамасынан олар Гаммет константынан үлкен болып келеді. Мысалы: NH 2 тобы үшін σ n =-0. 66, ал σ n =-1. 3, NO 2 тобы үшін σ n =+0. 78 σ n =+1, 27.
Тафт константы.
σ - ң Р. Тафт сынау үшін орынбасушылардың алфавиттік қатарындағы индуктивті константын ойлап тапты. Осы мақсатта ол гидролиздердің күрделі эфирдегі жылдамдығын Х-COOR қышқылды ортадағы әсерін оқып және σ* константтардың Х тобындағы әсерін алды. Қосылыстарды салыстыру үшін ол, сірке қышқылын алды, оған σ*
CH2
=0-ді қолданды. Тафт бір көміртегі атомы арқылы әлсіреу коэфициентін индуктивті әсерін
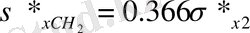 осы түрінде есептеп шығарды. σ* индуктивті орынбасушы әсердің биіктігі мен бағытын анықтайды. Мысалы: σ*
F
=+3. 1,
осы түрінде есептеп шығарды. σ* индуктивті орынбасушы әсердің биіктігі мен бағытын анықтайды. Мысалы: σ*
F
=+3. 1,
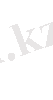 Equation. 3
Equation. 3
Тафт константы Гаммет константына ұқсас келеді:
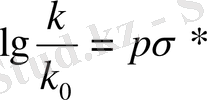 .
.
Орынбасушы әсерлерінің бөліну мәселесі.
Сызықты өзгерудің бас энергиясын білу үшін әсерлерді негізгі топтарға (индуктивті, мезомерлі, кеңістіктік) болу қажет және әр жерді өз константы арқылы өрнектеу керек. Мұны істеуге болады. Бүгінгі күні орынбасушылардың көп түрлі константары белгілі.
σ - Гаммет константы.
σ + , σ - - Гаммет-Браун константы.
σ* - Тафт константы.
Е S - кеңістік әсері константы.
σ 1 - өндірілген бензолдың индуктивті константы (σ 1 =0. 16σ*) .
σ C - орынбасушының мезомерлі әсерін анықтау константы (σ С =σ-σ 1 ) және т. б.
6-кестеде әртүрлі орынбасушылардың σ-константтары берілген.
6-кесте. σ - орынбасушы коснтанттары.
CH 3
F
Cl
OH
NH 2
N(CH 3 ) 2
COO CH 3
CN
NO 2
-0. 17
0. 06
0. 23
-0. 37
-0. 66
-0. 83
0. 46
0. 65
0. 78
-0. 31
-0. 07
-0. 4
-0. 02
-1. 3
-1. 7
-
-
-
-
-
-
-
-
-
0. 64
0. 88
1. 27
-0. 07
0. 34
0. 37
0. 12
-0. 16
0. 211
0. 315
0. 56
0. 71
-0. 14
0. 25
0. 2
-0. 3
-0. 35
-
-
-
0. 8
-
0. 52
0. 47
-
0. 10
-
0. 32
0. 58
-
0. 63
0
3. 1
2. 68
1. 31
0. 72
-
1. 75
3. 25
-
3. 53
Корреляциялы теңдіктердің қолданылуы.
Теңдіктер, яғни константтарды реакциямен және басқа физикалық константтарды орынбасушы константтармен байланыстыратын теңдіктер - корреляциялы теңдіктер деп аталады. Мұндай теңдіктердің ең қарапайымы Гаммет теңдеу болып табылады.
Корреляциялы теңдіктерді жаңа реакция топтары үшін, реакция механизмін анықтау үшін, жаңа атом топтарының электронды әсерін өрнектеу үшін, жаңа органикалық қосылыстардың реакциялы қабілетін білу үшін пайдаланылады. σ - константтары электронды және басқа да әсерлерді жартылай сандық өлшем енгізу қажет.
Реакция түрлері және реагенттер.
Реакция классификациясы химиялық ауысу қасиетінде және молекуладағы үзілу байланысы арқылы өткізіледі.
Химиялық ауысу қасиеті бойынша реакциялар былай топталады:
- бір электронды ауысу (бір электронды қышқылдық - қайта өңделу реакциясы) : D: + A → D∙ + A-∙
- диссоциация және рекомбинация: А - В ↔︎ А+В
- орын ауысу R-X+A→ R-A+X
- ажырау: У-R-A→У=R+A-B
B
- қосылу: У=R+A-B→У-R
B A
- циклоқосылу:
Циклоқосылу реакциясы деп - бір циклді аддукт негізінде қосылып, құрамында бір немесе екі молекула болатын, құрамында кішірейетін орын бар реакциясы. Перециклді немесе көп салалы болуы мүмкін.
- Изомерация немесе топтау реакциясы (қысқа байланысты, атом немесе топ миграциясы, циклдің тоғысуы) .
Бірінші реакциялардан басқаларының бәрінде химиялық байланыс орнайды а және б түріндегі реакциялар элементарлы акт құрайды. Орынбасу, қосылу, ажырау, изомеризация және топтау реакциялары аса қиын болып табылады.
Химиялық үзілу байланыс реакциясына орай төмендегіше топтасады:
- гомометикалық (бос радикальды механизм)
A : B ↔︎ A ∙ +B
- гетерометикалық (ионды механизм)
A : B ↔︎ [A:] - + [B] +
бір электрлі өткізгіш реакциясы өзіндік гибрид болып табылады. Оларда ион-радикалы құрылады, олар алдағы уақытта ионмен және бос радикалмен қатынас жасайды. Әдетте ион-радикал реакциясы гомометикалық реакция болып табылады.
- перециклді реакциялар - реорганизациялы байланыс ұйымды түрде циклді қалыптасу арқылы атомдармен байланысты болады.
Перециклді реакцияларға циклоқосылу реакциясының бөлігі және кейбір молекулалы топтар, электроциклді реакциялар және сигмотропты топтар кіреді.
Электроциклді реакциялар δ-байланыс пен π - электронды жүйені құрады.
және қайтымды процесс.
Гетерометикалық реакцияларда әртүрлі реагенттер болады: иондар полярлы молекулалар.
Иондар әртүрлі болуы мүмкін.
Ковалентті байланыс кезінде контактті (тар) ионды жұп түзіледі:

Контактты ионды жұп әртекті зарядталған ион түзеді, ковалентті байланыссыз кулонды қасиет арқылы жүреді. Мұндай ионды жұп өзін біртұтас дене деп танылады.
Контактты ионды жұп ерітінді (Sol) молекуласымен қосылып, бос ионды жұп құрайды:
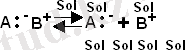
Нәтижесінде ерітіндіде бос ион пайда болады, ерітінділердің электросулылығы ұлғаяды.
Қышқылды және негіздік концепциясы.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz