Карбамидтер мен олардың функционалдық туындылары: синтез әдістері, изоцианаттар мен моноэтанол винил эфирімен реакциялары және физико-химиялық сипаттамасы


МАЗМҰНЫ
бет
КІРІСПЕ . . . 3
1 КАРБАМИДТЕР, ОНЫҢ НЕГІЗГІ ФУНКЦИОНАЛДЫ ТУЫНДЫЛАРЫ
1. 1 Карбамид . . . 5
1. 1. 1 Карбамидтерді аминдер мен цианаттардан алу . . . 9
1. 1. 2 Карбамидтерді аминдер және органикалық изоцианаттардан алу . . . 10
1. 1. 3 Карбамидтерді аминдер мен фосгеннен алу . . . 10
1. 1. 4 Карбаматтар және карбонаттар аммонолизі . . . 11
1. 1. 5 Карбамидті ацилдеу . . . 11
1. 1. 6 Карбамидті алкилдеу . . . 12
1. 2 Карбаматтар . . . 13
1. 3 Уреидтер . . . 14
2 АЗОТТЫ ОРГАНИКАЛЫҚ ҚОСЫЛЫСТАР
2. 1 Аминдер . . . 21
2. 2 Аминоспирттер . . . 25
2. 3 Винил эфирлері . . . 26
2. 3. 1 Моноэтаноламин винил эфирі және оның қасиеттері . . . 26
2. 4 Амидтер . . . 31
2. 4. 1 Амидтер реакциялары . . . 31
2. 4. 2 Көмір қышқылының амиді . . . 33
2. 5 Изоцианаттар . . . 34
3 ЗЕРТТЕУ НӘТИЖЕЛЕРІ МЕН ТАЛҚЫЛАУЛАР
3. 1 Изоцианатты қосылыстар мен азотты органикалық қосылыстар арасындағы реакцияларды зерттеу . . . 43
3. 2 Циклогексилизоцианат пен моноэтанол винил эфирі арасындағы
реакция . . . 43
3. 3 3-Хлорфенилизоцианат пен моноэтанол винил эфирі арасындағы
реакция . . . 44
4 ЭКСПЕРИМЕНТТІК БӨЛІМ
4. 1 Бастапқы химиялық реагенттердің физико-химиялық сипаттамасы… . . . 46
4. 2 Алынған заттардың физико-химиялық сипаттамасы . . . 50
4. 3 Изоцианаттар мен моноэтанол винил эфирі синтезі . . . 51
4. 5 Моноэтаноламин винил эфирін тазарту . . . 54
ҚОРЫТЫНДЫ
ҚОЛДАНЫЛҒАН ӘДЕБИЕТТЕР ТІЗІМІ
ҚОСЫМШАЛАР
КІРІСПЕ
Органикалық химия саласында карбамидті қосылыстар маңызды орын алады. Ең бірінші карбамидті қосылыстарды Велер калий цианаты аммоний сульфатымен әрекеттетстіріп, пайда болған аммоний цианатын қыздыру арқылы алған.
Карбамид - көмір қышқылының амиді. Молекуласындағы сутек атомдары қышқыл радикалдарымен орын басу арқылы түзілетін карбамидтің туындыларын уреидтер деп атайды [1] .
Дипломдық жұмыстың мақсаты: ғылыми зерттеу жұмысы барысында карбамидті қосылыстар қатарына жататын биологиялық белсенді қасиет көрсететін, әр түрлі туындыларын синтездеудің жаңа, тиімді әдістерін игеріп, физикалық және химиялық қасиеттері мен құрылыстарын инфрақызыл спектроскопиялық анализі арқылы зерттеу.
Дипломдық жұмыстың міндеті: Жұмыстың мақсатына жету үшін алға қойылған міндет:
- алынған барлық қосылыстардың физико-химиялық қасиеттерін анықтау.
Дипломдық жұмыстың теориялық және тәжірибелік маңызы:
Карбамид реакциялық қабілеттілігі жоғары қосылыс болып табылады, ол көптеген қосылыстармен бірге комплекстер түзеді. Карбамидтің қабілеттілігі алкандармен комплекс түзіп, мұнайдың депарафинизациясында қолданылады.
Карбамидті қосылыстар қышқылдармен әрекеттескенде тұздар түзеді. Алкилдеген кезде алкилкарбамид түзіп, спирттермен әрекеттескенде уретандар, ацилдегенде - уреидтер (N-ацилкарбамидтар) түзеді. Ацилдеу реакциясында гетероциклді қосылыстарды синтездеуде кең қолданылады. Карбамид формальдегидпен оңай конденсацияланып, ол шайыр өндіруде кең қолданылады.
Карбамидтің химиялық қасиеттері оның химиялық өндірісінде карбамид-альдегидті (ең бірінші карбамид-формальдегидті) шайыр синтезінде кең қолданылады, ағаш-талшықты плиталар және жиһаз өндірісінде кең қолданылады. Карбамидтің туындылары - тиімді гербицидтер. Олар дәнді-дақылдардың өсуіне кедергі келтіретін арам шөптерді жоюға қолданылады.
Карбамид - бұл минералды тыңайтқыш, кез келген дақылдар үшін топырақтың барлық түрінде қолданылады. Басқа азотты тыңайтқыштарға қарағанда карбамидте азоттың үлесі жоғары (46, 2%), негізінде кез келген топырақта көптеген ауыл шаруашылық өндірісінде тыңайтқыш ретінде оның экономикалық тиімділігі жағынан қолданылады.
Нитрозокарбамидтер туындыларды фармакология саласында ісікке қарсы дәрі-дәрмек ретінде қолданылады [2] .
Дипломдық жұмыс барысында алғаш рет кейбір изоцианаттардың моноэтанол винил эфирлерімен арасындағы реакция зерттелді.
Циклді изоцианаттардың моноэтанол винил эфирі арасында реакциясы изоцианитке карбамид тобына жатады, олардың жаңа функционлды туындылары синтезделінеді. Алынған жаңа мономерлердің физико-химиялық қасиеттері сипатталынады.
Ғылыми әдебиеттерге сүйене отырып, ол қосылыстардың бір-бірімен әрекеттесу реакцияларының жүру механизмі қарастырылады.
1 КАРБАМИДТЕР, ОНЫҢ НЕГІЗГІ ФУНКЦИОНАЛДЫ ТУЫНДЫЛАРЫ
1. 1 Карбамид
Карбамид - көмір қышқыл диамиді. Карбамидті алу барлық өнеркәсіптегі тәсілдері оның аммиактың көміртек диоксидімен реакциясында (200°С температураға жуық, 200 атм. және одан да жоғары қысымда) негізделген, сондықтан карбамидті өндіруде көбінесе аммиакты өндіріспен бірге жүреді.
Карбамидке әбден қанағатты сапалық реакциялар жоқ, ол кристалдардың балқу темпераурасы, CuSO 4 (сілтімен), AgNO 3 , с Рb(NO 3 ) 2 кері реакцияда, Шифф реакциясы және қыздырғанда биуреттің пайда болуынан білуге болады, ал оның ерітінділері - күшті HNO 3 (NaCl көп мөлшерінде болмауы да мүмкін), Нg(NO 3 ) 2 (саркозин немесе гидантонин қатысында болмайды) тұнбаларының түзілуінен, түссіз газ түзіліп, NaBrO немесе азотты қышқыл әсерінен ыдыратқанда және Люди реакциясы нәтижесінен білуге болады. Шифф реакциясы фурфуролдың концентрлі сулы ерітіндісінің бірнеше тамшысымен және HClAq тамшыларымен карбамидке әсер еткеннен тұрады. Мұнда карбамид сары түс береді, одан жасыл, көк, күлгін және қошқыл түстерге өтеді. Карбамидтің спирттік ерітіндісіне ортонитробензой альдегидін қосып, қыздырғанда карбамидтің о-нитробензилиденди ақ тұнбасын береді ((1, 2) - C 6 H 4 (NO 2 ) CH[CNHCONH 2 ] 2 - 200° балқиды) . Тұнбаны қайта кристалдау үшін өте аз болса, оны спиртпен бірнеше рет айдайды (әрекеттеспеген C 6 H 4 (NO 2 ) CОH толық жойылғанша) . Содан тұз қышқылды фенилгидразиннің күшті ерітіндісін, 5-10 тамшы 10% H 2 SO 4 қосып, қайнағанға дейін қыздырады. Соңында сұйықтық о- - C 6 H 4 (NO 2 ) CHNNH 2 С 6 Н 5 түзіп, қызыл түске боялу керек. Карбамидтің мөлшерлік анықтау әдістері Hg(NO 3 ) 2 ерітіндісімен тұнбаға түсіру және де бромлылау сілтімен, BaCl 2 мен Ва(ОН) 2 ерітіндісімен, азотты қышқылмен ыдырату тәсілімен негізделген [3] .
Карбамид молекуласы
- Химиялық айналулар бос радикалдарды қатыстырып, тізбекті реакцияларды құрайды. Сонда негізгі қарапайым әрекеті тізбекті жалғастыру реакциялары болып табылады, онда радикалдың бастапқы шикізат немесе өнім аралық молекулаларымен әрекеттесу нәтижесінде жаңа белсенді орталық пайда болады. Сонымен қатар бос радикалдар алмасу, айырылу және орынбасу реакцияларына түсе алады.
- Түзілген бос радикалдар бастапқы көміртек молекулаларымен кездесіп, олармен реакцияға түседі. Бос радикалдардың бастапқы көмірсутек молекулаларымен реакциясының жалпы нәтижесін шығару үшін біріншілік, екіншілік және үшіншілік сутек атомдар санын ескеру керек. Мысалы, пропан 6 біріншілік және 2 екіншілік сутек атомдары бар. Бос радикалдың біріншілік сутек атомымен жалпы салыстырмалы ықтималдық 6-ға тең, екіншілік сутек атомымен 4-ке тең.
- Кез келген сутек атомын бастапқы көміртек молекуласынан жұлып алу нәтижесінде алифатикалық радикал түзіледі, ол метил, этил және сутек атомының түзілуімен тез ыдырап кетеді. Соңғысы қайтадан бастапқы көмірсутек молекулаларымен әрекеттесіп, осылайша тізбекті реакцияны түзеді. Бос радикалдар бір-бірімен қосылып тізбек үзіледі [4] .
Химиялық қасиеттері. 150°С дейін қыздырғанда карбамид NH 4 NCO, NH 3 , CO 2 , биурет, цианур қышықылына айналады.
Қыздырылған карбамид ерітіндісіне аздап азотты қышқылды қосқан кезде азотты бөліп ыдыратады.
CO(NH 2 ) 2 + 2HNO 2 = CO 2 + 2N 2 + 3H 2 O
бромлылау қышқылы да сол сияқты әсер етеді:
CH 4 N 2 O + 3NaBrO = СО 2 + N 2 + 2H 2 O + 3NaBr
Сонымен қатар карбамид кейбір азотты органикалық қосылыстарымен әрекеттеседі (аналаинмен, толуидинмен, глицинмен, т. б. ) .
Реакциялық қабілеттілігі
1) Карбамидтің реакцияға түсу қабілеттілігі амидтер үшін типті: азоттың екі атомы да нуклеофил болып табылады, яғни карбамид күшті қышқылдармен тұздар түзеді, N-нитрокарбамидтерді түзіп нитрленеді, N-галогентуындыларды түзіп галогенденеді. Сәйкес N-алкилкарбамидтерді RNHCONH 2 түзіп, карбамид алкилденеді, альдегидтермен әрекеттесіп, 1-аминоспирттер RC(OH) NHCONH 2 туындыларын түзеді. Қатаң жағдайларда карбамид карбон қышқылдарының хлорангидридтерімен ацилденіп, уреидтерді түзеді (N-ацилмочевиналар) :
RCOCl + NH
2
CONH
2
 RCONHCONH
2
+ HCl
RCONHCONH
2
+ HCl
Карбамидтің дикарбон қышқылдары мен олардың туындыларымен (күрделі эфирлер) әрекеттесуі циклды уреидтерді түзуге әкеледі және гетероциклды қосылыстарды синтездеуге кең қоланылады; құмырсқа қышқылымен әрекеттескенде парабан қышқылын түзеді, ал малон қышқылдарын орын басқан эфирлер реакциясы - 1, 3, 5-үшоксипиримидиндерге - барбитур қышқылының туындылары, ұйықтататын дәрі-дәрмек ретінде кең қолданылады:
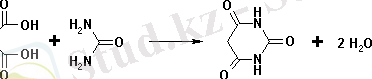
Сулы ерітіндіде карбамид аммиак пен көмірқышқыл газын түзіп гидролизденеді, сондықтан оны минералды тыңайтқыш ретінде қолданылуда қамтамасыз етіледі.
2) Карбамидтегі көміртектің карбонилді атомы әлсіз электрофилді, бірақ спирттер карбамидтен аммиакты бөліп шығара алады және де уретандарды түзеді:
NH
2
CONH
2
+ ROH
 NH
2
COOR + NH
3
NH
2
COOR + NH
3
Бұл реакциялар тобына карбамидтің аминдермен әрекеттесуі жатады, ол алкилкарбамидті түзеді:
RNH
2
+ NH
2
CONH
2
 RNHCONH
2
+ NH
3
RNHCONH
2
+ NH
3
гидразинмен реакциясында семикарбазид түзеді:
H
2
NNH
2
+ NH
2
CONH
2
 H
2
NNHCONH
2
+ NH
3
H
2
NNHCONH
2
+ NH
3
қыздырғанда биурет түзіледі: H 2 NCONHCONH 2
Өнеркәсіпте карбамид аммиак пен көмірқышқыл газынан Базаров реакциясы бойынша синтезделеді:
2NH 3 + CO 2 = NH 2 CONH 2 + H 2 O
Сондықтан карбамидті өндіруде амммиакты өндірісі бірге жүреді [5] .
Карбамид ірі мөлшерлі өнім болып табылады, негізінен азотты тыңайтқыш ретінде (азоттың мөлшері 46 %) қолданылады және түйіршіктелген түрде нығыздалып шығарылады. Карбамидті қолдану тағы да басқа маңызды өндірісі карбамид-альдегидті шайырлар синтезі болып табылады (ең бірінші карбамид-формальдегидті), жабысқақ түрінде ағаш-волокты плиталар (ДВП) және жиһаз өндірісінде кең қолданылуда. Карбамидтің туындылары - тиімді гербицидтер.
Сонымен қатар карбамид жылу электр станциялар, қазан, қалдықтарды жағып жою зауыттары, ішкі жану қозғалтқыштар, т. б. түтүндік газдарды азот оксидтерінен тазарту үшін қолданылады:
(NH 2 ) 2 CO + H 2 O → t° 2NH 3 + CO 2
3NO + 2NH 3 → N 2 + 3H 2 O
Карбамид E927b азық-түлік қосымшалары ретінде тіркелген. Шайнау сағызы өндірісінде қолданылады [6] .
Физикалық қасиеттері
Түссіз, иіссіз ақ кристалдар, кристалдық торы тетрагональды (а = 0, 566 нм, b= 0, 4712 нм, c = 2) ; полиморфты айналуларға шыдайды. Балқу температурасы - 132, 7°C, қайнау температурасы -333, 3°C. Тығыздығы - 1, 32 г/см. Суда ерігіштігі - 51, 8 (20°C) г/100моль.
Карбамид полярлы еріткіштерде жақсы ериді (су, сұйық аммиак пен күкіртті ангидрит), еріткіштің полярлылығы кемігенде ерігіштігі төмендейді, полярсыз еріткіштерде ерімейді (алкандар, хлороформ) .
Ерігіштік (еріткіштің 100 грамында) :
• суда - 51, 8 (20 °C), 71, 7 (60 °C), 95, 0 (120 °C) ;
• сұйық аммиакта - 49, 2 (20 °C, 709 кПа), 90 (100 °C, 1267 кПа) ;
• метанолда - 22 (20 °C) ;
• этанолда - 5, 4 (20 °C) ;
• изопропанолда - 2, 6 (20 °C) ;
• изобутанолда - 6, 2 (20 °C) ;
• этилацетатта - 0, 08 (25 °C) ;
• хлороформда - ~0 (ерімейді) .
Алыну жолдары. Көбінесе карбамид көміраммиакты немесе карбаминаммиакты тұздардан 130° - l40° дейін қыздарғанда алынады.
H 4 NOCOONH 4 = H 2 O + H 2 NCOONH 4 = 2H 2 O + Н 2 NCONН 2
Тиокарбамин және тиокөмір қышқылының аммиакты тұздардан күкіртсутекті бөліп тастағанда:
H 4 NSCOSNH 4 = H 2 S + H 2 NCOSNH 4 = 2H 2 S + H 2 NCONH 2
Фосген мен аммиактың қосылысынан:
OCCl 2 + 2NH 3 = NH 2 CONH 2 + 2НCl
Фосген мен натрий фенолятынан оңай түзілетін фенолдың көмір эфиріне аммиакты газбен әсер еткенде түзіледі:
ClCOCl + 2C 6 H 5 ONa = С 6 H 5 OCOOC 6 H 5 + 2NaCl
С 6 Н 5 ОСООС 6 Н 5 + 2NН 3 = NH 2 CONH 2 + 2C 6 H 5 (OH)
Цианамидтің гидратациясы кезінде:
NCNH 2 + H 2 O = NH 2 CONH 2
Штрекер карбамидті гуанинге тұз қышқылы мен бертолет тұзымен әсер еткенде алды:
2C 5 H 5 N 5 O + 7H 2 O + 3O 2 = 2C 2 O 4 H 2 + 5(NH 2 ) 2 CO + CO 2
Циан қышқылды калий мен күкірт қышқылды аммонийді суда ерітіп, құрғақ етіп буландырып және оны спиртпен бөледі, ол K 2 SO 4 ерімейді:
2KCNO + (NH 4 ) 2 SO 4 = 2NH 2 CONH 2 + K 2 SO 4
Аммиакты алофан эфирімен қыздырып әрекеттестіргенде және аммиакты әсерінде:
NH 2 CONHCOCBr 3 + NН 3 = С 2 Н 5 N 3 О 2 + СНВr 3
177°С температурада ыдырап кететін кристалды заттар. Сілтінің қатысында мыс купоросымен әсер еткенде биурет қою қызыл немесе күлгін түс береді [7] .
1. 1. 1 Карбамидтерді аминдер және цианаттардан алу
1-Моно- және 1, 1-диалмасқан карбамидтерді ыңғайлы тәсілмен алу сілтілік металдардың біріншілік немесе екіншілік аминдері және цианаттары арасындағы реакция болып табылады. Реакцияны минералды қышқыл қоса отырып, су немесе органикалық еріткіш ортасында жүргізеді. Әдетте, аминнің және цианаттың эквимолярлы қатынастарын қолданады.
Тәжірибеде аминдер тұздарын қолдану ыңғайлы, себебі олар, біріншіден, тиімдірек, ал екіншіден бұл жағдайда қосымша қышқыл қосуды қажет етпейді.
Реакцияны су ортасында өткізген дұрыс, өйткені аминдер және цианаттар тұздары суда жақсы ериді, ал түзілетін карбамидтер кейбір қарапайым алкилкарбамидтерден басқа суда аз ериді. Бұл жағдайда карбамид тұнбасының түсуі реакцияның дұрыс жүретінін көрсетеді.
Қарапайым алкилкарбамидтерді сәйкес аминдердің гидрохлоридтері (гидросульфаттары) және сулы ерітіндідегі KOCN-нан алады. Реакцияны амин тұзы және KOCN ерітіндісінен суды буландыру арқылы жүргізеді, өнімді қалдықтан этанолмен ыстық экстракция арқылы бөліп алады.
Фенилкарбамидті тұзқышқылды анилин және су ерітіндісіндегі KOCN-нан бөлме температурасында алады.
о-толилкарбамидті сірке қышқылы және су қоспасында бөлме температурасында о-толуидин және KOCN алады.
Нафтил-2-карбамидті мұзды сірке қышқылындағы 2-аминонафталин және KOCN-нан реакционды массаны әлсіз қыздыру арқылы алады [8] .
1. 1. 2 Карбамидтерді аминдерден және органикалық изоцианаттардан алу
Органикалық изоцианаттардың аминдермен әсерлесуі симметриялық емес карбамидтер синтезінің ең кең тараған әдісі болып табылады.
Бұл реакция көпшілік аминдер (біріншілік, екіншілік, алифаттық, ароматтық, гетероароматтық, гидроксиламиндер, аминоспирттер, амидтер, т. б. ) және изоцианаттардың көбіне (алифаттық, ароматтық, гетероциклді) жалпы болып табылады.
Изоцианаттар - жоғары реакциялық қабілетті қосылыстар. Сондықтан аминдермен реакцияны бөлме температурасында немесе суыту кезінде, сирек жағдайда қыздыру арқылы жүргізеді. Әдетте, реагенттердің эквимолярлы мөлшерлерін немесе органикалық изоцианаттың артық мөлшерін, сирек кезде амино-тобы бар қосылыстың артық мөлшерін қолданады.
Үрдісті әдетте органикалық еріткіште жүргізеді. Бұл мақсатта ароматтық көмірсутектер (бензол, толуол, ксилол, хлорбензол, т. б. ), спирттер (этанол, метанол), диоксан, ТГФ, ацетонитрил, ДМФА, галогенкөмірсутектер және т. б. пайдаланады.
Органикалық изоцианаттардың аминдермен реакциясы әдетте алмасқан карбамидтердің жоғары шығымдарымен жүреді [9] .
1. 1. 3 Карбамидтерді аминдерден және фосгеннен алу
Біріншілік және екіншілік аминдердің фосгенмен реакциясы симметриялық диалмасқан карбамидтердің түзілуіне әкеледі және бұл қосылыстар синтезінің жалпы әдісі болып табылады.
Реакция үшін аминнің артық мөлшерін пайдалану қажет, себебі оның жетіспеушілігі кезінде реакцияның негізгі өнімі изоцианат болады.
Егер бастапқы амин суда еритін болса, онда фосгенмен реакцияны фосгенді амин ерітіндісі арқылы өткізіп су ортасында жүргізген дұрыс. Сонымен қатар, инертті органикалық еріткіштер - ароматтық көмірсутектер, галогеналкандарды қолдануға болады.
Алмасқан карбамидтер шығымын арттыру мақсатында синтез кезінде бөлінетін хлорлы сутекті қоспа-акцепторлар көмегімен байланыстыру ұсынылады. Су ортасында хлорлы сутек акцепторлары ретінде сілтілер, натрий және кальций карбонаттары, натрий ацетаты, магний және мырыш тотықтарын қолданады. Органикалық еріткіш ортасында мұндай акцепторлар болып үшіншілік аминдер болады.
Фосгенмен реакция жылдамдығы аминдер негізділігіне байланысты болады. Алкил- және диалкиламиндер ароматтық аминдерге қарағанда жылдам әсерлеседі. Ароматтық аминдер ішінде ең жоғары реакционды қабілетті ароматтық ядрода электронодонорлы алмастырушылары бар қосылыстар көрсетеді.
Реакцияны бөлме температурасында немесе қыздыру арқылы жүргізеді [10] .
1. 1. 4 Карбаматтар және карбонаттар аммонолизі
Карбаматтар аммонолизі симметриялы алмасқан карбамидтерді, ал карбонаттар аммонолизі тек симметриялық карбамидтерді селективті түрде алуға мүмкіндік береді. Әдетте, реакцияны органикалық еріткіштерде жүргізеді. Карбаматтар және аминдерді қолданған кезде реакцияға эквимолярлы мөлшерге жақын реагенттерді, ал карбонаттар аммонолизі кезінде - екі және одан артық еселенген аминнің артық мөлшерін енгізеді [11] .
1. 1. 5 Карбамидті ацилдеу
Ацилкарбамидті алудың классикалық түрі карбамидке хлорангидридтер немесе карбон қышқылының ангидридтерімен әсер ету болып табылады.
Карбамидтерді хлорангидридтермен және карбон қышқылының ангидритерімен ацилдеу инертті органикалық еріткіштерде бөлме температурасында немесе аздап қыздырғанда (40 - 80є С) өткізеді: бензолда, толуолда, және т. б.
Карбамидті карбон қышқылының ангидридімен ацилдеу H 2 SO 4 әсерлі катализатор болып табылады. Реагенттердің қатынасына байланысты моно- немесе диацилді туындылар түзілуі мүмкін.
1-Моноалмасқан карбамидтің ароилхлоридтермен немесе негіздердің қатысында инертті еріткіш ортасында сәйкес 1-R-3-ароилкарбамид алынады. Реакцияда түзілген хлорлы сутектің байланысы үшін негіздердің болуы қажет.
Сонымен қатар карбамидті ацилдеу су сіңіретін реагенттердің қатысында, мысалы, олеум, хлорсульфонды қышқыл, сірке ангидриді, апротон еріткішіндегі трифенилфосфин (ДМФА, N, N-диметилацетамид), пиридин қатысында үшхлорлы фосфор, карбон қышқылдарымен өткізуге болады.
Карбамидті ацилдеу үшін арнайы реагент 2, 2-диметил-6-фенил-1, 3-диоксан-4-он болып табылады.
Карбамидті ацилдеу ацетонитрилдегі изоцианаттың эквимолярлы мөлшерімен шығымы 60-80% болатын моноарил- және моноалкилбиуреттер түзіледі.
Арилкарбомидтер BuLi (ТГФ, 0єС) өңдегенде карбамидтің литий тұздарын түзеді, олар хлорангидридтер мен қышқыл ацилирлеу ангидридтер өнімдері алынады.
Полярлы апротонды еріткіштерде имидазолин-2-он карбон қышқылының циклді ангидридтерімен реакциясында N-ацилалмасқан имидазолин-2-он алынады (MeCN, ДМСО, ДМФА) . Басқа әдіспен ең бірінші имидазолин-2-он NaH әсерімен минералды майда анионды түрге келтіреді, кейін карбон қышқылының хлорангидридімен өңдеп, шығымы 69% болатын N-ацилалмасқан имидазолин-2-он түзіледі [12, 13] .
1. 1. 6 Карбамидті алкилдеу
Карбамидтегі азот атомы карбонил тобымен байланысқандықтан төмендетілген нуклеофилді қасиеттерге ие болады. Осыған байланысты карбамидтерді біріншілік және екіншілік алкилгалогенидтермен алкилдеу қатаң жағдайларда жүріп, өнімдердің аз шығымымен сипатталады.
Карбамидтерді карбкатиондарды оңай түзуші қосылыстармен алкилдеу әдістері үлкен мағынаға ие. Мұндай қосылыстарға үшіншілік спирттер, бензгидрол, үшіншілік алкилгалогенидтер және бензилалогенидтер жатады. Сонымен қатар карбамидтер үшіншілік олефиндермен қышқыл қатысында, ең бастысы күкірт қышқылы қатысында алкилденеді.
Карбамидтің ацетосірке эфирімен ДМФА-SiClMe 3 жүйесіндегі конденсациядан шығымы 70 % 3-уреидобут-2-еноат (3-уреидокротон қышқылының этил эфирі) алынады.
1, 3-Диарилкарбамидтердің N-метилді және N-этилді туындыларын 1, 3-диарилкарбамидтерді NaH және йодты алкилдермен ДМФА-да өңдеу жолымен алады.
Алкилимидазолин-2-онның жоғары шығымды синтезі бастапқы алкилимидазолин-2-онды ДМФА-да NaH суспензиясымен өңдеп, кейін түзілген N-аниондарды алкилгалогенидтерімен алкилдеуге негізделген.
Имидазолин-2-онның эпихлоргидринмен үшэтиламин немесе аммонийдің төртіншілік тұздарының каталитикалық мөлшерлері қатысында әсерлесуі нәтижесінде 1, 3-диглилицидилтуындылар алынады [14-17] .
1. 2 Карбаматтар
Карбаматтар (уретандар) - қосылыстың жалпы формуласы R'R''NCOOR, мұндағы R' және R'' - H, Alk, Ar; R - Alk, Ar. Уретандар тұрақсыз карбамин қышқылының эфирлері болып табылады H 2 NCOOH және оның N-орынбасар туындылары. Көбінесе этилкарбамат туындыларын уретандар деп атайды [18] .
Қасиеттері. Түссіз кристалдық заттар, органикалық еріткіштерде ериді, төменгі уретандар суда ериді. Қосылыстар тобының аты - уретан, этилуретанның тривиалды атауынан H 2 NCOOC 2 H 5 шыққан.
Карбаматтар нуклеофилдермен (аминдер, т. б. ) оңай әрекеттесіп, спирттерді бөледі:
R'NHCOOR + HX R'NHCOХ + ROH
Уретандар сәйкес спирттер, аминдер (немесе аммиак) және СО 2 дейін гидролизденеді, ал аммонолиз - карбамид туындыларына дейін. Уретандардың N-ацилдеу және алкилдеуі мүмкін, бірақ бұл реакция көбінесе алкокситобының элимирлеуімен қиындатылады.
Литий алюмогидридімен уретанды R'R''NCOOR тотықсыздандырғанда метиламиндер, ал сұйық аммиакта каталитикалық гидрлеу немесе натриймен тотықсыздандырғанда аминдер R'R''NH түзіледі.
Уретандарды нитрлегенде және нитрозирлегенде N-нитрозо- және N-нитроуретандарды түзеді.
Қолданылуы. Өндірісте уретанды каучук, полиуретанды желім, полиуретанды лак, полиуретанды талшық түрінде полиуретандар көп қолданылады. Бірқатар уретандар дәрі-дәрмек түрінде (мысалға, прозерин, карбахолин, пропанидид) және гербицид түрінде қолданылады.
Уретандар нуклеофилді реагенттермен оңай әрекеттеседі, егер де оңай бөлінетін топ болса, реакция бөліну-қосылу механизмі бойынша жүре алады:
R'NHCOOAr R'NCOR'NHCOX
R'NHCOOR + HX R'NHCOX + ROH
Уретандардың қышқылды және сілтілік гидролизі сәйкес спиртке, NH 3 (немесе аминге) және CO 2 әкеледі. NH 3 -пен реакцияда карбамидтің сәйкес туындыларына, нитрозирлеу және нитрлеу - N-нитрозо- және N-нитроуретандарға келтіреді. N-нитрозо-метилуретан - диазометанды алу үшін қолданылатын қосылыс.
Уретандардың пиролизі кезінде изоцианаттар, LiAlH 4 тотықсыздандырғанда N-метиламин, каталитикалық гидрлеу немесе сұйық аммиакта натриймен өңдегенде - біріншілік аминдер түзіледі.
Уретанды алудың негізгі әдісі - изоцианаттарға спирттер немесе фенолдарды қосу. Сонымен қатар, хлорқұмырсқа қышқылының NH 3 -пен немесе біріншілік аминдермен, спирттердің NH 2 CONH 2 , NH 2 COCl немесе циан қышқылымен қосылыс эфирлері қолданылады.
Уретандар карбон қышқылының азидтері немесе амидтерінен түзіледі. Диизоцианаттардың гликольдермен әрекеттесуі полиуретандарға әкеледі.
Уретандар - инсектицидтер, гербицидтер, дәрі-дәрмектер, сонымен қатар диазоалкандардың синтезінде қолданылады [19, 20] .
1. 3 Уреидтер
Карбамид сутек атомдарын қышқыл радикалдарымен алмасқанда уреидтер пайда болады. Уреидтердің бірінші өкілі - бензоил ((C 6 H 5 CO) NHСОNH 2 ) және ацетил карбамид ((СН 3 СО) NНСОNH 2 ) . Оларды Зинин карбамид пен хлорангидридті әрекеттестіргенде алды [21] .
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz