Күміс металлургиясы: өндіру, тазарту және екінші ретті шикізатты өңдеу технологиялары


Қазақстан Республикасының білім және ғылым министрлігі
Реферат
Тақырыбы : Күміс металлургиясы
Орындаған:
Тексерген :
Жоспар
Кіріспе
1 Күмісті өндіру . . . 4
2 Күмістің зергерлік істе қолданылуы . . . 5
3 Күмістің ғылым мен техникадағы рөлі . . . 6
4 Тиын жасау өнеркәсібіндегі күмістің рөлі . . . 7
5 Күмісті бөліп алу әдістері . . . 9
6 Күмісті тазарту . . . 11
7 Күміс өндірудің екінші ретті металлургиясы . . . 13
8 Құрамында күмісі бар екіншілік шикізатты өңдеудің технологиялық схемасы . . . 14
9 Кино-, фото-, және рентгенопленкалардан, фотопластинкалардан, фотоқағаздан күмісті бөліп алу . . . 20
Қорытынды
Пайдаланылған әдебиеттер тізімі
Кіріспе
Күміс (лат. Argentum, Ag) - элементтердің периодтық жүйесінің І тобындағы химиялық элемент, атомдық нөмірі 47, атомдық массасы 107, 88. Табиғатта тұрақты екі изотопы бар: 107Ag және 109Ag. Күміс жұмсақ, созылғыш (1 г Күмістен ұзындығы 1800 м сым тартуға болады), ақ түсті металл, тығызд. 10, 5 г/см3, балқу t 961, 9°С, қайнау t 2170°С, тотығудәрежелері +1, +2, +3, сиректеу +4. Электр тогын, жылуды жақсы өткізеді. Күмістің активтігі нашар, коррозияға төзімді, бірақ күкірт, галогендермен тез әрекеттеседі. Қыздырылған концентрлі азот және күкірт қышқылдарында ериді. Ауадағы оттекпен жоғары температурада қыздырғанда да әрекеттеспейді, бірақ құрамында күкіртсутек бар дымқыл ауада оттек арқылы тез тотығып беті қараяды. Күміс қорғасын-мырышты, мыс, алтын-күмісті кентастар даналынады. Оның басқа металдармен қорытпасы зергерлік бұйымдар жасауда, медицинада қолданылады. Күміс препараттары (күйдіретін, микробтарды жоятын, т. б. ), кино және фото өнеркәсібінде, химия, электртех. Және электрондық өнеркәсіптерінде, т. б. қолданылады. Аg+ иондары суды жақсы тазартады. Қазақстанда Күміс Бозшакөл, Қоңырат, Ақтоғай, Айдарлы, Бақыршық, т. б. кен орындарында кездеседі. [5]
Күмісті өндіру
Асыл металдардың ішінен күміс табиғатта ең көп таралғаны болып келеді. Оның жер қыртысындағы мөлшері алтынның мөлшерінен 20 есе көп және платиноид элементтерінің мөлшеріне тең. Күмістің теңіз және мұхит суларындағы мөлшері шамалы (3-10мг/т), бірақ қазіргі кездегі әдістермен оны бөліп алу тиімсіз.
Күміс алтынға қарағанда сомтума түрінде кездесу мүмкіндігі аз. Күмістің экономикалық маңызы бар минералдарға : аргентит Ag2S; кераргирит AgCl; пираргирит Ag3SbS3; прустит Ag3AsS3; стефанит Ag5SbS4; бромирит AgBr; иодирит AgI жатады.
Күміс аз мөлшерде алтын, мыс, қорғасын және мырыш кендерінде кездеседі. Қазіргі кезде бұларға әлемдік біріншілік күміс өндірудің 2/3 бөлігі келеді.
Күміс өндіру көлемінің өсуімен оны өндіру және тазалау технологиялары да жетілдірілді. 1752 жылы академик У. Х. Сальхов алтын мен күмісті азот қыщқылы арқылы айыруды ұсынды. Одан кейін алтын мен күмістің негіздердің цианидті сулы ерітіндісінде жақсы еритіндігі анықталған. Алтын мен күмістің еруін ауа жылдамдататыны және оларды асыл емес металдармен қаптау мүмкіндігі ашылды. 1802 жылы француз ғалымы д. Арсе күкірт қышқылымен күмістің аффинажын ашқан. Бұл процесс кезінде тазартылмаған күмісті қайнаған мыс купоросында ерітеді, бұның нәтижесінде алтын төбіне шөгеді, ал күміс мыс немесе темір арқылы тотықсызданады. Бұл процесс XIX ғасырда кең қолдау тапқанымен кейін электролиз әдісімен ығыстырылды. Электролиз арқылы күміс нитратының ерітіндісі құйылған ваннада тазартылмаған күмістен жасалған анодтан тазалығы 99, 9% күміс алынды.
Бұдан кейінгі күміс металлургиясының дамуы қорғасын кендерін пісірудің жаңа 2 әдісімен байланысты. Біріншінің негізінде құрамына қорғасын кіретін күміс қорытпасының таңдамалы кристаллизациясына негізделген. Екіншісі қорғасында мырыштың шекті ерігіштігі және мырыштың күміспен бірге қосылыстар түзіп ерітінді бетіне көбіктенуіне негізделген. Егер бұл құйманы кристаллизациялану температурасына дейін салқындатсақ, біріншедіен күміс кристалл түріндегі құрылымдарды түзе бастайды, ал қорғасын кристалдары құрылым түзе алмай, балқыманың оңай балқитын түрінде қалады. Бұл бөліктерді ажырату арқылы концентрациясы жоғары күміс сомын алуға болады. Одан кейін сомды тотықтырғыш күйдіру процесі жүреді. Бұл процесс кезінде корғасын және тағы басқа асыл емес металдар пешке айдалатын оттек әсерінен тотығып, балқыған оксид түрінде бөлініп шығады. Процесс нәтижесінде сом ішіндегі күміс мөлшері 90 %дейін жоғарылайды. Таза күмісті алу үшін сом аффинаж процесіне жіберіледі. [1]
Күмістің зергерлік істе қоланылуы
Күміс - пластикалық қасиеті жоғары, жұмсақ және оңай өңделетін металл, бірақ қаттылығы жеткіліксіз. Сондықтан зергерлік істе күмістің мыспен қорытпасы қолданылады. Металдарды қосу нәтижесінде күмістің қаттылық, иілгіштік, термоөңдеу нәтижесінде құрылымын өзгерту қасиеттеріне ие болады.
Қарапайым қалыпты бұйымдарды құю арқылы алады. Ал қиындығы жоғары зергерлік бұйымдарды қалыптау процесі және қосымша қарайту арқылы өндірген. Қарайту процесі тек күміспен жұмыс жасағанда ғана қолданылады. Бұл процесс кезінде қиылып алынған суретті күкіртпен араластырылған күміс, мыс, қорғасын қорытпасынан жасалған ұнтақпен толтырады. Бұдан кейін ұнтақты балқытады да, салқындағаннан кейін жылтырлатады. Нәтижесінде суретте күңгірт сұр сызықтар пайда болады. Қарайту процесі көне Рим заманынан белгілі. Күміс бетінің таңдамалы қараюына алып келетін сульфид реактивін абайлап жалату бұндай әсерге жақын нәтиже береді.
Күмістен жасалған бұйымдарды көп жағдайда эмальмен сәндейді. Эмальдау көне Греция және Римде кең қолдау тапты, бірақ бұл жерде эмальдау тек мыс және алтыннан жасалған бұйымдарға қолданған. Күміс эмальдануын Еуропаның бірқатар музейлерінен көруге болады . Олардың ерекшелігі эмаль күміске нашар жабысуы және тұрақтылығымен ерекшеленеді.
Күмістің ірі сомдарын алуды үйренгеннен кейін күмістің қолдану аясы өсті. Енді күміс ыдыс-аяқ жасауда кең қолданыс тапты. Көне Рим дәуірінен бастап күмістен жасалған ыдыс-аяқ жоғарғы қоғамда кең қолданыла бастады. Шіркеу де өз монастырлары және ғибадатханаларын сәндеу жұмыстарында күмісті қолдана бастады, ал күмістен жасалған ыдыстар діни рәсімдер өткізілген кезде қолданылған. Гильдиялар және басқа да одақтар пайда болғаннан бастап күміс айырма белгеілер(күміс күрзі) түрінде қолданыла бастады. [2]
Күмістің ғылым мен техникадағы рөлі
Күмістің қышқылдарға төзімділігі және гигиеналық қасиеттері дәрігерлерге оны стоматология және хирургияда қолдануға мүмкіндік берді. Мысалға бассүйек трепанациясы кезінде пайда болған тесікті жабу үшін күмістен жасалған пластиналар, сынған сүйектердің қозғалуын шектеу үшін күміс сымдары қолданылды. Күміс амальгамасын стоматологияда пломба жасау үшін қолданған.
Сәндеу үстелінде алғашқылардың бірі болып айна пайда болды. Алғашқыда айна ретінде қарапайым жылтырланған пластина немесе диск қолданылған. XIV ғасырда Венецияда айнаның жетілдірілген түрі пайда болды, бұл айна үстіне қалайы амальгамасын салу арқылы жасалған. Бұл процесс арқылы жасалған айнамен дүниежүзінің әрбір түкпірінде қолданды. 1855 жылы француздық ғалым Птижан күміс нитраты ерітіндісінен шарап қышқылы және оның тұздар арқылы күміс қабықшасының пайда болуы нәтижесінде қолдану мерзімі үлкен айна жасауды ойлап тапты. Дәл сол уақытта күмістің металл емес заттардың бетіне жалатуды қамтамасыз ететін процестер табылды (вакуумда булану және электрлік доғасы әсерінен шашырату)
Күмістің құнды қасиеттеріне қарамастан XIX ғасырдың аяғында күміске деген сұраныс ұсынысқа қарағанда аз болды. Бұл кезде электротехникалық өндіріс жаңа пайда болған. Бірақ бұның қажеттілктерін мыс та қанағаттандыра алды. XX ғасырда да сұраныс өндірістен қалып отырды. XX ғасырдың 30 -жылдары өндірістік қажеттіліктер дүниежүзілік өндіріс көлемінің тек ¼ тең болды. Екінші дүниежүзілік соғыс қарсаңында жаңа техникалық құрал-жабдықтар, техниканың салалары және қару түрлері пайда болды. Зымыран техникасы, суасты флоты, торпедалар және басқармалы оқтардың пайда болуы жаңа, өлшемдері кіші болатын аккумуляторларды талап етті. Бұл аккумуляторлар күміс-мырышты, күміс-кадмилі болатын. Екінші дүниежүзілік соғыс уақытында АҚШ -та электролит зауыттарында мыстан жасалған ток өткізгш шиналар күмістен жасалғандарға ауыстырылды.
Күмістің көп бөлігі әртүрлі металдар мен қорытпаларға дәнекерлеуші припайка жасауға қолданылды. Күмістен жасалған припоилар соққы және вибрация әсерлеріне төзімді, берік және пластикалық спаиларды түзеді. Осы припоилармен дәнекерленген паилар өзінің беріктігін төмен температураларда да жоғалтпайды, арнайы қызуға берік проипойлар 500оС температураға дейін тұрақты. Тотығуға қарсы тұру қабілеті күмістің авиа және космо өндірістерде, ал оның жақсы электроөткізгіштігі - электротехникада қолдануға мүмкіндік береді. Күмістің каталитикалық қасиеттері химия саласында бірқатар химиялық заттарды алуда қолданылса, оның химиялық қасиеттері оны агрессивті сұйықтарды сақтауда қолданылады. [2]
Тиын жасау өнеркәсібіндегі күмістің рөлі
Күміс бертінге дейін дүниежүзінің көпшілік елдеріндегі ақша айналымында алдыңғы орынды иеленді. Көне Египет елінде ақша айналымында негізінен алтын мен күміс тиындары саналған, ал Аравия елінде күміс алтынға қарағанда құны 10 есе көп болды. Техниканың жетілдірілуі арқасында күміс алтынға қарағанда көбірек өндіріле бастады. Сауданың қызу жүруіне байланысты ақша көлемін өсірту керек болды. Жалпы алтын мен күмістің қолдану аясы әр жерде әркелкі болды. Мысалға Ассирия және Вавилонда күміс сом және жүзік түрінде таралды, бұл жерде тауар бағасы күмістің массасымен анықталған. Көне Греция жерінде бастапқыда тиындарды алтыннан соққан, уақыт өте келе тиындарды күмістен соға бастады. Көне Персия мемлекетінде Дарии патша кезінде ақшаның басым көпшілігі алтыннан болса, Ескендір Зұлқарнайын кезінде қайтадан басымдылығын күміс алды.
Алғашқыда саудада эквивалент ретінде күмістің дұрыс емес формалары және сомдары қолданылған болса, кейін қолайлы болу үшін күмістің жалпақ кесектерін қолдана бастады. Ертедегі Киев Русінде ерте кезден бастап рим динары, Шығыстан әкелінген дирхемдар және драхмалар қолданылды. XI ғасырдан бастап олардың орнына батыс еуропалық тиындар келді. Сол кезгі ресейде өзінің шикізат базасы болмады, сондықтан тиын соғу шетелден әкелінген тиындарды қайта соғу арқылы жасалған. Бұл жағдай тиын соғу үрдісінде ерекшелік қалдырды. Тиынды соғуда кең қолдау тапқан күміс металын бетке дейін жазып, одан тиындарды ойып алу орнына, тартылған сымнан жасады. Сымның керекті салмағын өлшеп алып, пресс астында жалпайтқан. Нәтижесінде формасы дұрыс емес дөңгелектер алынды. Бұл әдістің артықшылығына нәтижесінде қалдық қалмауын жатқызуға болады. Бұл дөңгелектер айналымға рубль деген атаумен енгізілді.
XVIII ғасырда күміс тиынмен қатар мыстан және алтыннан жасалған тиындар қолданыла бастады. Алтынның Америкадан көптеп әкелінуіне байланысты, басқаларына қарағанда кең қолданыс тапты. Бірақ тек Англияның қаржы жүйесінде үстемдік етті. Қалған барлық елдерде биметалды қаржы жүйесі орын алды. XIX ғасырдың аяғында күмісті өндіру көлемінің шектен тыс асып кетуі оның құнсыздануына алып келді. Нәтижесінде Еуропа елдері бірінен кейін бірі алтын стандартына көшті. Күміс стандартының алынуына байланысты, күмістің бағасы күрт төмендеді. Бағаның төмендеуі уақытша бірінші дүниежүзілік соғыс салдарынан тоқтады, бірақ бағасының төмендеуі 1929-1932 жылғы кризиске дейін жалғасты. Бұл кездегі күмістің бағасы 1 грамына 0, 78 цент болды.
XX ғасырдың 30-жылдары АҚШ-та күмісті өндірушілердің мүддесін қорғайтын, күмістің бағасын тұрақтандыратын заң жобасы қабылданды. Іс жүзінде АҚШ қайтадан биметалдық стандартқа келді.
Қазынашылар жергілікті халықтан нарықтағы бағадан жоғары бағамен сатып алған. Бірақ АҚШ-қа күміске деген жоғары сұранысты соған байланысты жоғары бағааны ұстап тұра алмады. Бұның себебі болып Үндістан және Қытайдан көптеп әкелінген күміс бөгет жасады.
Екінші дүниежүзілік соғыстан кейін өнеркәсіптегі күміске жоғары сұраныс және күмісті өндіру көлемінің қысқаруының себебінен тұтынушылар күмістің дефицитіне тап болды. Күміс бағасының өсуі себебінен айналымдағы күміс тиындарды алу туралы қаулы қабылданды және оның орнына никель тиындарымен алмастырды.
Бұдан кейінгі жылдары күміс, тиныдарды жасау өнеркәсібінде тек мерейтойлық және естелік тындарды соғу үшін ғана қолданылды. Бұл тиындарды сату мемлекет қазынасына қомақты қаражатты әкеледі. [3]
Күмісті бөліп алу әдістері
Цианидтау күмісті алуда ең көп қолданылатын әдістердің біріне жатады. Бұл процесс күміс шикізатын цианид гидроксидінің судағы ерітіндісінде еріту арқылы жүргізіледі. Цианидтау процесін ең алғаш ойлап тапқан П. Р. Багратион болған. Бұл жаңалық 1843 жылы «Вестник» деген газетте жарияланған болатын. Асыл металы бар кендерде басқа керексіз қоспалар да болады.

Сондықтан да құрамындағы асыл металды бөлу үшін цианидтау процесін қолданады. Күміс оксидіне бір сәтте екі сыртқы фактор әсер етеді. Біріншісі бұл оттегі, екіншісі ерітіндідегі цианид. Бөлек бұл химиялық заттар күміс оксидіне ешқандай әсер етпейді. Ал бұлардың қосынды әсері күміс өндіру өнеркәсібінде күмісті табысты бөліп алуға мүмкіндік береді. Егер сулы оксидте цианид бар болғанда, күміс бұл ерітіндіде тез уақыт еріп кетеді.
Кеннен алынатын пайдалы металдарды өңдеу ыдыстағы асыл емес немесе жартылай асыл металдар цианид шаңымен бірге шөккеннен кейін басталады. Бұдан кейін күкірт қышқылы көмегімен шөгіндіден барлық керексіз заттардан тазартылады. Қалған ерітіндіні жуады, фильтрлейді, буландырып алып, балқытып, сомдарға құяды. Күміс сомдарын алғаннан кейін оларды келесі тазарту сатыларына зауытқа жібереді.
Өндірудің келесі әдісі- күмісті амальгамалау - ерте кезден бастап белгілі болған. Бұл әдіс 2 мың жыл бұрын пайда болған. Бұл процесс күмістің немесе басқа да асыл металдардың сынаппен қосылыстар түзуіне негізделген . Бұл қосылу реакциясы қалыпты жағдайда өтеді. Күмістің аз мөлшері ерітілген сынап, металдың сулану қасиетін арттырады.
Амальгамация процесі арнайы құрылғыларда жүргізіледі. Құмға дейін ұнтақталған кен сумен қосылып, сынап беті арқылы жүреді. Нәтижесінде күмістің майда бөлшектері сынаппен қосылып сулы қосылыс түзеді, одан кейін бұл қосылыстан пресстеу арқылы суды ығыстырып шығарады, бұл процесс арқылы сусыз амальгама алады. Осы амальгамадан буландыру арқылы сынапты бөліп алады. Нәтижесінде құрамында 1 бөлшек алтын мен 2 бөлшек күмісі бар металдар қоспасы алынады. [3]
Күмісті тазарту
Күмісті өңдеудің басқа да түрлерін активті түрде қолданады . Егер шикізат ретінде мыс және қорғасын концентреттары қолданылса, өңдеудің пирометаллургиялық әдісін пайдаланған ыңғайлы. Бұл әдісті ең тиімді деп атайды, өйткені қорғасын және мыс қоспалары жоғары бағаланбағанына байланысты, өндіру құны да төмендейді және бағалануы төмен металдарды өндіруге жұмсалған қаражат ақталады. Күмісті мыс концентратынан бөлу электрохимиялық әдіс арқылы жүзеге асырылады.

Күмістен жасалған бұйымдар. Шикі мыс қосылысынан бөлініп алынған анодтар элетролиттік ваннаға салынады, содан соң электролиз процесі жүзеге асырылады. Анодта мыс еріп, жіңішке катодта шөгеді, ал күміс ыдыс түбіне шөгіп штамп түзеді. Кейін бұл штамптан күміс бөлініп алынады. Шикі қорғасыннан күмісті қосындыларын бөліп алу үшін күміс және мырышпен өңдейді. Процесс жоғары температурада жүргізіледі (450°C)
Бұл металл қорғасынға қарағанда балқытылған мырышта жақсырақ ериді, сөйтіп ол жоғарғы қабатқа, мырыш ерітіндісіне қарай орын ауыстырады. Бөлініп алынатын күміспен мырыш қабаты бөлініп алынады, келесі сатыда бұл қабаттан тек құнды металды бөліп алу керек. Бұл үшін қалдықты 1250°C температурада графит ретортасы арқылы айдайды. Жоғары температура жағдайында мырыш буланып кетіп, ақырында күміспен бірге мышьяк және басқа да қоспалар қалады. Тазалығы жоғары металды алу үшін оны қосымша 1000°C температурада оттек қатысында балқытып сомдарға құяды. Соңғы өнім электрохимиялық әдіспен тазалауды қажет етеді.
Күміс кенінің негізгі кен орындары дүниежүзінде келесі мемлекеттерде орналасады:
1. Германия.
2. Испания.
3. Чили.
4. Мексика.
5. Канада.
6. Перу.
7. США.
8. Австралия.
9. Китай.
10. Россия.
11. Швеция.
12. Норвегия.
13. Казахстан.
14. Польша.
2008 жылы дүниежүзілік күміс өндірісі 20900 тонна металды шығарды. Бұл жылы өндіріс көлемі бойынша Перу 3600 тонна металл өндіріп, бірінші орынды иемденді. Екінші орында Мексика 3000 тонна, үшінші орынды Қытай 3000 тонна иемденді. [3]
Күміс өндірісінің екінші ретті металлургиясы
Күміс және басқа асыл металдардың халық шаруашылығында көптеп қолданылуы, бізді бұл металдарды жұмсауды үнемдеуді, оларды екіншілік шикізат көздерінен алуды мәжбүр етеді. Қазіргі кезде асыл металдарға деген сұраныс оларды өндіру көлемімен қамтамасыз етілмейді. Сондықтан олардың екіншілік шикізат көздері игерілген.
Екінші ретті металлургияның ерекшелігі асыл металдардың көптеген физикалық формасы, химилық құрамдарының алуан түрлілігінде болып келеді.
Көп жағдайда асыл металдардың екіншілік шикізат көздеріндегі асыл металл мөлшері біріншілік шикізатқа қарағанда жоғары болып келеді. Сондықтан мұндай шикізатты қайта өңдеу тиімді болып келеді. Асыл металдардың мөлшері аз қалдықтарды да қайта өңдеу олардың өзіндік құны жоғары болуына байланысты тиімді. [3]
Құрамында күмісі бар екіншілік шикізатты өңдеудің технологиялық схемасы
Құрамында күмісі бар екіншілік шикізатты өңдеудің технологиялық схемасы келесі операциялардан тұрады: шикізатты сынамалау, доғалы және индукциялы пештерде балқыту, анодтарды электролиттік рафинадтау және ұнтақтарды алу.
Лигатуралық күмісті балқытудың басты мақсаты күмісті оның қандай да химиялық қосындыдан бос күйге шығару, қосындыларды қождау және пайда болған металдан қожды бөліп алу болып табылады.
Күмісті металдық күйге көшіру жоғары температура әсерінен және қосындылармен бірге(флюс) химиялық әсерден болуы мүмкін. Флюс ретінде көмір, сода, темір, бура, натрий селитрасы, кварц құмы, және бор қолданылуы мүмкін. Электрдоғалы пештерде қалдықты балқыту шихтасының құрамы V. 1. таблицада көрсетілген.
Құрамында күмісі бар шикізатты өңдеген кезде шикізаттың көп бөлігі бромды, күкіртті және хлорлы түрде болады. Шихтаның құрамына бір уақытта қалдықтың бірнеше түрін әр түрлі концентрацияларда салады.
Бұдан кейін көмірқышқылды күмістің термиялық ыдырауы жүреді. Ары қарай күміс оксиді де ыдырайды.
Ag2CO3=Ag2O+CO2^; 2Ag2O=4Ag+O2^
Күкіртті күмісті балқытқан кезде күмістің тотықсыздануы кальцийленген содамен реакциясы нәтижесінде жүреді:
2Ag2S+4Na2CO3=8Ag+3[Na2S*Ag2S] +Na2SO4+CO2
Na2S*Ag2S құрамындағы күмістің тотықсыздануы үшін балқымаға темірді енгізеді. Нәтижесінде сульфид ішінен күміс ығыстырылып шығарылады.
Бромды және хлорлы күмісті балқытқан кезде флюс ретінде кальцийленген соданы қолданады. Сонымен қатар алмасудың негізге процестері жүреді:
2AgBr+Na2CO3=Ag2CO3+ 2NaBr;
2AgCl+Na2CO3=Ag2CO3+2NaCl.
Темірдің артық мөлшерін байланыстыру үшін кообразды күкіртті қолданады. Әдетте бромды, хлорлы, күкіртті күмістің құрамында асыл емес металдар жоқ болады. Ал қалдықтардың күл, креца, балқымалар және тағы басқа түрлері құрамында асыл емес металдардың мөлшері бар болады. Сондықтан шихтаның құрамында асыл емес металдардың қосындыларын тотықтыру үшін натрий селитрасын қосады, ал пайда болған оксидтерді қождау үшін техникалық бураны, құм және шыныны қосады.
1100-1200°C температурада күміс балқымада оқсид түрінде жүре алмайды, өйткені >0, 021 МПа. Сондықтан да асыл емес металдардың қосындыларының тотығуы жүреді. Тотықты балқыту кезінде бірінші ретте мырыш тотығуға ұшырайды, өйткені ол басқа металдарға қарағанда оттегіге жақынырақ қасиет көрсетеді. Балқыту кезінде асыл металдардың қосындылары, әсіресе мырыш пен мыстың, тотығып, қожға жиналады.
Отандық және шетелдік күмістің екінші ретті шикізатын балқыту зауыттардың жұмыс істеу тәжірибесіне қарағанда балқыту шикізаттың құрамына байланысты шихтаның және флюстардың арақатынасы әр түрлі болады. Шихтаның құрамын әдеттегі құрамы V. 1. таблицада көрсетілген.
Шикізатты балқыту үшін ДС-0, 5 (сурет 1) доғалы болат балқыту пеші қолданылады. ДС-0, 5 техникалық сипаттамасы төмендегідей:
Балқыту уақыты, сағ . . . 1, 5
Бір балқытудан алынған, кг :
Күміс . . . 546, 19
Шаң . . . 60, 89
Қож . . . 70, 1
Күмістің мөлшері, %:
Шаңда . . . 1, 56
Қожда . . . 0, 36
Күмістің . . . түрге өтетін бөлігі:
Шаңға . . . 8, 682
Қожға . . . 2, 307
1 т балқытып алынған күміс үшін электроэнергия мөлшері кВт*сағ . . . 3153, 6
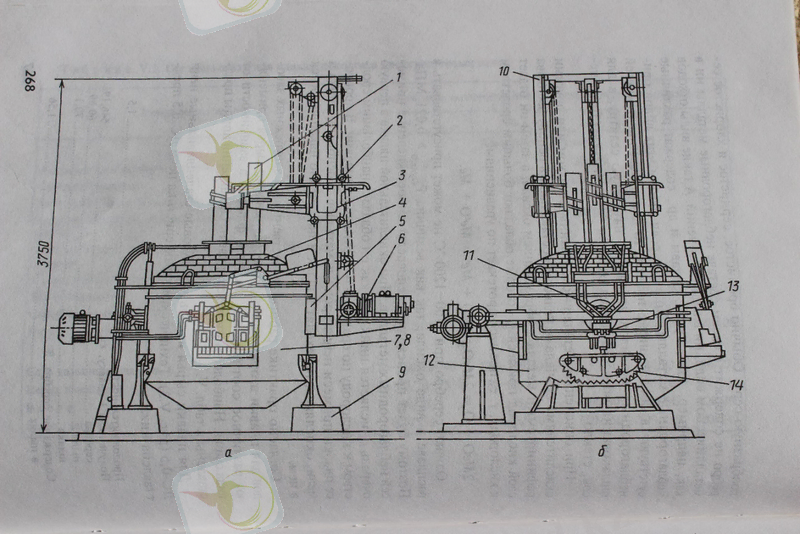
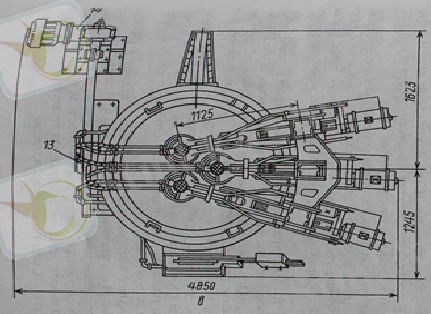
Сурет 1. Құрамында күмісі бар кенді балқытуға арналған ДС-0, 5 пешінің көлденең кесіндісі.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz