Платинаның ерітіндідегі 2,3-димеркаптопропансульфонатпен (унитиол) кешен түзілуін зерттеу және оны спектрофотометриялық әдіспен сандық анықтау


МАЗМҰНЫ
КІРІСПЕ . . . 3
І. ӘДЕБИЕТТІК ШОЛУ
І. 1. 2, 3 - және оның
қасиеттері . . . ……. . 4
І. 2. Платинаның комплесті қосылыстары . . . 6
І. 3. Платинаның фотоколориметриялық әдіспен
анықтау . . . 8
ІІ. ЭКСПЕРИМЕНТАЛЬДЫҚ БӨЛІМ
ІІ. 1. Негізгі заттардың сипаттамасы . . . 10
ІІ. 2. Эксперимент методикасы.
ІІ. 2. 1 Ерітіндідегі платина (ІІ) - 2, 3 -
системасын спектрофотометриялық әдіспен зерттеу . . . 10
ІІ. 2. 2. Платина (ІІ) унитиол әрекеттесуінің
мольдік қатынасын анықтау . . . 12
ІІ. 3. Эксперимент нәтижелері және оларды талдау . . . 15
II. 4. Спектрофотометриялық әдіспен унитиол
арқылы платинаның сандық мөлшерін анықтау
әдістемесі . . . 17
АНЫҚТАУ БАРЫСЫ . . . 18
ҚОРЫТЫНДЫ . . . 19
ҚОЛДАНЫЛҒАН ӘДЕБИЕТТЕР ТІЗІМІ . . . 20
КІРІСПЕ
Бұл дипломдық жұмыс - 2, 3 - натрий металдардың әртүрлі қоспаларымен әрекеттесу заңдылықтарын зерттеуге негізделген [1] . Унитиолдың аналитикалық қасиеттері өте кеңінен тараған, атап айтқанда сезімталдығымен, талғампаздығымен, металдардың кейбір катиондарымен берік комплексті қосылыстар түзу қабілетімен ерекше, оның тотығу - тотықсыздану қасиеті аналитикалық мақсаттарда пайдалануға мүмкіншілік береді. [2] . Басқаша айтқанда тиолдармен әрекеттесу нәтижесінде түзілген (унитиол тиолдарға жатады) комплексті қосылыстар өте активті ісіктерге қарсы препарат болып есептеледі [3] . Осыған байланысты зерттелген биологиялық активті (ісікке қарсы) қосылыстардың басым көпшілігі (1500 ден аса) платинаның цис-диамин комплексті қосылыстары болып табылған. Бұрын платинаның унитиолмен мынадай қосылысы PtHUn * 3H 2 O, PtHUn * 2H 2 O зерттеліп, ісікке қарсы жақсы нәтиже көрсеткен [4] . Бірақ қосылыстың фармакологиялық активтілігін арттырып, оның кері әсерлерін (побочные явления) азайту платинаның унитиолатты қосылыстарындағы лиганды ауыстыру арқылы іске асырылады деген пікір бар [5] . Осындай қосылыстардың қасиеттері зерттелмеген.
Бұл жұмыстың мақсаты платинаның ерітіндідегі комплекс түзілуін зерттеу.
Диплом жұмысының өзектілігі - бұл синтез деп алынған қосылыстар аппробациядан өткен, қатерлі іскке қарсы биологиялық активтілігі зерттеліп анықталған.
Диплом жұмысы кіріспе, екі тарау анықтау барысы, қорытынды, қолданылған әдебиеттер тізімінен тұрады.
Кіріспеде тақырып бойынша ғылыми ақпарат беріледі. Олар зерттеу жұмысында көрсетілген өзекті мәселе, зерттеу орны, мақсаты, міндеттері анықталған.
І. ӘДЕБИЕТТІК ШОЛУ
І. 1. 2, 3 - және оның қасиеттері
Химияның көп салаларында, әсіресе комплексті қосылыстар химиясы саласында, құрамында сульфгидрлі тобы бар - тиолдар (меркаптандар) органикалық реагенттер аса маңызды орын алады. Бұндай реагенттер өте сезімтал және берік комплексті қосылыстар түзуге бейім боп келеді.
Әсіресе өте берік комплексті қосылыстар түзетін дитиолдар. Оларға жататындар 2, 3 - натрий, оны бірінші рет Петрунькин 1950 жылы (Украина) атты ғалым тапқан [1] .
Унитиолдың синтезі алты стадиядан тұрады:
- Натрийдің алкилсульфатын алу.
- Оны натрийдің айналдыру.
- Дибромидті КSН - пен өңдеу.
- Реакциялық ортадан дитиолды бөліп алу.
- Бұл тұздан суда немесе спиртте күкіртті сутекпен ыдырату.
- Түзілген дитиолсульфоқышқылды содамен бейтараптау.
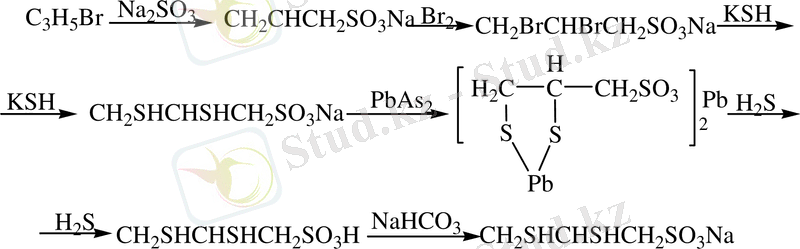
Унитиолдың структуралық формуласы:
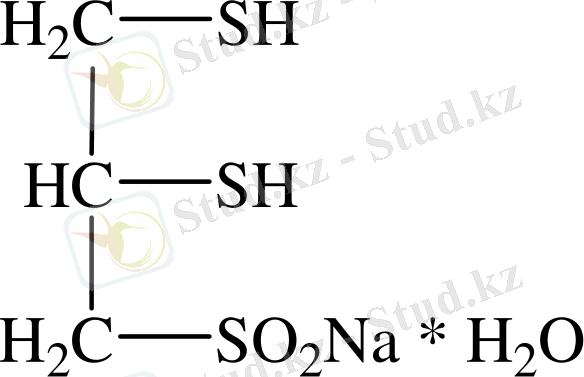
Унитиол - майда кристалды структуралы ақ порошок, суда жақсы ериді;
Органикалық еріткіштерде (спирттен басқаларында; эфир, бензол, хлороформ) ерімейді. Азот қышқылы мен аммиакта жақсы ериді. Ерігіштігі мына қатар бойынша төмендейді:
НNО 3 > H 2 SO 4 >HCl
Сулы ерітіндіде унитиол әлсіз екі негізді қышқылдық қасиет көрсетеді (рН=5) күшті қышқылыды ортада (рН=1) 2, 3 - қышқыл түрінде болады
CH 2 - SH
CH - SH
CH 2 - SO 3 H
рН артқанда протондар рет-ретімен бөлінеді:
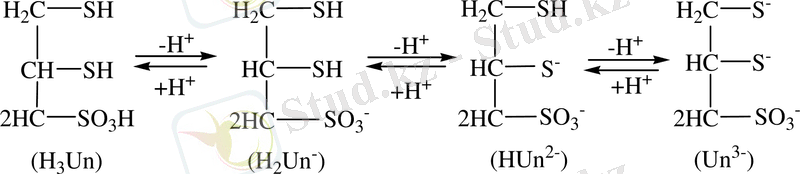
Сулы ерітінділердегі диссоцациялану константалары
К 1 = К 2 =(1, 44 + 0, 18) *10 -9 К 3 =(6, 35 + 2, 30) *10 -14
Унитиолдың құрғақ препараты атмосфералық әсерлерге тұрақты, көп жылдарға дейін сақтауға болады. Бес жылда SН-тың құрамы 1%-ғана төмендейді екен[6] . Сілтілік ортадағы сулы ерітінділері тұрақсыздану болады. Унитиол тек үшінші суткада (сөткеде) тотыға бастайды. Тотықтырғыштарымен әрекеттескенде унитиолдың тотығуы бірнеше сатыда өтеді.
Тотығу процесінің схемасы:
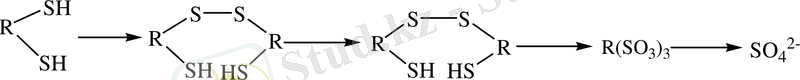 унитиолди сульфид тетрасульфид сульфакислота сульфат
унитиолди сульфид тетрасульфид сульфакислота сульфат
ионы
Унитиолдың тотықтырғыштармен әрекеттесуі аса маңызды орын алады [2] . Стандартты тотығу-тотықсыздандыру потенциалы + 0, 5В және одан жоғары болса, унитиолмен төменгі тотығу дәрежесіне дейін тотықсызданады.
Сульфгидрлі топтағы күкірттің бөлінбеген жұп электрондарының қатысуымен унитиол берік хелатты комплекс түзеді. Осыған байланысты унитиолдың ауыспалы топ элементтерімен әрекеттесіп, қосылыс түзуі ғылым мен техникада аса маңызды орын алады.
І. 2. Платинаның комплесті қосылыстары
Платинаның заряды жоғары, иондық радиусы кіші және толмаған d -орбиталі бар, сол себепті күшті комплекстүзгіш металл боп саналады.
Платинаның (0), (ІІ), (VІ), (V) комплексті қосылыстар белгілі, ал платина (ІІІ) қосылысы белгісіз деп айтуға болады. Бүгінгі таңда немесе көп зерттелген платинаның комплексті қосылыстары Рt(ІІ) және Рt(ІV) . Платинаның (ІІ) комплексті қосылысының құрылысы квадрат боп келеді, ал Рt(V) және Pt(IV) сирек кездеседі және оның құшрылысы туралы айту қиын. Бірақ платинаның кейбір қосылыстары әлсіз байланыстар арқылы октаэдр конфигурациясын түзеді деген жорамал - мәліметтер бар. Ерітіндіде бұлардың орнына еріткіш молекуласы ауысуы - мүмкін [7] . Лигандтармен орын басу реакцияларында атакаға (өзгеріске) осы октаэдр құрылысы ұшырайды. Қазіргі уақытта металлдардың көптеген лигандтары оксиальды күйімен (положения) әрекетттесетіні дәлелденіп отыр [8] .
Атом лигандтарының байланыспайтын электрондармен әрекеттесуі [Pt(NH 3 ) 2 Cl 2 ] сияқты комплекстердегі N-Н тобының валенттік және деформациялық тербелістері нәтижесінде іске асады. Бұл (аномалия) ауытқуды ғалымдар [7] d xy несеме d xz металл орбитальдарымен Н атомдары арасындағы сутектік байланыс арқылы деп жорамалдап түсіндіреді. Pt(ІІ) комплекстері кинетикалық және термодинамикалық тұрғыдан қарағанда инертті, оларды Pt(IV) комплексіне дейін тотықтыруға болады (бастапқы конфигурациясын сақтай отырып ) .
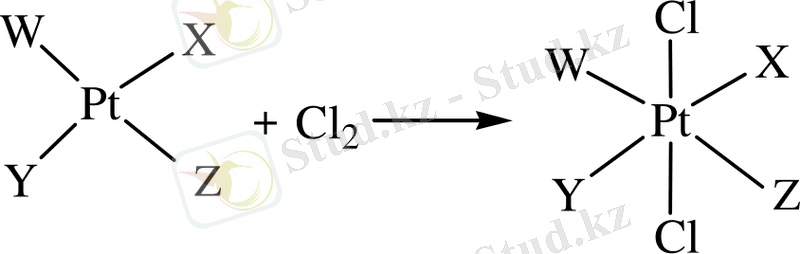
Төртмүшелі циклді мұндай комплексті қосылыстардағы электрондар металл атомының толтырылған d xy және d xz орбитальдарының лигандаларының осындай толтырылмаған орбитальдарымен бүркесуі нәтижесінде тұрақты бола алмайды.
Тотығу дәрежесі төртке тең платинаның қосылысы оңай түзіледі. Pt(ІV) комплексінің құрылысы октаэдр пішінді екені белгілі. Платинаның (ІV) зерттелген қосылыстарының ішіндегі ең көп тараған түрі аминдермен орын алмасқан [PtAm 6 ] X x типтес комплекстері. Бұл комплекстердің құрамына түрлі аминдер (аммиак, гидрзин, гидроксиламин және этилендиамин) және кейбір топтар (галогендер, тиоцинаттар, гидроксилдер, нитротоптар) да кіреді.
Әртүрлі бірядролы комплекстер де белгілі, атап айтқанда: [ML 4 ] 2+ , [ML 3 X] + цис - және транс -[ML 2 X 2 ] ; [MLX 3 ] - бұл жерде M-Pt(II), L - бейтарап лиганд, X - бір зарядты анион. Pt(ІІ) азотқа, галаогендерге, цианидтерге, фосфарға, күкіртке үлкен тартымдылық (сродство) білдіретіні белгілі. Оттегі мен фторға тартымдылығы онша үлкен емес.
Металл атомдары мен донор атомдарының арасындағы байланыстың мықтылығы толтырылған dπ - орбитальдарының (d xy, d xz, d yz ) бүркелуі нәтижесінде түзілгендіктен.
Бір ядролы комплекстерден Pt (ІІ) басқа, екі ядролы комплекстер де белгілі:
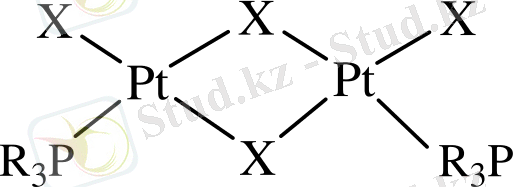
Мұндағы Х - СІ - , Br - , CNS -
Pt (ІV) қосылысының типтік координациясы октаэдр, координациялық саны 6. Pt (ІV) кинетикалық инертті тұрақты комплекс түзеді.
(SO, N 2 H 4 т. с. с. ) қатысуымен Pt (ІV) молекуласының конфигурациясы өзгермей, платина (ІІ) дейін тотықсызданады. Мұнда октаэдрлі құрылыстағы Pt(ІV) комплекстің үш координатасының тек біреуіндегі ғана лиганд бөлініп қалады.
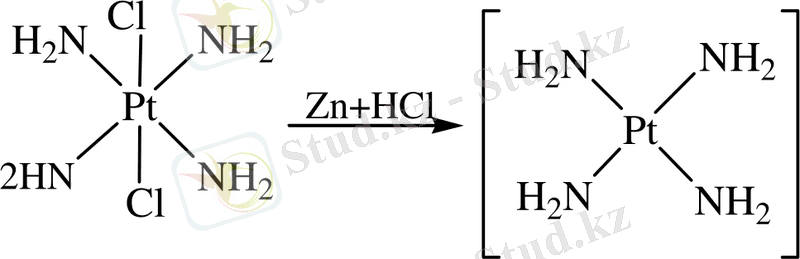
Металл лигандтары мен унитиол арасындағы координация нәтижесінде түзілген Pt(ІІ) де, Pt(ІV) де циклді (хелатты) комплексті қосылыс болып табылады.
Ертеректе [9-11] платинаның хлоридті комплекстерінің унитиолмен әрекеттесуі зерттелген. Зерттеу нәтижесінде платинаның унитиолмен комлекс түзуі күрделі екені және ол ортаның қышқылдығына тәуелді екені, метал: лиганд қатынасына тәуелді екені анықталған.
Спектрофатометриялық зерттеулердің қорытындысы бойынша қышқыл ортада комплексті қосылыстың құрамы мен беріктігіне өте қолайлы және бұл ортада (қышқыл) процесс тезірек жүретіні байқалады.
Түзілген комплексті қосылыстың құрамын әртүрлі әдістремен (потенциометриялық, спектрофотометриялық) анықтағанда, комплекс түзілу платина: унитиолдың мольдік қатынасы 1:1 болғанда қышқыл ортада да, сілтілік ортада да түзіледі екен. Қышқыл ортада түзілген қосылыстың түсі қара қоңыр, ал сілтілік ортада түзілген қосылыстың түсі ашық сары. Түзілген комплексті қосылыстардың беріксіздік константасы (25 0 C - да және иондық күш 1 ге тең болғанда μ=1) әртүрлі орталарда есептелген.
Хлорлы қышқыл ортада К=(1, 93±0, 21) *10 -10
Гидроксид калий ортасында К=(0, 62±0, 10) *10 -5
Калий нитраты ортасында K=(1, 61±0, 45) *10 -9
Унитиолмен бір валенттіге дейін тотықсызданатын мыс (ІІ) және алтын (ІІІ) сияқты, ерітіндідегі платина (ІV) екі валеттіге дейін тотықсызданып, сосын барып Pt (ІІ) унитиолмен әрекеттеседі.
Синтезделген платинаның (ІІ) қатты комплекстерін термографиялық әдіспен зерттегенде, су молекуласының ең көп мөлшері бейтарап ерітіндіден бөлінген қатты Pt(ІІ) комплексті қосылыстың құрамында екені көрсетілген. Сілтілік ерітіндіден бөлінген комплекстің құрамында екі молекула су, ал қышқыл ерітіндіден бөлінген комплекстің құрамында үш молекула су болатыны айқындалды. Алғышқы қыздыруда эндоэффект, сосын су молкуласы бөлінеді, одан кейін тотығады және қосылыс ыдырайды.
Авторлар [12] берік координациялық байланыс түзуге унитиолдың SO 3 - тобы тікелей қатыспайды деп тұжырымдайды: координация унитиолдағы сульфгидрлі (SН) топтағы екі күкірт атомы арқылы іске асып, бес мүшелі металл циклі түзіледі.
Химиялық анализ, термограмма, ИК спектр, ренгенограмма синтезделген комплексті қосылыстардың структуралық формуласын (Pt(ІІ) :Un, мольдік қатынасы 1:1(І) ; 1:2 (ІІ) ) . Төмендегідей жорамалдайды:
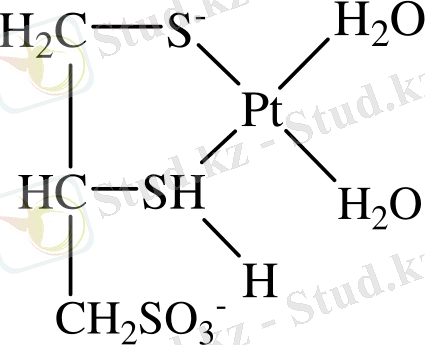 және
және

І ІІ
Жоғарыда көрсетілген (есептелген) комплексті қосылыстардың белгісіздік константалары (10 -5 ÷ 10 -10 ) бойынша қорытынды былайша жасалынады: платинаның унитиолатты комплекстері өте берік, сары түсті және спектрдің көрінетін аймағындағы сәулелерді сіңіреді, бұл платинаны (ІІ) спектрофотометриялық әдіспен анықтауда унитиолды аналитикалық реагент ретінде пайдалануға мүмкіншілік береді
І. 3. Платинаның фотоколориметриялық әдіспен анықтау
Платинаны фотоколориметриялық әдіспен анықтау өте кең интервалда жүргізіледі, концентрациясы жүздік үлестен жүз микрограмм милилитрге дейін мкг/мл (кесте І) . Өте сезімтал әдіске диацетоимид (0, 02-0, 007 мкг/мл) және нитрофенол (0, 04 мкг/мл және оданда төмен) арқылы анықтаулар жатады. Платинаның көп мөлшерін анықтауға мүмкіншілік беретін әдістердің ішіндегі қолайлысы тиосемикарбазидпен (100-1000 мкг/мл) анықтау болып табылады. Платинамен боялған қосылыс түзілетін реагент ретінде хлорлы қалайы және құрамында азот пен күкірт бар органикалық қосылыстар, фенилдиамин (1-12 мкг/мл), антронил қышқылы (4-64 мкг/мл), фенилтиосемикарбозид (0, 07-19 мкг/мл) қолданылады. Және де платинаны анықтау үшін комплексті галогенидтердің бояулары да пайдаланылады.
Бірақ бұл әдістердің кемшіліктері көп: бөтен иондар әсеріне сезімтал, температура мен қышқылдылыққа да сезімтал.
Жоғарыда аталған реагенттердің барлығыдерлік (почти) платиналық металдармен (Au, Cu, Ni, Co, Fe) боялған қосылыс түзеді. Бұл әдістің тағы да негізгі кемшіліктері: қиын немесе күрделі, қыздырылған және улы органикалық еріткіштерді қолдануы.
Кесте І
Платинаны спектрофотометриялық әдіспен анықтау
t, (
С 0 )
λ
нµ
ІІ. ЭКСПЕРИМЕНТТІК БӨЛІМ
ІІ. 1. Негізгі заттардың сипаттамасы
Жұмыста қолданылғандар:
- Дистелген су;
- «х, ч» маркалы унитиол;
- Концентрлі минерал қышқылдар;
- Күкірт қышқылы (тығыздығы 1, 83)
- Тұз қышқылы (тығыздығы 1, 93) - керекті концентрация сұйылту арқылы дайындалады;
- Концентрлі сірке қышқылы:
- 1 М NаОН ерітіндісі;
- Платинахлорлысутек қышқылынан алынған калий хлорплатинаты арқылы синтезделген платинаның комплексті тұзы.
ІІ. 2. Эксперимент методикасы
ІІ. 2. 1 Ерітіндідегі платина (ІІ) - унитиол системасын спектрофотометриялық әдіспен зерттеу
Бұл әдіс Бугер-Ламберт-Бер заңына сүйенеді, бұл заңы бойынша: боялған ерітінді қабаты арқылы өткен жарық интенсивтілігінің түскен жарық интенсивтілігі, ерітінді қабатының қалыңдылығы және концентрация аралықтарындағы байланыс төмендегі теңдеу бойынша өрнектеледі:
I = I 0 *10 -KCl (1. 1)
Мұндағы К-сіңіру коэффициенті, ол еріген заттың табиғатына тәуелді және температура мен жарық толқынының ұзындығына тәуелді.
 Сурет 1. Оптикалық тығыздықтың
Сурет 1. Оптикалық тығыздықтың
ерітінді концентарциясына тәуелділігі.
Егер концентрация моль/л - мен өрнектеліп, ℓ - сантиметрмен өрнектелсе, онда К-жарық сіңірудің молярлы коэффиценті деп аталады да, ε λ - мен белгіледі. (1. 1) теңдеу мынадай түрге енеді:
I = I 0 *10 - ελ C * ℓ (1. 2)
- және (1. 2) теңдеулерін логарифмдеп негізгі фотометриялық шамаларды алуға болады.
D = ε λ * c* ℓ (1. 3)
Бұл (1. 3) теңдеу бойынша ерітіндінің оптикалық тығыздығы жарық сіңірудің молярлы коэффиценіне, ерітіндінің концентрациясы мен қалыңдығына тура пропорционал деп, жарық сіңірудің негізгі заңы сақталады.
Оптикалық тығыздықтың концентрацияға тәуелділігінің графигі түзу сызықты тәуелділік болады (сурет 1) .
- және (1. 3) теңдеулер монохроматты жарыққа арналған, монохроматты жарық деген белгілі бір толқын ұзындығы бар, арнайы монохромат деген оптикалық қондырғыдан бөлінетін жарық. Фотоколориметриялық зерттеулерде интенсивтілікті монохроматты жарықта емес, полихроматты жарықта өлшейді, яғни толқын ұзындығының өте кең интервалында 200-1000 нм. Бұл жағдайда (1, 3) теңдеудегі ελмолярлы коэффициенттің орнына, жарық сүзгіштерге (светофильтр) тәуелді жарық сіңірудің орташа молярлы коэффиценті қолданылады [17] .
ІІ. 2. 2. Платина (ІІ) унитиол әрекеттесуінің мольдік қатынасын анықтау
Үздіксіз өлшеу әдісі (изомолярлы серия) .
Бұл әдісті ұсынған Остромысленский және Жоба [18], кейінірек А. К. Бабоко өзінің қызметкерлерімен әдісті кең таратты [17] .
Әдіс әрекетесетін заттардың изомолярлы концентрацияларының қатынасы түзілген комплексті қосылыстың ең жоғарғы (мах) мәніне сәйкес келуін анықтауға негізделген. Түзілген комплекстің ерітінді құрамына тәуелділігінің қисық сызығы экстрмальді нүктемен сипаталады. Бұл нүкте төмендегі реакция бойынша түзілген комплексті қосылыстың Мm Рn мүмкіндігінше ең жоғары концентрациясына сәйкес келеді.
mM+nP=MmPn
Реакцияның күйі стехиометриялық коэффицентпен және m және n байланысты :
C p n
X max = =
Cm + Cp m+n
Мұндағы С м және С р - әрекеттесуіші компоненттердің М және Р алғашқы концентрациясы.
Анализді орындау үшін концентрацияларын бірдей етіп екі ертітіндіні дайындайды, сосын төмендегідей 1:9, 2:8, 3:7, 4:6, 5:5, 6:4, 7:3, 8:2, 9:1 қатынас бойынша араластырады. Араластырғанда жалпы көлемі (V m + V p = const) тұрақты болуы керек.
Оптикалық тығыздықты ерітіндінің белгілі бір рН мәнінде және иондық күштің тұрақты мәнінде өлшейді. Ерітіндінің рН -ын тұрақты бір қалыпта ұстап тұру үшін буферлі ерітінді қолданады, ал буферлі ерітіндімен компонеттер реакцияға түсіп, ешқандай комплекс түзілмеген жөн.
Оптикалық тығыздықтың дұрыстығына немесе дәлдігіне күмән болмас үшін, оны бірнеше толқын ұзындықтарда өлшейді, оны светофильтрлер (жарықсүзгіз) арқылы іске асыруға болады. Оптикалық тығыздықты өлшеп болғаннан кейін. Оның концентрацияға немесе изомолярлы сериядағы компоненттердің көлеміне тәуелдігінің графигін тұрғызады.
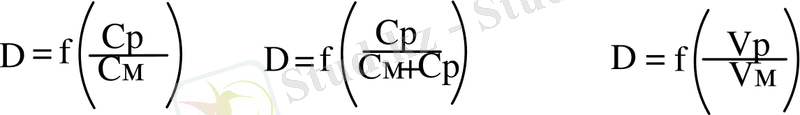
Графиктен (сурет 2) изомолярлы серия қисықтарының ең жоғарғы (мах) мәнін анықтайды.
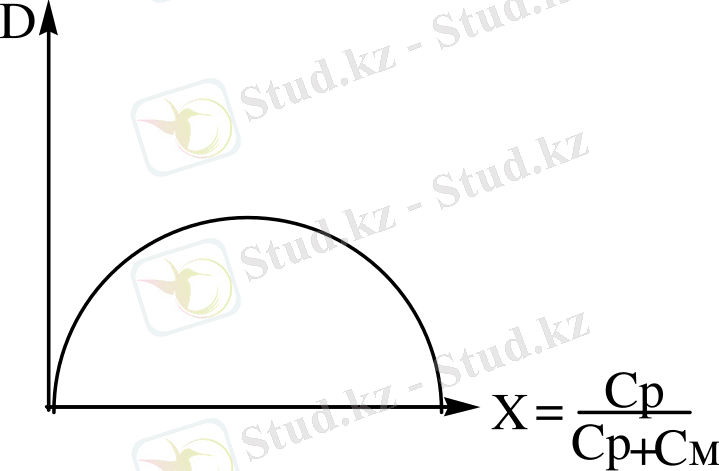 Сурет 2. 2. Оптикалық тығыздықтың комплекс құрамына тәуелділігі.
Сурет 2. 2. Оптикалық тығыздықтың комплекс құрамына тәуелділігі.
Түзілген комплексті қосылыстың құрамы ең көп болғанда, жарық сіңірудің де мәні ең жоғары болады. Сол себепті изомолярлы серия компоненттерінің көлемдік қатынасы әрекеттесуші заттардың стехиометриялық қатынасына тең.
Егер изомолярлы қисықтағы жарық сіңірудің ең жоғарғы мәні анық болмаса, онда экстраполяция тәсілі қолданылады: бастапқы нүктеден бастап екі қисыққа жанама түзу сызық қиылысқанға дейін жүргізіледі. Қиылысқандағы нүкте жоғарыда көрсеткен экстремальды нүктеге сәйкес келу керек.
Жалпы жағдайда, таңдап алынған толқын ұзындығында жарық комплексті қосылыспен бірге М m Р n және алғашқы компоненттерді де сіңіреді, бұл кезде оптикалық тығыздықтың аудитивтіліктен ауытқуының тәуелділігінің графигін тұрғызады. ΔД =Д см -Д м -Д R (мұнда Д см - ерітіндідегі барлық компоненттердің оптикалық тығыздықтарының қосындысы; Д м және Д R - ертінідідегі компоненттердің оптикалық тығыздықтары) .
Егер әртүрлі концентрациялы ерітінділер дайындалып, олардың
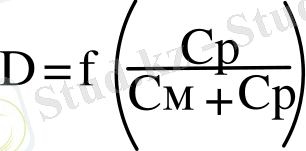
графигіндегі максимумдары бір-біріне сәйкес келсе, ол комплексті қосылыстардың құрамы тұрақты деген сөз.
Өкіншке орай, изомолярлы серия әдісі әмбебап (универсальный) әдіске жатпайды. Ол тек төмендегі жағдайларда ғана қолайлы [18] :
- Әрекеттесуші заттардың арасындағы химиялық реакция қосымша процесстерсіз (гидролиз, ассоциация т. с. с. ) тек тура және қатаң берілген теңдеу бойынша өту керек.
- Жүйеде тек бірақ комплексті қосылыс түзілу шарт.
- Ерітіндінің иондық күші тұрақты болуға тиіс.
Бірақ бұл жағдайларда изомолярлы серия әдісі құрамды анықтайтын графикалық тәсіл болғандықтан тиімсіздеу, себебі қисықтардың сырқы пішіні түзілетін комплекстің беріктігіне, әрекеттесуші компонеттердің концентрациясына және стехиометриялық коэффиценттердің шамасына тәуелді [18] .
Изомолярлы серия бойынша өте берік комплексті қосылыстарды зерттегенде екі түзу сызықтың қиылысындағы ең жоғарғы (максимум) мәні комплекстің түзілу константасына да, әрекеттесуші компонеттердің бастапқы концентарцияларына да тәуелсіз. Ал, беріктігі нашар комплексті қосылыстардың мзомолярлы қисықтарының максимумын анықтауда біраз қиыншылықтар кездесуі мүмкін.
Қисық сызықтағы максимумды анықтаудағы тағы бір түйінді мәселе жоғары координациялы қосылыстардың түзілуі немесе бөлшек стехиометриялық коэффиценттері бар көп ядролы қосылыстардың түзілуі.
Бұндай қосылыстың қисық сызығындағы максимум изомолярлы диаграмманың шетіне ығысып кетеді де, оны анықтау қиынға соғады. Сондықтан экспериментте кеткен аздаған қателіктер анализ қорытындысына кері әсер етеді. Мұндай жағдайда Л. П. Адамович [18] әдісі немесе аналитикалық әдіс қолданылады[18] . Соңғысында көмескі экстремаль нүктені алып тастайды да, изомолярлы қисықтың екі бұтағының теңдеуін есептейді, сосын ізделіп отырған көлемдер қатынасын анықтайды.
Сенімді қорытынды алу үшін әртүрлі концентрациялы ертінділер дайындайдап, олардың жарық сіңіруін де түрлі толқын ұзындықтарында өлшеген жөн.
Изомолярлы серия әдісінің теориясын терең зерттеп, оның мүмкіншіліктерін түрлі реакцияларға қолданған М. П. Комар [18, 19] . Автор қарастырылған тепе-теңдіктердің күрделігі.
Қарастырылып отырған тепе-теңдіктің күрделенуі әртүрлі қосымша процестердің әсерінен, ол кезде изомолярлы серия әдісі бойынша түзілген комплексті қосылыстың формуласындағы стехиометриялық индесті анықтау қиыншылыққа соғады. Сонымен қатар реакция нәтижесінде түзілген өнімнің құрамының дәлдігі де кей жағдайда күмән туғызады.
Мысалы, мына реакция:
МР + Р І = МР + Р және МР + Р І = МРР І
немесе
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz