Биология мамандығына арналған Жалпы химия пәнінің зертханалық сабақтары: әдістемелік нұсқаулық


Ы. АЛТЫНСАРИН АТЫНДАҒЫ АРҚАЛЫҚ МЕМЛЕКЕТТІК ПЕДАГОГИКАЛЫҚ ИНСТИТУТЫ
Жаратылыстану және ақпараттандыру факультеті
Химия, биология және география кафедрасы
«Бекітемін»
Кафедра меңгерушісі
Қоразбекова К. У

«16» маусым 2018 ж.
Зертханалық сабақтарды орындауға арналған әдістемелік нұсқаулық
Жалпы химия пәні бойынша
«5В011300»-Биология мамандығына арналған
Зертханалық сабақтарды орындауға арналған әдістемелік нұсқаулықтың құрылымы
№ 1 Зертаханалық сабақтың тақырыбы: Қауіпсіздік техникасының ережесі.
Зертаханалық сабақ тапсырмасы:
1. Зертханада қауіпсіздік сақтау ережелері және алғашқы көмек.
Химиялық зертханада (лабораторияда) жұмыс істеу қауіпсіздік шараларын толық сақтауды талап етеді. Қауіпсіздік сақтамау әдетте өрт, қопарылыс және т. б. келеңсіз жағдайға соқтырады.
Сондықтан зертханада (лабораторияда) жұмыс жүргізетін студенттер немесе басқа да адамдар мынандай ережелерді қатаң сақтауы тиіс:
1. Зертханалық тапсырманы орындау кезінде оқытушының нұсқауларын сақтап, жұмыс желісінен ешқандай ауытқымау керек.
2. Сақтық ережесін оқып, оқытушыдан рұқсат алған студенттер ғана зертханалық жұмысқа жіберіледі. Қауіпсіздік техникасымен танысқандығы жөнінде арнайы журналға жазылып, қол қояды.
3. Ерітінді құйылған немесе құрғақ зат салынған құтының аузы әрқашан жабық болсын. Оны пайдаланған кезде ғана ашу керек.
4. Құтылардың тығындарын, сонымен қатар ерітінді алатын тамызғыштарды ауыстырып алмаңдар.
5. Реактивтің артық мөлшерін құтыға немесе ыдысқа қайта құюға, салуға болмайды.
6. Оңай тұтанатын заттармен істелінетін жұмысты жанып тұрған оттан алыс жүргізу керек.
7. Реактивтерді құйған кезде ыдысқа еңкейіпқарауға болмайды. өйткені реактив киімге, бетке шашырауы мүмкін.
8. Сұйықтарды қыздырған кезде пробирканың аузын өзіне немесе қасындағыларға қаратуға болмайды.
9. Ыстық заттарды қысқашпен ұстау керек.
10. Улы және өткір иісті заттармен жұмыс тек желдеткіш шкфта жүргізіледі.
11. Концентрлі қышқылмен және сілтілермен жұмыс істегенде аса мұқият болу керек. Концентрлі суға қышқыл қосады. Керісінше істеуге болмайды.
12. Концентрлі қышқыл мен сілтілер қалдығын раковинаға төгуге болмайды. Оларды арнайы ыдысқа құйып, желдеткіш шкафта сақтайды.
13. Реактивтердің дәмін білуге, зертханада тамақтануға болмайды.
14. Жұмыс аяқталғанда жұмыс орнын тазалап, кезекшіге не зертханашыға өткізіліп, қолды жақсылап жуу керек.
15. Зертханада алғашқы дәрігерлік көмек көрсетуге арналған дәріқалта (аптечка) болу керек.
Қолдың немесе дененің жарақаттанған жерін сутегі асқын оксидінің 3%-тік ерітіндісімен өңдеп, йод не зеленка жағады.
Қышқылға күйген жерді сумен жақсылап жуады, натрий гидрокарбонаты (ас содасы) ерітіндісімен нейтралдап, вазелин жағады.
Ыстыққа күйген теріге глицерин не этил спирті жағылған мақта қою керек. өте қатты күйген жағдайда концентрлі калий перманганатының ерітіндісі қолданылады.
Көзге қышқыл немесе сілті тиген кезде сумен жақсылап жуады. Қышқыл тисе натрий гидрокарбонатының, ал сілті тисе бор қышқылының ерітінділермен өңдейді.
Зертханада кездескен барлық келеңсіз жағдайларды зертханашыға не оқытушыға айту керек.
Зертханалық жұмыс жүргізу кезінде әр студенттің зертханалық дәптері (журналы) болады. Оның сыртында студенттің аты-жөні, факультеті, курсы, топ нөмірі жазылады. әр жұмыс бойынша есеп толтырылады. Есеп мынандай ретте жазылады:
1. Жұмыстың аты, нөмірі және жүргізілген мерзімі (айы, күні) ;
жұмыстың мақсаты;
әр тәжірибенің реті және аты;
тәжірибеде байқалған құбылыстар - тұнба түсуі, еруі, ерітінді түсінің өзгеруі, газ түзілуі және химиялық реакциялардың теңдеулері, пайдаланған аспаптардың сызба нұсқасы (схемасы), есептеулер, нәтижелерді кесте не қисық (график) түрінде кескіндеу;
қорытыңды.
2. Зертханалық журнал жұмыс кезінде толтырылады. Жұмыс соңында журналды оқытушы тексеріп, қол қояды.
2. Зертханалық жабдықтары және химиялық ыдыстармен танысу.
Химиялық зертхана түрлі аспап-құралдармен жабдықталады. Зертхана жабдықтарына столдар, желдеткіш шкафтар, реактивтер қоятын шкафтар, дистилляторлар, кептіргіш шкафтар, қыздырғыш пештер, таразылар, микроскоптар, Кипп аппараты, эксикаторлар, ыдыстар және т. б. жатады.
Зертханалық жұмыс жүргізу үшін әр түрлі қысқыштары мен сақиналары бар штативтер пайдалынады.
Студенттер зертханалық жұмыс жүргізу кезінде әр түрлі аспаптармен және приборлармен нақты танысады.
3. Таразылар және олармен жұмыс істеу.
Химиялық тәжірибелер жүргізу үшін стандартты зертханалық ыдыстар қолданылады. Оларға түбі дөңгелек, жайпақ конус колбалар, химиялық стақандар, сүзгіш воронкалар, арнайы краны бар бөлгіш және тамшылатқыш воронкалар жатады.
Зертханада кәрден (фарфор) ыдыстар да кеңінен қолданылады: стақакн және кружка, қайнатып буландыруға арналған табақша, қыздыруға арналған тигаль, келі-келсабымен, шпатель және қасық.
Өлшеуіш ыдыстар сұйықтар мен ерітіңділердің көлемін өлшеу үшін қажет. өлшенетін заттың дәлдігіне орай өлшеуіш цилиндрлер немесе мензуркалар, тамызғыштар, бюреткалар, өлшеуіш колбалар қолданылады.
Кейбір газдарды алу үшін Кипп аппараты қолданылады. Бөлінген газдарды газометрлерде жинап, сақтайды.
Газдарды тазартып, құрғат үшін тазартқыш құтылар және құрғатқыш колонкалар пайдалынылады. Олар қыздырылған кальций хлориды, магний сульфаты, құрғақ сілті, концентрлі күкірт қышқылы және т. б. су сіңіргіш заттармен толтырылған.
№ 2 Зертаханалық сабақтың тақырыбы: Көміртегі (IV) оксидінің мольдік массасын анықтау.
Зертаханалық сабақ тапсырмасы:
Жұмыстың мақсаты: газдың мольдік массасын анықтаудың бір әдісімен таныстыру, өлшеп үйрету және газ заңдарын қолданып, есептеулер жүргізу.
Реактивтер мен құрал жабдықтар: Кипп аппараты, технологиялық таразы; өлшеу цилиндр; тығыны бар түбі жайпақ колба (200-250мм) ; термометр; барометр; тұз қышқылы (1/3) ; мәрмәр.
Жұмыс барысы:
Көміртегі (IV) оксидін мәрмәрге (СаСО 3 ) тұз қышқылымен әсер ету арқылы Кипп аппаратында алады. Түзілген көміртегі оксидін тазартып, құрғату үшін натрий гидрокарбанаты ерітіндісі және концентрлі күкірт қышқылы арқылы өткізеді.
Таза құрғақ колбаны тығындап, 0, 01г дәлдікпен термохимиялық таразыда өлшеу керек. Ауасы бар колбаның массасын жазады - m 1 .
Кипп аппаратында алынған көміртегі (IV) оксидімен колбаны толтырады (3-4 мин) . Газ жүретін түтікті жайлап колбадан алып оны тығындап өлшейді. Колбаны газбен толтыру мен өлшеуді 2-3 рет тұрақты салмаққа дейін қайталайды.
Колбаның көміртегі (IV) оксидімен массасын жазады - m 2 .
Колбаға белгіге дейін су құйып, ол судың көлемін цилиндрмен өлшеп, колбаның көлемін анықтайды. Колба көлемін жазады - Ү. Тәжірибе кезіндегі темперптураны өлшеп (t 0 C), оны абсалют температураға (Т 0 К) айналдырады (Т = t 0 + 273) .
Барометр бойынша атмосфералық қысымды өлшейді Р, кПа. Менделеев - Клапейрон теңдеуі бойынша Р, Ү, Т -мәндерін біле тұра, колбадағы ауаның массасын (m ауа ) есептейді:
m ауа = M ауа *P*Y/RT = 29*P*Y/RT;
Колбадағы көміртегі (IV) оксиді массасын (m со2 ) есептейді:
m со2 = m 2 - (m 1 - m ауа )
Газ көлемін (Ү) мына теңдеу арқылы қалыпты жағдайға келтіреді:
мұндағы Т -температура, К; Ү 0 - Т = 273 К және қысым Р - 101, 3 КПа болғандағы көлем.
СО 2 - нің мольдік массасын мына жолдармен есептеңдер:
- Ауа бойынша салыстырмалы тығыздығы арқылы:
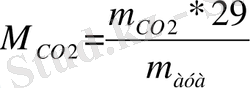
- Газдың мольдік көлемі бойынша:
Осы жолмен есептелген мольдік массасын ортақ мәнін 0, 01 г/м тәж дәлдікпен есептеңдер.
СО 2 - нің теориялық мәнін (М теор ) біле тұра, тәжірибенің салыстырмалы қателігін процентпен есептеңдер:
Қатенің% =
Кипп аппараты мен сүзгіш ыдыстарда жүретін химиялық реакциялардың теңдеулерін жазыңдар.
Тапсырма сұрақтары:
1. Салыстырмалы молекулалық масса деп нені айтады және оны қалай есептейді? Екі мысал келтіріңдер.
2. Мольдік масса деген не? Мольдік массаның өлшемі қандай бірлік? 3-4 мысал келтіріңдер.
№ 3 Зертаханалық сабақтың тақырыбы: Металл эквивалентінің мольдік массасын сутегін ығыстыру әдісімен анықтау.
Зертаханалық сабақ тапсырмасы:
Жұмыстың мақсаты: металл эквивалентінің мольдік массасын қосылыстарынан сутегін ығыстыру арқылы анықтау әдісімен танысу.
Реактивтер мен құрал жабдықтар: металл эквивалентінің мольдік массасын анықтауға арналған аспап; аналитикалық таразы; термометр, барометр; өлшеуіш цилиндр (25 - 50мл), химиялық стақан (50мл), өлшенген маталл (шамамен 0, 2г), тұз қышқылы (20%) .
Жұмыс барысы:
Аспапты жинап, оның герметикалығын (ауа жібермеуін) тексеріңдер. Ол үшін пробирканың тығынын ашып, теңестіргіш ыдыс арқылы бюреткадағы судың деңгейін нөлдік белгіге жақындатады, содан соң пробирканың тығынын жауып, теңестіргіш ыдысты төмен (10 - 15см) түсіріп, штатив сақинасына орнатады. Егер осы кезде бюреткадағы су деңгейі тұрақты ьолса, онда аспап ауа жібермейді (герметикалы) . Аналитикалық таразыда металл (Mg, Zn, Al) бөлшегін өлшейді. Реакция жүргізетін пробиркаға 2 - 3мл тұз қыщқылын құяды. Пробирканы жантайтып тұрып, өлшенген металды оның қабырғасына салады. Металл қышқылмен жанаспауы керек. Сол күйде пробирканың тығынын жабады. Теңестіргіш ыдыстағы судың деңгейі мен бюреткадағы судың деңгейін тең ұстап, бюреткадағы газдың алғашқы көлемін жазып алады. Металды қышқылға түртіп түсіріп, сутегінің бөлініп, суды бюреткадан ығыстырғанын бақылайды. Металл толық еріп ерітінді суығаннан кейін теңестіргіш ыдыстағы судың деңгейі мен бюреткадағысудың деңгейін теңестіріп, бөлінген су сутегінің көлемін анықтайды. Ол бюреткадағы судың реакциядан кейінгі деңгейі мен алғашқы деңгейінің айырмасы болады. Атмосфералық қысымды Р атм кПа; тәжірибе температурасын t 0 тәж. С өлшейді; кесте бойынша тәжірибе температурасындағы су буының қысымын (1 - қосымша ) - Р H2O , кПа және сутегінің қысымын Р H2 /Р атм -Р H2O /, кПа табады.
Бөлінген сутегінің көлемін қалыпты жағдайға айналдырады:
Мұнда Ү-тәжірибеде бөлінген сутегінің көлемі: Р H2 - сутегінің парциалды қысымы. Осы көлем бойынша металл эквивалентінің мольдік массасын есептейді:
m э2 металл - Ү 0 мл сутегін ығыстырады
М ЭКВ /Ме/ - 11200 мл
Берілгендердің бәрін кестеге түсіріңдер:
Тапсырма сұрақтары:
1. Заттың эквиваленті деп нені айтады?
2. Эквиваленттің мольдік массасы деген не?
3. Қышқылдарың, негіздердің, тұздардың эквивалентінің мольдік массасын қалай деп есептейді?
4. Эквивалент заңына анықтама беріңдер.
5. Эквивалент заңының математикалық өрнегі қандай?
№ 4 Зертаханалық сабақтың тақырыбы: Бейорганикалық қосылыстардың негізгі кластары.
Зертаханалық сабақ тапсырмасы:
1. Оксидтердің, негіздердің, қышқылдардың қасиеттері.
Жұмыстың мақсаты: бейорганикалық заттардың жіктелуін, қасиеттерін және олардың арасындағы генетикалық байланыстарды оқып-үйрену.
Реактивтер мен құрал жабдықтар: мырыш сульфаты, алюминий сульфаты, кесегін муфель, фарфор табақша, фенолфталеин, кальций оксиді, мыс оксиді, натрий силикаты, тұз қышқылы, натрий ацетаты, H 2 SO 4, натрий гидроксиді, күміс нитраты, сұйытылған күкірт қышқылы, барий хлориді.
1-тәжірибе. Кальций оксидін және мыс пен кальций гидрооксидтерін алу.
Бордың кішкене кесегін муфель пешінде қыздырып, суытады. Оны фарфор табақшаға салып, бірнеше тамшы су құяды. Не байқадыңдар?
Үстіне 2-3 тамшы фенолфталеин ерітіндісін тамызу керек. Ерітінді қышқылдық немесе сілтілік ортаны көрсете ме?
Борды қыздырғанда және одан түзілген өнімнің сумен әрекеттескенде жүретін реакция теңдеулерін жазыңдар. Соңғы өнімнің электролиттік диссоциациясын жазып, қосылысты атаңдар.
Мына сұрақтарға жауап беріңдер: 1. Барлық негіздік оксидтер сумен әрекеттесе ме? қайсылары әрекеттеседі? 2. Мыс оксидін сумен әрекеттестіріп, мыс гидроксидін алуға бола ма? Мыс сульфатынан мыс гидроксидін тәжірибе жүзінде алып, оның амфотерлі гидроксиді емес, негіз екендігін дәлелдеңдер. Реакция теңдеуін жазыңдар.
2-тәжірибе. Амфотерлі гидроксидтердің алынуы және қасиеттері.
Екі пробирка алып, біреуіне 3-5 мл, мырыш сульфаты, екіншісіне сондай мөлшерде алюминий сульфаты ерітінділерін құйыңдар. Екеуіне де араластырып тұрып, аморфты тұңба түзілгенше күйдіргіш натрий ерітіндісін қосыңдар. Реакция теңдеуін жазыңдар.
Мырыш және алюминий гидроксидтерінің амфотерлігін көрсететін тәжірибелер жасаңдар. Жүретін химиялық реакция теңдеулерін жазыңдар. Түзілген қосылыстарды атаңдар.
Амфотерлі гидроксидтердің негіздерден айырмашылығын мыс және мырыш гидроксидтері қасиеттерін салыстырып, іс жүзінде дәлелдеңдер. Басқа амфотерлі қосылыстарды мысалға келтіріңдер.
3-тәжірибе. Қышқылдар, олардың алынуы және қасиеттері.
1. Кремний қышқылының алынуы. Пробиркаға 10 мл натрий силикаты ерітіндісін құйыңдар да, оған тамшылатып тұз қышқылын қосыңдар. Қоспаны шыны таяқшамен араластырыңдар. Кремний қышқылы түзілгендіктен, қоспа қоюланып, қата бастайды. Реакция теңдеуін жазыңдар.
2. Сірке қышқылының алынуы. Пробиркаға натрий ацетатының шамалы кристалын салып, оған бірнеше тамшы H 2 SO 4 қосыңдар. Иісі бойынша қандай зат түзілгенін анықтаңдар. Реакция теңдеуін жазыңдар.
3. Қышқыл мен сілтінің әрекеттесуі. Пробиркаға 10 тамшы натрий гидроксидін құйыңдар, оған көк лакмус қағазын салыңдар, оның түсін байқаңдар. Осы пробиркаға тамшылатып, тұз қышқылы ерітіндісін қосыңдар. Қоспаны үнемі араластырып тұрып, лакмус қағаз түсінің өзгергенін байқаңдар. Индикатор қағаздың түсі неліктен өзгерді? Жүрген реакция теңдеуін молекулалық және иондық түрде жазып, байқаған өзгерістерді түсіндіріңдер.
4. Қышқылдарының тұздармен әрекеттесуі. Пробиркаға 3 тамшы сұйытылған тұз қышқылын құйып, оған бір тамшы күміс нитраты ерітіндісін қосыңдар. Осындай тәжірибені сұйытылған күкірт қышқылы мен барий хлоридін қосып жүргізіңдер. Не байқадыңдар? Қандай заттар тұнбаға түседі? Реакция теңдеуін жазыңдар.
Тапсырма сұрақтары:
1. Қышқыл, тұз гидроксидтердің электролиттік диссоциация теңдеулерін жазыңдар.
2. Барлық кластардың номенклатурасын біліңдер.
2. Тұздардың қасиеттері
Жұмыстың мақсаты: тұздардың жіктелуін, қасиеттерін және олардың арасындағы генетикалық байланыстарды оқып-үйрену.
Реактивтер мен құрал жабдықтар: мырыш сульфаты, металл темір, қорғасын (ІІ) тұзы, мырыш, кесегін муфель, фарфор табақша, натрий сульфаты, тұз қышқылы, H 2 SO 4, натрий гидроксиді, күміс нитраты, сұйытылған күкірт қышқылы, темір (ІІІ) хлориді, кобальт нитраты, азот қышқылы, барий хлоридіне, алюминий сульфаты, калий нитраты, магний хлориді, магний оксидін.
1-тәжірибе. Орта тұздардың алынуы және қасиеттері.
1. Мыс (ІІ) сульфаты ерітіндісі құйылған бір пробиркаға металл темір, ал қорғасын (ІІ) тұзы бар екінші пробиркаға мырыш салыңдар. Біраз тұрғаннан соң металлдардың стандартты электродттық потенциал қатарына сүйеніп, осы реакциялардың жүру мүмкіндігін түсіндіріңдер.
2. Пробиркаға, күкірт қышқылы ерітіндісін құйып, оның үстіне мыс (ІІ) оксидін салыңдар да, шамалы қыздырыңдар. Ерітіңдінің көк түске боялуын тсіндіріңдер. Реакция теңдеуін жазыңдар.
3. Фарфор табақшаға 10 мл сұйытылған тұз қышқылын құйыңдар, оның үстіне лакмус қағазының түсі өзгермегенгн дейін натрий гидроксидін қосыңдар. Реакция теңдеуін жазыңдар.
4. Үш пробиркада темір (ІІІ) хлоридінің күміс нитратына, натрий сульфатының барий хлоридіне, алюминий сульфатының калий нитратына әсерлерін байқаңдар. Реакция теңдеуін молекулалық, иондық түрде жазыңдар.
2-тәжірибе. Негіз тұздардың алынуы және қасиеттері.
А) Мыс (ІІ) гидроксосульфатын алу.
Мыс (ІІ) сульфаты ерітіндісіне араластырып тұрып, жасыл көк түсті аморфты тұнба (CuOH) 2 SO 4 түскенше шамалы сілті ерітіндісін құйыңдар. Пробиркадағы тұнбаны шамалы қыздырыңдар, сонда тұнба когуляцияланып, түсі сақталады. Реакция теңдеуін жазыңдар.
Ә) Кобальт гидроксанитратын алу.
Пробиркаға 0, 5 - 1 мл кобальт нитратын құйыңдар, оған араластырып тұрып 5 - 8 тамшы сілті ерітіндісін қосыңдар. Көкшіл түсті тұнба түскенін байқаңдар, оны екіге бөліңдер. Бір бөлігіне сілті (артық мөлшерін), екіншісіне қышқыл (HNO 3 , H 2 SO 4 ) қосыңдар. Сілті қосқанда тұнбаның түсі қызылға айналып ерігенін, ал қышқыл қосқанда - тұнба еріп, қызыл ерітінді түзілгенін байқаңдар. Реакциялар теңдеулерін құрып, байқаған құбылысты түсіндіріңдер.
Б) Магний оксохлоридінің түзілуі және оның полимерленуі.
5 мл магний хлориді қанық ерітіндісіне араластырып тұрып, 0, 5 г магний оксидін қосыңдар. Қоспа 5 - 10 минуттан кейін қоюланып қатады. Реакция теңдеуін жазыңдар.
Тапсырма сұрақтары:
1. Тұздардың алыну жолдарын келтіріңдер.
2. Мына тұздарды атаңдар FeCl 3 , NaHS, Zn(HSO 3 ) 2 , Al 2 (SO 4 ) 3 , (BaOH) 2 CO 3 , CrOHSO 4 , Ca(H 2 PO 4 ) 2 , MgOHCl.
3. Мына тұздарды алудың барлық мүмкін тәсілдерінің реакция теңдеулерінің жазыңдар мыс (11) сульфаты, кальций карбонаты, магний хлориді.
4. Мына тұздардың алыну реакциясының теңдеуін құрыңдар: кальций дигидрофосфаты, барий гидросульфаты, алюминий дигидроксохлориді, хром (111) гидроксокарбонаты. Бұл тұздарды орта тұзға қалай айналдыруға болады? Сәйкес реакциялардың теңдеулерін жазыңдар.
№ 5 Зертаханалық сабақтың тақырыбы: Д. И. Менделеевтің периодтық жүйесі. Атом құрылысы.
Зертаханалық сабақ тапсырмасы:
Жұмыстың мақсаты: атомдар мен иондардың, металдардың және металл емес элементтердің электрондық конфигурациясын көрсететін формулаларын жазып үйрету.
Құралдар мен реактивтер: Кипп аппарыты (хлор алуға арналған), қорғасын нитраты, натрий иодидінен сульфиді ерітінділері (0, 1М), мырыш, магний және темір кесектері.
1 - тәжірибе. Атомдар мен бір атомды иондардың электрондық құрылымы.
Металдар тотыққанда олардың электрондық қабатындағы - электрон саны кемиді де, оң зарядты иондар түзіледі.
Мысалы, Mg 0 - 2e - Mg 2+ … 3S 2 3S 0
Үш пробиркаға қорғасын нитраты ерітіндісін құйыңдар (1/3 көлем) . Бірінші пробиркаға темір, екіншіге мырыш, үшіншіге магний салыңдар. Бірнеше минуттан соң ерітіндідегі металдардың бетіне назар аударыңдар.
Қорғасын нитраты ерітіндісі мен оған салынған темір, магний және мырыш арасындағы жүретін реакция теңдеуін молекулалық, иондық және қысқарған иондық түрде жазыңдар. Не байқадыңдар Мына кестені толтырыңдар.
Fe
Mg
Zn
Pb 2+
Осы атомдардың электрондық формуласын кванттық ұяшықтарда электрондардың орналасуы арқылы көрсетіңдер: а) магний; ә) темір, б) мырыш, в) қорғасын.
Периодтық жүйеден электрондық аналогтарын тауып, олардың электрондық формуласын жазыңдар.
2-тәжірибе. Металл еместердің атомдары мен иондарының электрондық құрылымы.
Металл емемтердің атомдары тотықсызданған кезде электрондық қабаттағы электрон саны артады да, теріс зарядты иондар түзіледі.
Мысалы, Bz + e → Bz -
… 4S 2 4p 5 →… 4S 2 4p 6
Бұл тәжірибені желдеткіш шкаф астында жүргізу керек. Екі пробиркаға натрий сульфиді және иодиді ерітінділерін құйыңдар (1/3 көлем) . Алдымен бірінші, содан соң екінші пробиркадағы ерітінділерге түтік арқылы Кипп аппаратынан хлор жіберіңдер. Не байқадыңдар. Жүрген реакцияның теңдеулерін молекулалық, иондық және қысқаша иондық түрде жазыңдар:
S 2
J -
Cl
1. Күкірт; 2. Хлор; 3. Иод атомдардың қысқаша электрондық формуласына электрондардың кванттық ұяшықтарда орналасу сызбанұсқасын келтіріңдер.
2. Д. И. Менделеевтің периодты жүйесінен электрондық формуласы … 4S 2 4p 5 болатын элементті табыңдар. Бұл элементтің сыртқы р электрондары қандай сандарымен сипатталады?
Тапсырма сұрақтары:
1. Хунд ережесі. Осы ережені пайдаланып, фосфор, алюминий, кремний, күкірт атомдарының электрондарын орбитальдарға орналастырыңдар.
2. Электрондық конфигурация тұрғысынан элементтер қаситтерінің периодты өзгеруін қалай түсіндіруге болады?
3. Электрондық конфигурациясы. 3 d 8 4s 2 болса, ол қай элемент? Электрондарын кванттық ұяшықтар бойынша орналастырыңдар.
4. Хром атомы мен Cr 3+ ионының электрондық конфигурациясын жазыңдар.
5. Электрондық конфигурациясына сүйеніп, ванадий мен мышьяк қасиеттерінің алшақтығын түсіндіріңдер.
6. Рет нөмірі 21, 35, 37, 73, 58 - ге тең элементтердің электрондарының орбитальдарда орналасуын Хунд ережесін пайдаланып жазыңдар.
7. Мына иондардың электрондық формулаларын жазыңдар:
а/ Ca 2+ ; Sn 2+ ; Mп 2+ ; в/ Со 2+ .
8. Реттік нөмері 21, 31, 41 және 52 элементтерде электрондар энергетикалық деңгейлерде және орбитальдарда қалай орналасқан?
9. Реттік нөмері 38, 42, 51, 74, 85-ке тең элементтер атомдарының қандай тотығу дәрежелері болуы мүмкін, соларға сәйкес қосылыстарының формуласын жазып, қасиеттерін сипатта.
10. Төмендегі молекулалардың атомдардан түзілу сызбасын электрондық теңдеулермен көрсетіңіз: AlCl 3 , H 2 S, Br 2 , BaO.
№ 6 Зертаханалық сабақтың тақырыбы: Химиялық кинетика және тепе-теңдік.
Зертаханалық сабақ тапсырмасы:
Жұмыстың мақсаты: химиялық тепе - теңдіктің орнауы мен ығысуына әр түрлі факторлардың әсерін зерттеу.
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz