Азетропты қоспалар: физикалық сәйкессіздіктері, бөлшектеп және үздіксіз айдау


Оңтүстік Қазақстан Медицина академиясы “АҚ”
« Химиялық пәндер » кафедрасы
Тақырыбы: Азеотропты қоспалар. Физикалық сәйкессіздіктері. Бөлшектеп және үздіксіз айдау.
Орындаған: Аймахан Н. Ә.
Тобы: В-ФҚБ-02-17
Қабылдаған: Джантураева А. М.
Жоспар:
І. Кіріспе
1. Шексіз еритін сұйықтар
ІІ. Негізгі бөлім
2. 1 Коновалов заңдары
2. 2 Азеотропты қосылыстар
2. 3 Азеотропты қосылыстарды бөлу.
ІІІ. Қорытынды
ІV. Пайдаланылған әдебиеттер
Шексіз еритін сұйықтар деп өзара кез-келген мөлшерде араласып, бір сұйық фаза түзетін жүйелерді айтады. Түзілген ерітіндінің құрамы сұйықтардың қайнау температураларына, ерітінді үстіндегі бу фазасының құрамы мен қаныққан бу қысымына байланысты.
Тұрақты тмпературада қаныққан бу қысымының ерітінді құрамына тәуелділігіне байланысты шексіз еритін сұйықтарды үшке бөлеміз:
- Идеал ерітінділер, яғни Рауль заңына бағынатын ерітінділер;
- Рауль заңынан оң және теріс ауытқу көрсететін ерітінділер;
- Қ. б. қ. - ерітінді құрамы қисығында максимум немесе минимумн үктелері бар жүйелер.
Идеал ерітінділерді компоненттерді өзара кез-келген көлемде араластырғанда жалпы көлемінің артуы не кемуі, жылудың бөлінуі не сіңірілуі байқалмайды. Идеал ерітінділердің компоненттері өзара әрекеттеспейді. Идеал ерітінділер молекулаларының полярлылығы, құрылысы және химиялық құрамы ұқсас заттардан түзіледі.
Идеал ерітіндідегі әр компоненттің қ. б. қ. Және ерітінді үстіндегі жалпы бу қысымы, Рауль заңы бойынша, ерітінді құрамына түзу сызықты тәуелді.
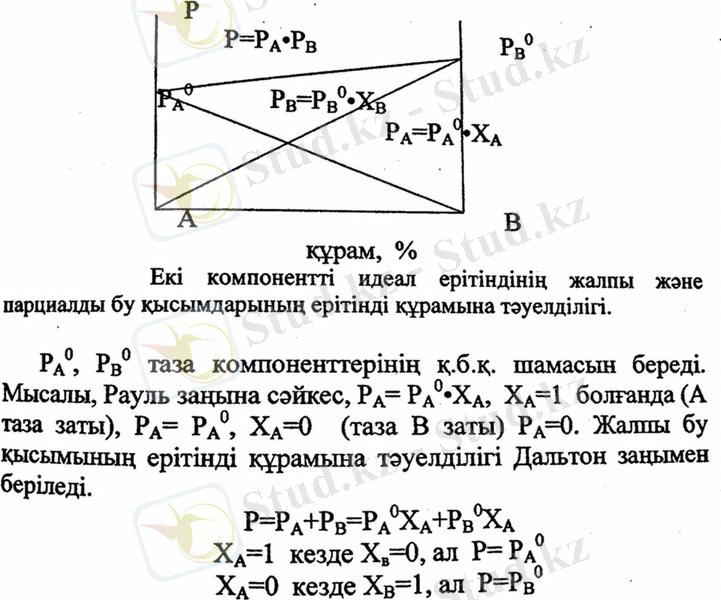
Практикалық есептерді шешу үшін қайнау диаграммалары қолданылады. Диаграмманы таза заттардың қайнау температурасын және олардың концентрацияға байланыстылығын біліп, тәжірибеде бу құрамын анықтамай сыліға болады. Берілген температурада компоненттердің сұйық және бу фазаларындағы концентрациялары әртүрлі.
Сұйық пен будың тепе-теңдік құрамдары арасындағы қатынасты зерттеп, орыс ғалымы М. И. Коновалов (1881ж. ) екі заңды ашты
1-ші заңнан берілген компоненттің буы мен тепе - теңдіктегі ерітіндідегі құрамдарының сәйкессіздігі байқалады. Бастапқы ерітіндіге қосқанда оның қайнау температурасын төмендететін немесе ерітінді үстіндегі қаныққан будың жалпы қысымын арттыратын компонент бу құрамында көбірек болады.
Оң ауытқы көрсететін ерітіндінің түзілуі жылуыдң жұтылуына байланысты, себебі булану үдерісі жеңілденеді. Сондықтан жүйе үстіндегі бу қысымы Рауль заңы бойынша есептегенде жоғары болады. Оң ауытқу көптеген біртекті жүйелерге тән ( ацетон-бензол, ацетон-су, бензол-төртхлорлы көміртек т. б. ) . Рауль заңынан теріс ауытқу сирек кездеседі ( мысалы, эфир - хлороформ) .
Теріс ауытқуы бар ерітіндінің түзілуі жылудың бөлінуі арқылы жүреді, сондықтан булану үдерісі қиындайды және қаныққан бу қысымы Рауль заңымен есептегеннен төмен болады. Кейбір жүйелерде Рауль заңынан өте көп ауытқығандықтан бу қысымы - құрым тәуелділігінің қисықтарында ұшқыш таза заттардың бу қысымдарына қарағанда бу қысым жоғары немесе аз ұшатын компоненттің бу қысымына қарағанда төмен нүктелер түзіледі. Нәтижеде жалпы бу қысымы қисығында максимум не минимум пайда болады.
Бу қысымы қисығында максимумға қайнау t◦С қисығындағы минимум сәйкес келеді және бұл нүктеде ерітінді мен оның бу құрамы өзара тең.
Диаграммадағы максимум, минимум нүктелеріне сәйкес қоспалар
азетропты
не
үнемі қайнайтын ерітінділер
деп аталады. Олар қайнау температурасы ең төменін Рауль заңынан оң ауытқуда, ең жоғарысын - теріс ауытқуда көрсетеді. Азетропты ерітінді тұрақты температурада құрамы өзгермей қайнайды.
Бірақ сыртқы қысым өзгергенде оның қайнау температурасы да, құрамы да өзгереді. Демек, азетропты қоспа химиялық қосылыс емес. Көбінесес ең төмен қайнау температурасы бар азетропты қоспалар жиі кездеседі. Оларға су - этил спирті, метил спирті - ацетон, бензол - сірке қышқылы жатады. Қайнау температурасының максимумы бар азетроптар сирек кездеседі. Оларға қышқылдардың сулы ерітінділері (тұз, күкірт, құмырсқа қышқылы) хлороформ - ауетон қышқылы жатады.
Азетропты қоспаларды бөлу:
а) Азетропты қоспаның бір компонентін химиялық байланыстыру. Мысалы, абсолютті этил спиртін алу. Спирт ерітінділерін ректификациялағанда колонканың куб бөлігінде 98% спирт және 4% судан тұратын қоспа қалады. Абсолют спирт алу үшін азетропты қоспаны су тартқыш затпен өңдейді ( металды Na немесе CaCl2) .
б) Азетропты қоспаны үшінші зат қосып алу.
Абсолют спиртті азетропты қоспаны бензол қосып, қайнатып алады. Түзілген екі фазалы жүйе басқа температурада қайнайды. Бензол қабатын айдаған соң абсолют спирт қалады.
в) екі бағанада әртүрлі қысымда кезектесіп ректификациялау.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz