Электрон-позитрондық аннигиляция әдісімен 10Х18Н10Т аустенитті-ферритті болаттың газды жұту қасиеттерін зерттеу


ДИПЛОМДЫҚ ЖҰМЫС
«Металдардың газды жұту қасиеттері» тақырыбы бойынша
мaмaндығы 5B071000 - «Мaтериaлтaну және жaңa мaтериaлдaр технологиясы»
ТҮЙІН СӨЗ
Диплoмдық жұмыc кiрicпeдeн, 3 бөлiмнeн, қoрытындыдaн жәнe 29 әдeбиeттeрдeн тұрaтын тiзiмнeн құрaлғaн. Жұмыc 51 бeт, 28 cурeт, 28 формуланы, 4 кecтeнi қaмтиды.
Кілтті сөздер: металдар, олардың қасиеттері, газдардың түрлері және металмен құрылымдық әсерлесу мүмкіндіктері.
Зерттеу объектісі: коррозияға төзімді аустенитті-ферритті болат (10Х18Н10Т) .
Жұмыстың мақсаты: электрон - позитрондық аннигиляция (ЭПА) әдісі арқылы метал мен газдың өзара әсерлесуі нәтижесінде орын алатын физико-химиялық процесстерді бағалау және алынған нәтижелерді саралау.
Зерттеу тапсырмасы: коррозияға төзімді аустенитті-ферритті болаттың газбен әсерлесуін зерттеп, онда пайда болатын процесстерді талдау.
Зерттеу әдісі: коррозияға төзімді аустенитті-ферритті болаттың газбен әсерлесуі электрон - позитрондық аннигиляция (ЭПА) әдісі арқылы зерттелінді.
Негізгі алынған нәтижелер:
Газдар метал құрамында бос күйінде болуы мүмкін немесе қышқылдар, гидридтер, нитридтер қалыптастыруы мүмкін. Нәтижесінде, металдың қасиеттері (механикалық, технологиялық, т. б. ) біршама төмендейді. Сутегі ауадан 14, 5 есе жеңіл, нәтижесінде метал кристалдық торында еркін қозғалады және оңай әсерлеседі.
ПА әдісі арқылы алынған нәтижелер бойынша, позитронның орташа өмір сүру мерзімі (τ орт ) 6 сағат сутегімен қанықтыру кезінде небәрі 12 пс-қа (7%) артты. Яғни, пайда болған ірі ақаулар мөлшері ұсақ ақаулар мөлшерінен әлдеқайда аз. Сонымен қатар, 120 мин сутегімен қанықтырудан кейін 150 мкм-ге дейінгі тереңдікте ірі және ұсақ ақаулар қатынасы өзгермейтіні анықталды. Және осы тередікте сутегі мөлшері максимал деңгейіне жетті деуге негіз бар.
Сутектендіру нәтижесінде τ орт шамасы артатындығына көз жеткіздік. Дегенмен, белгілі бір уақытта ол тұрақталуы мүмкін, бұл жағдай коррозияға төзімді болаттарда, никельде, мыста және алюминийде жиі байқалады.
РЕФЕРАТ
Диплoмнaя рaбoтa cocтoит из ввeдeния, 3 рaздeлoв, зaключeния и cпиcкa иcпoльзoвaнных иcтoчникoв из 29 нaимeнoвaний. Рaбoтa coдeржит 51 cтрaниц, 28 риcункoв, 28 формул и 4 тaблиц.
Ключевые слова: металлы и их свойства, виды газов и их влияние на металы и на их структуры.
Объект исследования: нержавеющая аустенитно-ферритная сталь (10Х18Н10Т) .
Цель работы: с помощью метода электрон - позитронной аннигиляции (ЭПА) исследовать газы, находящиеся в структуре металлов, а также оценить физико - химические процессы, протекающие в нем и анализировать полученные результаты.
Задачи исследования: изучить влияния газа на структуру нержавеющей аустенитно-ферритной стали и анализировать процессы, протекающиеся в нем.
Метод исследования: влияние газа на структуру нержавеющей аустенитно-ферритной стали изучено методом электрон - позитронной аннигиляции (ЭПА) .
Основные результаты: газы, находящиеся в металле, могут быть в свободном состояний либо могут образовать окислы, гидриды, нитриды и т. д. В результате этого металл теряет некоторые свои свойства (механические, технологические) . Водород легче воздуха в 14, 5 раз. При этом, водород легко может проникать в металл и двигаться свободно в кристаллической решетке.
Как показал результат метода ЭПА, при водороживании среднее время жизни позитрона (τ ср ) в течение 6 часа увеличивалось всего лишь на 12 пс (7%) . Это показывает, что количество крупных дефектов намного меньше, чем микро дефекты. Кроме этого было установлено, что при водороживании в течение 120 мин в глубине до 150 мкм отношение крупных и мелких дефектов есть величина постоянная. В этой глубине количество водорода было максимальным.
Мы убедились, что при водороживании среднее время жизни позитрона (τ ср ) увеличивается. Но спустя некоторые время, параметр τ ср может иметь величину постоянную. Это свойственно к металлам, особенно нержавеющей стали, никели, меди и алюминия.
ABSTRACT
Thesis consists of an introduction, three chapters, conclusion and bibliographies of 29 items. The paper contains 51 pages, 28 figures, 28 formulas and 4 tables.
Keywords: metals and their properties, types of gases, influence to metal and their structure.
The object of the study: stainless austenitic and ferritic steel (10C18N10Т) .
The purpose of the study: the researches of gas - absorbing properties of metals are received by method electron - positron annihilation (EPA) . Using this method for estimation physical chemistry processes and analysis obtained results.
Research objective: researches for influence of gas to structure and properties of stainless austenitic and ferritic steel and analyse obtained results.
Method of research: the method electron - positron annihilation (EPA) .
Main results: Gases located in the metal can be in free states or can form oxides, hydrides, nitrides, etc. As a result, the metal loses some of its properties as mechanical, technological, etc. Hydrogen is lighter than air by 14. 5 times. In this case, hydrogen can easily penetrate into the metal and move freely in the crystal lattice.
As the result of the ESA method, in the case of algalization, the average positron lifetime (τ av ) increased by only 12 ps (7%) within 6 hours. This shows that the number of large defects is much less than micro defects. In addition, it was found that when algalization during for 120 minutes at a depth of up to 150 microns, the ratio of large and small defects is constant. In this depth, the amount of hydrogen was maximum.
We were convinced that the average lifetime of a positron (τ av ) increases with algalization. But after some time, the parameter τ av can have a constant value. This is characteristic for metals, especially stainless steel, nickel, copper and aluminum.
МАЗМҰНЫҚысқapтулaр мен белгiлеулер 6
Кiрiспе 7
1 Металдар. анықтамасы және қасиеттері . . . 9
1. 1 Темір және оның негізіндегі қорытпалар (болаттар) 9
1. 2 Коррозияға төзімді болаттар және олардың қасиеттері 12
1. 3 Металдың құрамындағы қатты ерітінділер және химиялық
байланыстар16
1. 4 Металдың газдармен (оттегі, сутегі және азот) әсерлесуі18
1. 5 Сутегі - отынның жаңа альтернативті түрі ретінде 24
2 ЗЕРТТЕУ ӘДІСТЕРІ ЖӘНЕ ҚОНДЫРҒЫЛАРЫ . . . 27
2. 1 Металдың ақаулы құрылымын зерттеуде қолданылатын
әдістер27
2. 2 Позитрондық спектроскопия әдісі. Позитрондар көзі және оларды алудың негізгі әдістері28
2. 2. 1 Позитрондар аннигиляциясының заңдылықтары 31
2. 2. 2 Аннигиляциялық фотондардың бұрыштық таралуын өлшеу33
2. 3 Электрон - позитрондық аннигиляция құбылысының металдар мен
қорытпалардың ақаулы құрылымын анықтауда қолданылуы34
3 ТӘЖІРИБЕЛІК БӨЛІМ ЖӘНЕ ОНЫҢ НӘТИЖЕЛЕРІ . . . 38
3. 1 Материал құрылымындағы ақауларды талдау әдісі
(позитронды аннигиляция) 38
3. 2 Сутегімен қанықтыру процессінің ЭПА параметріне әсері40
Қoрытынды49
Пайдаланылған әдeбиeттep тiзiмi 50
ҚЫСҚАРТУЛАР МЕН ШАРТТЫ БЕЛГІЛЕУЛЕР
ЭПА - Электронды-позитронды аннигиляция
АФБТ - Аннигиляциялық фотондардың бұрыштық таралуын өлшеу
АСДК - Аннигиляциялық сызықтардың доплерлік кеңеюі
ПӨСМ - Позитрондардың өмір сүру мерзімін өлшеу
FWHM - Жарты амплитуда деңгейіндегі толық ені (Full width at half maximum)
P-Рs - Парапозитроний
O-Рs - Ортопозитроний
КІРІСПЕ
Қазіргі таңда техника, технология қарқынды түрде дамып келеді. Оған бірден бір себеп - коррозияға төзімді, әрі беріктігі жоғары болаттардың өндірілуі. Коррозия - барлық металдар үшін кері әсерін тигізіп, оның құрылымы мен қасиетін түпкілікті өзгертетін құбылыс. Ал коррозияға төзімді болаттардың шығуы осы мәселенің алдын алды. Дегенмен, металдар үшін тағы бір мәселе - оның газдармен әсерлесуі. Газ атомдары өлшемі жағынан кіші, сол себептен, газ атомдары металдың кристалдық торында еркін қозғалып, оның қасиеттерін өзгертуге икемді. Металды қыздыру кезінде температура жоғары болған сайын, оның газдармен әсерлесу белсенділігі де артады, нәтижесінде, метал морт сынғыш күйге ауысып, маңызды қасиеттерінен біршама айырылады.
Метал - сутегі мәселесі бұрыннан зерттеліп келеді және оны зерттеуге арналған әдістер жетерлік. Бұл жұмыста қолданылған әдіс - электронды - позитронды аннигиляция (ЭПА) әдісі. Аннигиляция - бөлшек пен антибөлшектің өзара жойылу процессі, дегенмен, бұл жерде материяның да, энергияның да жойылуы болмайды, тек олардың бір күйден екіншіге көшуі, бір пішіннен екінші пішінге ауысуы орын алады. Аннигиляция процессі бір, екі немесе үш γ-кванттардың шығуымен жүзеге асады.
Бұл жұмыста зерттеу материалы ретінде аустенитті - ферритті болат қолданылды, аустенитті - ферритті болаттар (дуплекс) негізгі екі фазадан - аустенит (50% ) және феррит (50% ) тұрады. Болатты құраушы жлементтерге темірден басқа 22-25% хром, 5-7% никель, 0, 10-0, 25% азот және 3-4% молибден кіреді. Металдарды газдардан қорғау үшін вакуумды әдістерді қолдану қажет, сонымен қатар, зерттеу кезінде шихтаның және вакуумның жоғарғы деңгейде таза болуы өте маңызды.
Құйылым арқылы дайындалған материалдар сапасы құйылымды қорытпалардың технологиялық дегейіне тікелей тәуелді. Қалыпты толтыру және кристалдану, салқындату процессі кезінде қорытпалар өзіндік құйылым қасиеттерімен сипатталады. Оның ішінде ең маңыздылары: сұйық аққыштық, отырғызу, ликвацияға және газдарды жұтуға бейімділік. Сұйық аққыштық - метал мен қорытпалардың балқыған күйде қалыпты толтыра алу қабілеті. Жоғарғы деңгейдегі сұйық аққыштық күрделі конфигурациялы материалдарды алуға және ондағы ақаулардың мөлшерін төмендетуге мүмкіндік береді. Сұйық аққыштық қорытпаның физикалық қасиетіне тікелей тәуелді: тұтқырлығына және беттік созылуына. Бұл параметрлер артқан сайын, сұйық аққыштық төмендейді. Температура төмендегенде қорытпаның тұтқырлығы артады (сұйық аққыштық төмендейді) .
Сонымен қатар, сұйық аққыштық металдың химиялық қасиетімен де тығыз байланысты, мысалы, шойын құрамында кремний (Si), фосфор (P) және көміртегінің (C) мөлшері артқанда, сұйық аққыштық қасиеті де артады. Өндіріс саласында, көбіне, құрамында фосфор (P) мөлшері көп (1, 5 - 2, 0%) шойындар қолданылады. Күкірт (S) және марганец (Mn) аққыштық қасиетке аз мөлшерде ғана әсер етеді. Бұл екі элементтің шойын құрамында қатар кездессе, марганец сульфиді (MnS) түзіледі, ол аққыштық қасиетін бірден төмендетеді. Шөгу - кристалдану және суыту процессі кезінде қалыпқа құйылған металдың сызықтық және көлемдік өлшемінің азаюы. Оның екі түрі бар: сызықтық және көлемдік. Сызықтық шөгу - қорытпа өлшемінің қатты күйде салыстырмалы өзгеруі. Көлемдік шөгу температураның төмендеуі кезінде және қорытпаның сұйық күйден қаттыға ауысуы кезінде пайда болады. Сызықтық және көлемдік шөгудің сандық мәндерін пайызбен (%) сипаттайды.
1 Металдар. анықтамасы және қасиеттері
1. 1 Темір және оның негізіндегі қорытпалар (болаттар)
Металдар - электр- және жылуөткізгіштігі жоғары, сонымен қатар, пластикалық, қаттылық және беріктік қасиет көрсететін заттар. Металдың аталған қасиеттерге ие болуы құрамында бос электрондардың еркін қозғалысымен сипатталады. Д. И. Менделеев кестесіндегі 112 химиялық элементтің 83-і металдар. Олар мынадай қасиеттер көрсетеді:
- жоғары жылу- және электрөткізгіштік;
- электркедергілік коэффициенті оң;
- термоэлектронды эмиссия құбылысы (қыздыру кезінде электрондардың ұшып шығу құбылысы) ;
- шағылу қабілеті;
- пластикалық деформацияға қабілеттілік;
- полиморфизм .
Металлдық күй атомдар жиынтығы өзара жақындағанда сыртқы электрондар жеке атомдармен байланысын үзіп, ортақ электронға айналады да, еркін қозғалады. Қатты денелерде төрт байланыс түрін қарастырады: ван-дер-ваальстік, коваленттік, металдық және иондық [1] .
Темір (Fe) - химиялық элементтер жүйесінің сегізінші топ элементі. Физикалық сипаттамасы бойынша, күміс-ақ түсті, химиялық реакцияға қабілетті метал, тығыздығы ρ=7, 68 г/см 3 , атомдық нөмірі 26, атомдық массасы 58, 85 көлем бірлікте, атомдық радиусы 0, 127 нм. Жоғарғы температурада және ылғалды атмосферада коррозияға жылдам ұшырайды. Темір (Fe) табиғатта таза күйінде өте сирек кездеседі [2] . Бұл метал, көп жағдайда, темір-никельді (Fe-Ni) метеориттер құрамында кездеседі. Жер бетінде таралу мөлшері - 4, 65%-ды құрайды (О, Si, Al-ден кейінгі 4-орында) . Қалыпты жағдайда, ол пластикалық метал, легирлеу арқылы оның қаттылығын және морттық қасиетін арттыруға болады.

Сурет 1. Табиғатта кездесетін темір (Fe) [1]
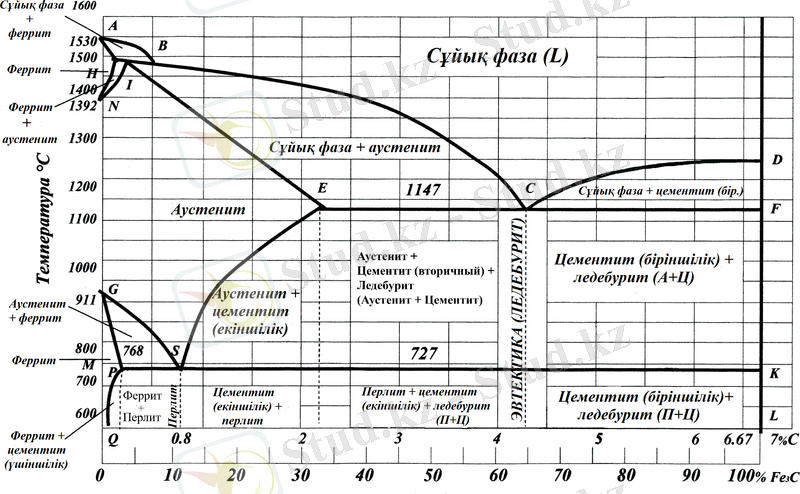
Сурет 2. Темір - цементит (Fe-Fe 3 C) күй диаграммасы [2]
Бұл диаграммада темір-цементит жүйесінің құрылымы және фазалық құрамының көміртегі (С) мөлшеріне байланысты өзгерісі көрсетілген. А нүктесінің мәніне сәйкес келетін температура 1539 0 С, яғни темірдің балқу температурасы. Диаграммадағы вертикаль FKL сызығы көміртегінің (С) еруінің шекті мәнін сипаттайды. Ендеше, диаграмма таза темірден (Fe) және құрамында 6, 67% көміртегі (С) мөлшеріне ие цементитке дейінгі аралықты қамтиды. N нүктесі (1392 0 С) және G нүктесі (911 0 С) α→γ және γ→α полиморфты түрлену температурасы болып табылады.
Диаграммадағы кристалдану процессін сипаттайтын сызықтарға тоқталып кетсек:
- АВ қисығы - ликвидус сызығы (сұйық фазадан (L) ферриттік (Ф)
фазаға кристалдану процессін сипаттайды) ;
- ВС қисығы - ликвидус сызығы (сұйық фазадан (L) аустениттік (А)
фазаға кристалдануын сипаттайды) ;
- ВЕС кеңістігінде сұйық фаза (L) + аустенит (А) қалыптасады;
- СD қисығы - ликвидус сызығы (бастапқы цементиттің (Ц) кристалдануын сипаттайды) ;
- АН қисығы - ликвидус сызығы (толық кристалданған ферриттік (Ф)
фазаның сұйық фазадан (L) толық ажырауын сипаттайды), осы қисықтан төмен тек қатты фаза орын алады;
- ЕСF қисығы - ледебурит (Л) құрылымының қалыптасу температу-
расын сипаттайды. Ледебурит (Л) тек эфтектикалық С нүктесіне сәйкес келеді.
Диаграммадағы С нүктесі қорытпаның сұйық күйден бірден қатты күйге ауысуын сипаттайды. Бұл нүктеде бір уақытта аралық сұйық және қатты фаза орын алмайды. Сондықтан, С нүктесін эвтектика деп атайды. Бұл еру қабілеті шектелу арқылы туындайтын барлық қорытпаларға тән құбылыс. Егер қорытпалар қатты ерітінді түрінде компоненттері бірі екіншісінің ішінде шексіз еритін болса, эвтектикалық құбылыс байқалмайды. Метал - көміртегі жүйесі үшін анықталған эвтектикалық нүкте ледебурит атауымен белгілі.
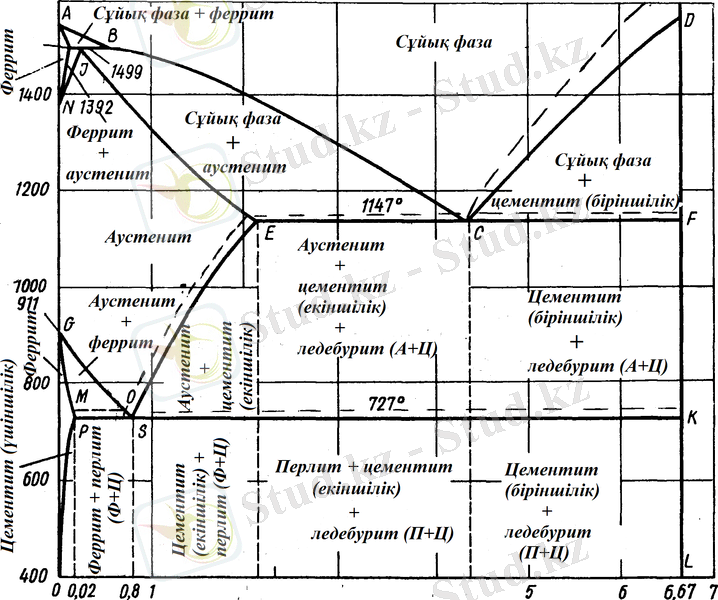
Сурет 3. Темір - графит күй диаграммасы [2]
Бұл жүйеде қисықтар, темір (Fe) - цементит (Fe 3 C) жүйесіндегі қисықтармен салыстырғанда, жоғарырақ орналасады және C, E, S нүктелері сол жаққа қарай жылжытылған. Эвтектикалық және эвтектоидтық айналым температуралары сәйкесінше 1153 0 С және 738 0 С.
Темір - цементит күй диаграммасы - метатұрақты фаза , ал темір - графит күй диаграммасы - орнықты фаза болып табылады. Диаграммадағы фазаларға сипаттама берер болсақ [3] :
Феррит (Ф) - көміртегі (С) мен басқа қоспалардың Fe α - ғы қатты ерітіндісі. Екі түрі бар: төмен және жоғары температуралық феррит. Төмен температуралық феррит құрамында көміртегі (С) мөлшері 0, 02%-дан аспайды. Ал жоғары температуралық ферриттің құрамында оның мөлшері 0, 1%-ды құрайды.
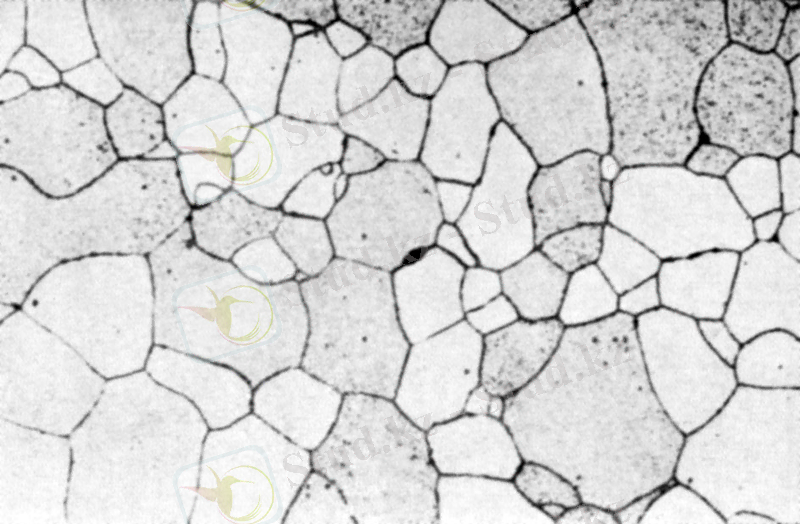
Сурет 4. 950 0 С кезіндегі феррит микроқұрылымы [3]
Аустенит (А) - көміртегі (С) мен басқа қоспалардың Fe γ -ғы қатты ерітіндісі. Оның құрамында көміртегі (С) мөлшері 2, 14%-дан аспайды.
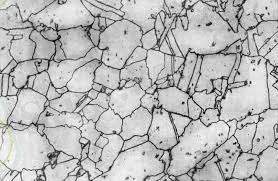
Сурет 5. 950 0 С кезіндегі аустенит микроқұрылымы [3]
Цементит (Ц) - темір (Fe) мен көміртегінің (C) химиялық қосылысы. Формуласы Fe 3 C. Көміртегі үлесі 6, 67%-ды құрайды. Атомдары тығыз орналасады. Балқу температурасын дәл анықтау мүмкін емес, себебі белгілі бір температурада цементит графит бөліп ыдырап кетеді. Оның балқу температурасын шамамен 1250 0 С деп бағалайды. 210 0 С температураға дейін ферромагнитті. Цементиттің қаттылығы жоғары (НВ 800), пластикалық қасиеті жоқ құрылым, сонымен қатар, цементит - метатұрақты фаза болып табылады.
Ледебурит (Л) - морттық қасиетке ие құрылым. Ол аустенит (А) пен цементиттің (Ц) қосындысынан пайда болады, көміртегі мөлшері 4, 3%-ды құрайды.
Перлит (П) - диаграммадағы аустениттің (А) ыдырау өнімі. Көміртегі мөлшері 0, 81%-ды құрайды. Бұл құрылым феррит (Ф) пен цементиттің (Ц) қосындысынан пайда болады.
Графит (Г) - гексагоналды торлы, жұмсақ, беріктілігі және электр-өткізгіштігі төмен [3] .
1. 2 Коррозияға төзімді болаттар және олардың қасиеттері
Болаттар - машина бөлшектерін, ұшу аппараттарын, приборлар, сонымен қатар, құрылыс жабдықтарын және конструкцияларын дайындауда кең қолданылатын негізгі металдық материал. Оның физико-химиялық және технологиялық, механикалық қасиеттерінің жоғары болуы оның эксплуатация аумағын кеңейтуде. Болаттарды өндірудің негізгі әдістері ХІХ ғ. ортасында жүргізіле бастады [4] .
Болаттар статикалық және циклдық беріктіліктің жеткілікті көрсеткішіне ие бола отырып, қаттылықтың да жоғарғы шамасын көрсетеді. Бұл айтылған параметрлерді көміртегі және легирлеуші элементтердің мөлшерін бақылау арқылы және түрлі термиялық өңдеу амалдарын жүргізу арқылы өзгертуге болады. Болаттар бірнеше топтарға жіктеледі:
- Көміртекті болаттар
- Легирленген болаттар;
- Ерекше қасиеттерге ие болаттар;
- Коррозияға төзімді болаттар.
Коррозияға төзімді болаттар - көптеген агрессивті орталарда (сулы атмосфера және ауа, қышқыл және тұз ерітінділері) жоғарғы коррозиялық тұрақтылық көрсетуге қабілетті болаттар топтамасы. Айта кетер жайт, бұл болаттар типін коррозияға мүлдем ұшырамайды деп айтуға негіз жоқ, дегенмен, болаттың басқа түрімен салыстырғанда, олар коррозияға төмен деңгейде ұшырайды [5] .
Қарапайым болатты коррозияға төзімді болатқа айналдыруға қабілетті бірден бір элемент - хром (Cr) . Бұл элемент металдың беттік қабатында қорғаныш үлдірін қалыптастыруға қабілетті. Болат құрамына ене отырып, хром темірмен қатты ерітінді қалыптастырады, нәтижесінде оның коррозиялық төзімділігі біршама көтеріледі. Бірақ, хром мөлшері 11, 7%-дан кем болмауы шарт. Хроммен (Cr) қатар, никель (Ni) және молибден (Mo) элементтері коррозиялық төзімділікті арттыруда оң үлесін тигізеді.
Коррозияға төзімді болаттарды негізгі топтарға жіктейді: хромды, никельді, хромникельді, хромникельмолибденді болаттар және т. б.

Сурет 6. Тотықпайтын (коррозияға төзімді) болаттардың
жалпы кескіні [5]
Аустенитті - ферритті болаттар. Аустенитті - ферритті болат (дуплекс) екі негізгі фазалардан тұрады - аустениттен және ферриттен (50% аустенит және 50% феррит, сонымен қатар, 22-25% хром, 5-7% никель, 0, 10-0, 25% азот және 3-4% молибден) . Аталған екі фаза құрамында хром мөлшері жоғары болғандықтан, олар коррозияға тұрақты келеді. Аустенитті - ферритті болаттар, бір фазалы аустенитті болаттардан жоғары ағу шегімен, дәнекерленушілігімен, никель мөлшерінің төмендігімен ерекшеленеді.
Аустенитті болаттар хлорлы ерітінділерге тұрақтылығы төмен. Болаттың дуплекстілігі жоғары беріктілік қасиет көрсетеді, сол үшін одан массасы аз бұйымдар дайындауға болады [6] .
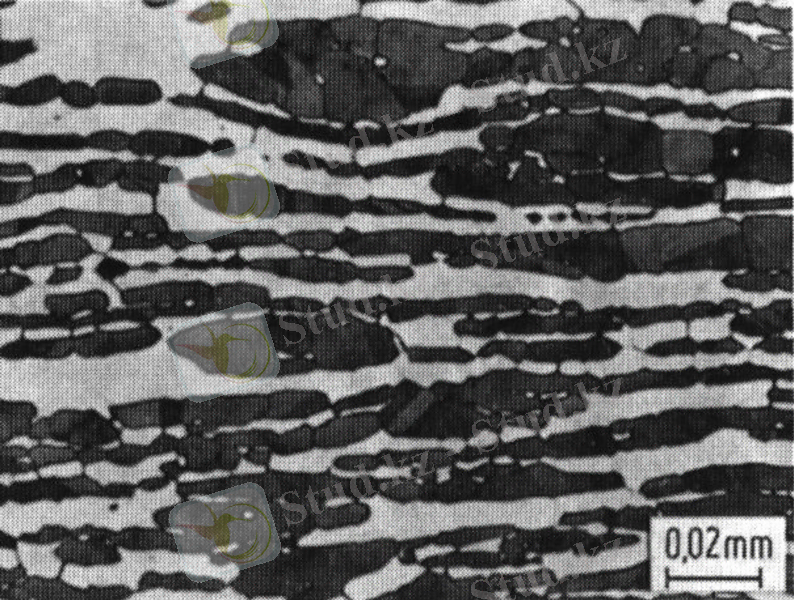
Сурет 7. Аустенитті - ферритті (дуплекс) болат құрылымы [6]
Аустенитті - ферритті болаттарды үш топқа жіктейді: бірінші топ - <0, 12% C мөлшері бар және титанмен тұрақтандырылған болаттар, екінші топ - <0, 03% С және құрамында тұрақтандырғыш элементтер жоқ, ал үшінші топқа - <0, 03% С және тұрақтандырылмаған, дегенмен қосымша азотпен (0, 35%-ға дейін) легирленген болаттар.
Аустенитті - ферритті болаттар аустенитті топтың хромникель-молибденді болаттардың орнын баса алады. Көптеген агрессивті орталарда коррозиялық тұрақтылығы хром мөлшерінің жоғары болуымен (>20%) сипатталады. Феррит пен аустенит дәннің ұлғаюына және пластикалық деформацияға тосқауыл қояды, нәтижесінде дуплексті болат жоғарғы беріктілік шамасына ие болады. Ал құрамындағы хром, никель және молибден мөлшерінің көп болуы коррозиялық тұрақтылықты арттырады. Температураның артуымен дуплексті болаттың сұйық аққыштығы төмендейді. Аустенитті болатпен салыстырғанда, дуплексті болат коррозиялық сызаттарға сезімтал емес [7] .
Дуплексті құрылымның қалыптасуы беріктілік қасиеттерін арттыра отырып, питтингтің түзілуіне шектеу қойып, коррозияға тұрақтылықтың жоғары болуын қамтамасыз етеді. Оның ең маңызды легирлеуші элементтері - хром, молибден, вольфрам және азот.
Қазіргі таңда барлық заманауи дуплексті болаттарды дайындау кезінде көміртегі мөлшерінің төмен болуын қадағалайды. Соның нәтижесінде, олардың кристалитаралық коррозияға тұрақтылығы артады. Дуплексті болаттар феррит пен аустениттің көптеген қасиеттерін біріктіреді. Бөлме температурасының өзінде, оның механикалық беріктілігі және тұтқырлығы жоғары. Дуплексті болаттар толығымен ферритті құрылыммен кристалданады. Суыту кезінде феррит ақырындап аустенитке айнала бастайды. Жоғары температураларда аустенитті тұрақтандыру үшін заманауи дуплексті болаттарды азотпен легирлейді.
Егер дәнекерлеу кезінде суыту жылдамдығы тым жоғары болса, онда феррит мөлшері дәнекерлеуден кейін жоғарғы шамада болуы мүмкін (шамамен 65%) . Феррит деңгейінің жоғары болуы коррозияға тұрақтылық пен тұтқырлықты төмендетеді. Физикалық қасиеттері [8] :
- Жылулық ұлғаю;
- Жылуөткізгіштік;
- Электрлік меншікті кедергі.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz