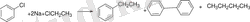Органикалық химия ІІ: оқу-әдістемелік кешен (мамандық 5В072100 - Органикалық заттардың химиялық технологиясы)


ҚАЗАҚСТАН РЕСПУБЛИКАСЫ ҒЫЛЫМ ЖӘНЕ БІЛІМ МИНИСТРЛІГІ
СемЕЙ қаласыныңШӘКӘРІМ атындағыМЕМЛЕКЕТТІК УНИВЕРСИТЕТІ
ПОӘК
Оқу-әдістемелік материалдар «Органикалық химия ІІ»
Баспа № 1
күні 11. 09 2014ж.
ПӘННІҢ ОҚУ-ӘДІСТЕМЕЛІК КЕШЕНІ
«ОРГАНИКАЛЫҚ ХИМИЯ ІІ»
мамандық үшін 5В072100 - «Органикалық заттардың химиялық технологиясы»
ОҚУ-ӘДІСТЕМЕЛІК МАТЕРИАЛДАРЫ
Семей
2014
Мазмұны
1 ГЛОССАРИЙ
- Алмасу реакциялары - айырылып, бір байланыс түзіп және сол жерге ескі атом тобының орнын жаңасы келіп басу реакциясы.
- Қосылу реакциялары - екі атом тобы немесе атом қос байланыстың үзілген жеріне қосылу реакциясы
- Бөліп алу реакциялары (элиминдеу) -екі σ - байланысын бір π - байланысымен ауыстыру
- Ациклді қосылыстар - ашық көмірсутегі тізбегі күйіндегі заттар.
- Карбоциклді қосылыстар - көмірсутегі атомдарының сақиналы тізбек күйіндегі қосылыстар.
- Көмірсутек қаңқасы - көміртегі атомдарының тізбегі
- Қаныққан көмірсулар - сутегіге бай, сутегі және галоген атомдарын қосып ала алмайды.
- Қанықпаған көмірсутектер - қосып алуға бейім.
- Изомер-молекулалық массасы және құрамы бірдей, бірақ физикалық және химиялық қасиеттері әртүрлі заттар
- Гидрлеу - сутегінің қосылуы
- Дегидрлеу - сутегігің бөлінуі
- Галогендеу -галогенді қосу
- Дегалогендеу - галогенді бөліп алу
- Гидрогалогендеу -галогенсутегін қосу
- Дегидрогалогендеу-галогенсутегін бөліп алу
- Гидратация -суды қосу
- Дегидратация- суды бөліп алу
- Карбоксилдеу-СО2қосу
- Декарбоксилдеу-СО2бөліп алу
- Полимеризация- қос байланыс үзілгенде бір молекулаға екішнші бір молекуланың келіп қосылуы.
2 ДӘРІСТЕР
Микромодуль 1 - Циклді қосылыстар химиясына кіріспе
Дәріс 1, 2 - Кіріспе
Дәріс жоспары:
1. Ароматты көмірсутектердің классификациясы
2. Изомерия. Гомология
Органикалық қосылыстардың негізі етіп көмірсутекті алады да, қалған қосылыстарды, олардың туындылары ретінде қарайды. Көміртек тізбегінің құрылысына қарай органикалық қосылыстар ашық тізбекті (алифаттық) және циклді (тұйық) қосылыстарға бөлінеді.
Тұйық тізбекті қосылыстар екіге бөлінеді : .
Карбоциклді қосылыстардың тұйық тізбегі тек көміртегі атомынан тұрады және сонымен бірге алициклді және ароматты болып екіге бөлінеді.
Гетероциклді қосылыстардың тұйық тізбегі көміртегі мен сутегі атомдарымен қоса басқа да атомдардан құралады. Гетероциклді қосылыстар түзуге көбінесе азот, күкірт, оттегі атомдары қатысады.
Органикалық қосылыстар құрамы мен құрылысына байланысты кластарғабөлінеді.
Ароматты қатардың ең қарапайым өкілдері - көмірсутектер.
Егер көмірсутектердегі сутегі атомдарын басқа атомдарға не атомдар топтарына - функциональды топтарға - ауыстырса, сол қатардың басқа кластары пайда болады.
Органикалық қосылыстар кластарының химиялық өзгерістері бағытын орын басқан атомдар мен функцинальды топтар анықтайды.
Орын басқан атомдары не функциональды топтары бірдей көмірсутектер және олардың туындылары гомологтыққатар түзеді. Сонымен, гомологтық қатарға құрылысы ұқсас, сондықтан химиялық қасиеттері де ұқсас, бір-бірінен СН 2 (метилен тобы - гомологтық айырмашылық) тобына айырымы бар заттар қатары жатады.
Органикалық қосылыстардың негізгі кластары:
1. Ароматты көмірсутектер (Ar - H) ;
2. Ароматты галогентуындылар (Ar - Hal) ;
3. Фенолдар және ароматты спирттер (Ar - OH) ;
4. Ароматты карбонильді қосылыстар - альдегидтер мен кетондар (Ar - CHO; Ar - CO - R) ;
5. Ароматты карбон қышқылдары (Ar - COOH) ;
6. Ароматты аминдер (Ar - NH 2 )
7. Ароматты нитроқосылыстар (Ar - NO 2 ) ;
8. Ароматты сульфоқосылыстар (Ar - SO 3 H) ;
Ароматты көмірсутектерге бір немесе бірнеше бензол сақинасы бар қосылыстар жатады. Бензол сақинасының саңына байланысты бірядролы (моноциклді) және көпядролы (полициклдер) деп бөлінеді.
Дәріс материалдарын игергеннен кейін білуге қажетті негізгі түсініктер: ароматты қосылыстардың құрылысы, классификациясы, гомология
Өзін өзі бақылауға арналған сұрақтар:
- Ароматты қосылыстар функционалды топтарға байланысты қалай классификацияланады?
- Гомологтық қатар дегеніміз не?
- Бірядролы ароматты қосылстарға мысал келтіріңіз?
Ұсынылған әдебиеттер:
1. Бруис, П. Ю. Органикалық химия негіздері. 1-бөлім: оқулық /П. Ю. Бруис; [қазақ тіліне ауд. Бажықова К. Б. ] - Алматы: Полиграфкомбинат, 2013. 290-300 б.
2. В. Л. Белобородов, С. Э. Зурабян, А. П. Лузин, Н. А. Тюкавкина. Органическая химия. - М. : Дрофа, 2008. -Кн. 1, С. 10-12
3. В. Ф. Травень. Органическая химия. - М. : Академкнига, 2008. Т. 1., С. 33-37
Дәріс 3, 4-Алициклді қосылыстар
Дәріс жоспары:
- Номенклатура. Изомерия
- Алу әдістері
- Физикалық және химиялық қасиеттері
- Жеке өкілдері
Циклді қосылыстардың аттарын «цикло» деген сөз қосылып май қатары көмірсутектерінің аттары тәрізді етіліп жасалады.
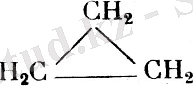
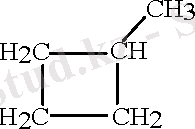
Оларға структуралық изомерияның мына түрлері тән:
- сақинаның үлкен-кішілігі бойынша, мысалы үшін С6Н12
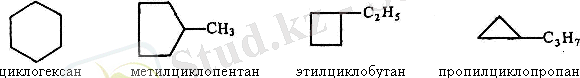
2) сақинадағы орын басушылардың үлкен-кішілігіне қарай:

3) сақинада орын басушылардың орналасуларына қарай:
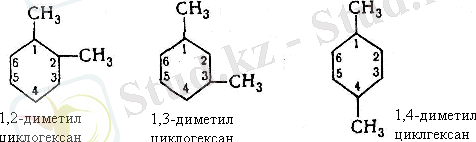
4) орын басушылардың құрылысына қарай:
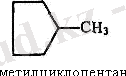
Сақинада бір ғана орын басушы болса, стереоизомерияға орын қалмайды. Екі орын басушы болып қалса геометриялық та, оптикалық та изомерия бола алады.
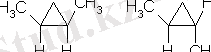
Геометриялық изомерия (цис-транс-изомерия) геминальдық күйінен басқа (орынбасарлар көміртектің бір ғана атомында) орын басушылар күйлерінің барлығында да болады:
Оптикалық изомерия, молекуланың симетриялық жазықтығы болмаған күнде ғана байқалады.
Алу әдістері.
1. Циклопарафиндерді алудың жалпы әдістердің біріне мырышты дигалогенмен әрекеттестіріп туындыларын гологенсіздендіру жатады. Ондай жолмен циклопропан және оның гомологтары оңай алынады:
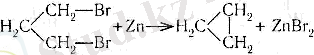
2. Циклопропанды және оның гомологтарын этиленді көмірсутектерге диазометанмен әрекеттестіріп алуға да болады.
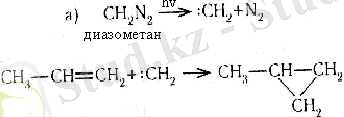
3. Төрт-(одан да көп) буынды циклдері көмірсутектердің цикліндегі атомының сондай санымен қанықпаған көмірсутек сутектетдіріп алуға болады.
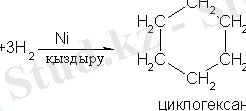
Химиялық қасиеттері.
1. Сутектендіру.
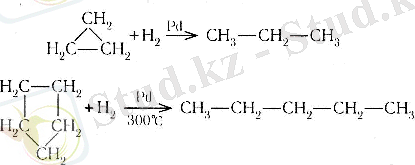
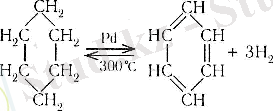
2. Галогендендіру.
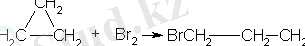
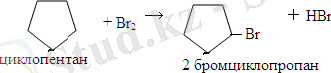
3. Галогенсутектердің қосылуы.
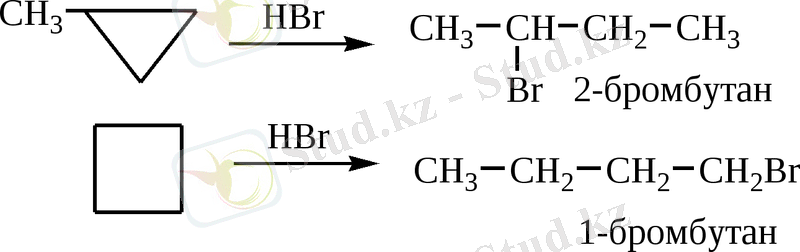
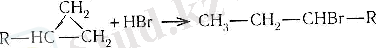
4. Тотығу реакциясы. Күшті тотықтырғыштар әсер етсе циклопарафиндер циклдерін үзіп көміртек атомының саны өздерінікіне тең екі негізгі қышқылдар түзеді. Циклопарафиндердің изомерлік олефиндерден өзгешеліктері олар көміртек атомдарының саны кем қышқылдар немесе карбонилді қосылыстар түзетіндігінде.
Жеке өкілдері. Қарапайым циклопарафин-циклопропан - қайнау температурасы -34 0 С газ күйіндегі зат. Өнеркәсіп мөлшерінде этанолға араласқан мырыштың тозаңымен 1, 3-дихлорпропанға әрекеттестіру арқылы алынады, ол нигаляциялық, анестездегіш құралдар ретінде қолданылады.
1, 3-дихлорпропанды пропанды 100 0 С-де газ күйіндегі хлор мен хларландырып алады. Бұл процесте құрамында 19, 3% 1, 3-ди-хлор-пропан бар, дихлоридтердің қоспасы түзіледі, қайнау температураларының айырмашылығы болғандықтан 1, 3-дихлорпропан басқа изомерлерден оңай бөлініп шығарылады.
Циклогексан-қайнау температурасы 81 0 С сұйық зат. Бензол сутектендіріп алынады. Адипин қышқылын және капролактам алуда еріткіш есебінде қолданылады.
Дәріс материалдарын игергеннен кейін білуге қажетті негізгі түсініктер: циклоалкандардың номенклатурасы мен изомериясы, физикалық және химиялық қасиеттері, жеке өкілдері
Өзін өзі бақылауға арналған сұрақтар:
- Алициклды қосылыстарды қандай жолмен алады?
- Алициклді қосылыстардың химиялық қасиеттері қандай?
- Алициклді қосылыстарға тән изомерия?
Ұсынылған әдебиеттер:
1. Бруис, П. Ю. Органикалық химия негіздері. 1-бөлім: оқулық /П. Ю. Бруис; [қазақ тіліне ауд. Бажықова К. Б. ] - Алматы: Полиграфкомбинат, 2013. 93, 115-127 б.
2. В. Л. Белобородов, С. Э. Зурабян, А. П. Лузин, Н. А. Тюкавкина. Органическая химия. - М. : Дрофа, 2008. -Кн. 1, С. 171-182
3. В. Ф. Травень. Органическая химия. - М. : Академкнига, 2008. Т. 1., С. 208-232
Микромодуль 2 - Ароматты көмірсутектер және олардың туындылары
Дәріс 5, 6-Ароматты қосылыстар
Дәріс жоспары:
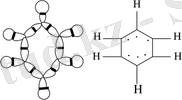
- Ароматтылық. Кекуле формуласы.
- Бензол құрылысы туралы замануи электрондық және кванттық-химиялық көзқарастар
- Бензол және оның гомологтары
Ароматикалық көмірсутектер- құрамында бір немесе бірнеше бензол сақиналары бар заттар жатады. Жалпы формуласы С n Н 2n-6 .
Классификациясы:
- Гомоциклді ароматты қосылыстар
- Гетероциклді ароматты қосылыстар



Пиридин Пиррол фуран
Гомоциклді ароматты қосылыстардың ең қарапайым өкілі бензол. Формуласы С 6 Н 6 . Бензолдың бірнеше құрылымдық формулалары бар.
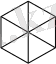
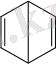

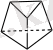
АрмстронгБайер Дьюар Клаус Ладенбург
Бірақ осылардың ішінен ең ықтималдысы кекуле формуласы болып табылады. Оны эксперименттік түрде дәлелдеген.

Бензол малекуласында барлық алты көміртек атомы бір-бірімен 2σ-байланыс арқылы, ал бір атомы 1σ-байланыспен сутегіне байланысқан.
Сурет. 1 σ - байланысының түзілуі
Сонымен қатар көміртегі атомдарының әр қайсысының бір-бірден р-электроны бар. Осы р-электрондары арқылы π секстет түзеді. Секстет дегеніміз алтыны білдіреді.
Изомериясы бүйір тізбегіндегі көміртегі атомдарының санына және орналасу тәртібіне байланысты.
Хюккельдің ароматтылық ережесі
Кез-келген жазық орналасқан тұйық система ароматты болады, егер оның құрамындағы гибридтелмеген р-электрондарының саны 4n+2 ге тең болса (n=0, 1, 2, 3…)
Хюккель ережесіне мысал:
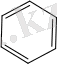
1) циклді +
2) копланарлы+
(барлық көміртегі sp 2 гибриттелген)
3) 4n + 2 = 6
бензол n = 1 ароматты
- циклді +
- копланарлы +
- 4n + 2 = 10
n = 2 ароматты
нафталин
- циклді +
- копланарлы емес -
- 4n + 2 = 4
n = 0, 5ароматты емес
циклопентадиен
- циклды +
- копланарлы емес -
- 4n + 2 = 6
n = 1 ароматты емес
циклогептатриен
- циклды +
- копланарлы +
- 4n + 2 = 6
n = 1 ароматты
тропилий катионы
Дәріс материалдарын игергеннен кейін білуге қажетті негізгі түсініктер: ароматтылық, Кекуле формуласы, бензол құрылысы туралы замануи электрондық және кванттық-химиялық көзқарастар, бензол және оның гомологтары
Өзін өзі бақылауға арналған сұрақтар:
- Қандай қосылыстар ароматтылыққа ие?
- Неліктен бензол және оның гомологтары ароматты қосылыстарға жатады
- Бензолдың құрылысы жайлы қандай көзқарастар бар?
Ұсынылған әдебиеттер:
1. Бруис, П. Ю. Органикалық химия негіздері. 1-бөлім: оқулық /П. Ю. Бруис; [қазақ тіліне ауд. Бажықова К. Б. ] - Алматы: Полиграфкомбинат, 2013. 293-330 б.
2. В. Л. Белобородов, С. Э. Зурабян, А. П. Лузин, Н. А. Тюкавкина. Органическая химия. - М. : Дрофа, 2008. -Кн. 1, С. 249-298
3. В. Ф. Травень. Органическая химия. - М. : Академкнига, 2008. Т. 1., С. 380-384, 411-457
Дәріс 7, 8-Бензол және оның гомологтары
Дәріс жоспары:
- Бензолдың гомологтық қатары.
- Изомерия. Номенклатура.
- Ароматты қосылыстардың көзі. Синтетикалық алу әдістері.
- Химиялық қасиеттері.
- Орынбасу реакцияларының механизмі. Орынбасарлардың бағыттаушы әсердің механизмі.
Бензол гомологтары:
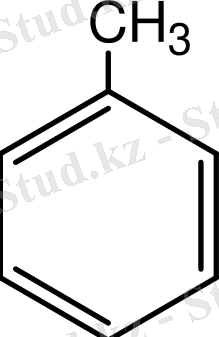
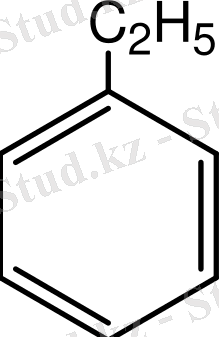
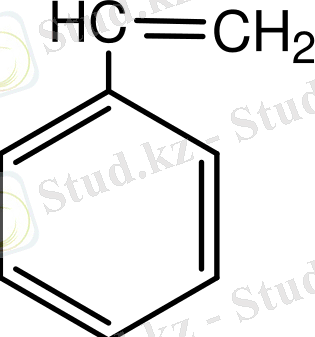
Изомерия . Құрылымдық изомерия

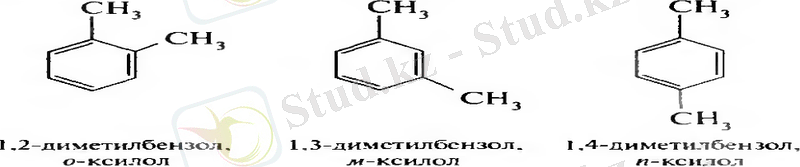
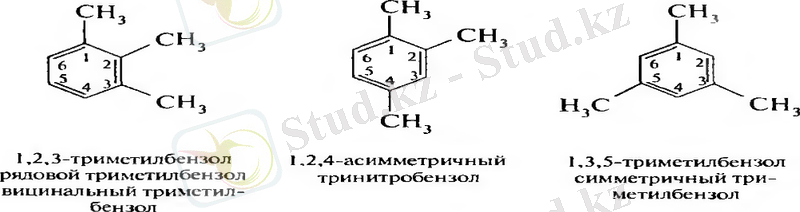
Бензолды алу жолдары:
- Өндірісте: бензол және оның гомологтарын мұнайдан, кокс газынан, тас көмір шайырынан алады.
- лабораториялық әдіс
- Бензойқышқылын декарбоксилисациялау:
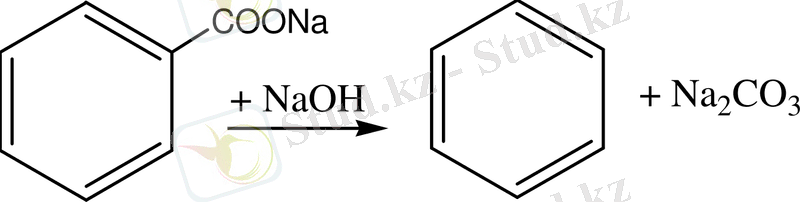
2. Вюрца-Фиттиг реакциясы
Физикалық қасиеті. Бензол және оның гомологтары - түссіз сұйықтық. Олар суда еримейді, бірақ органикалық еріткіштерде ериді
Бензолдың химиялық қасиеттері.
Бензол және олардың гомологтарына тән химиялық қасиетті S E 2
Электрофильдік орынбасу реакциясы.
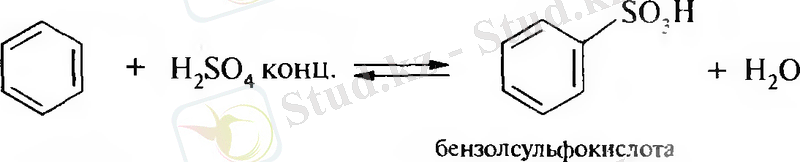
Қосылу реакциялары:
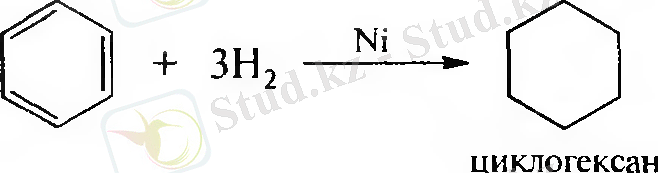
Тотығу реакциясы:
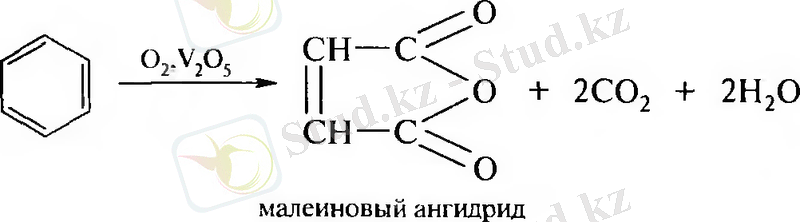
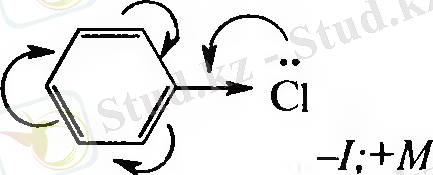
І текті орынбасарлар - орто-пара-ориентанттар. Оларға жатады: радикалдар, - ОН, -NH 2 , - NHR, - NR 2 , -ОН, OR, - NHCOR, -OCOR, -SH, - галогендер.
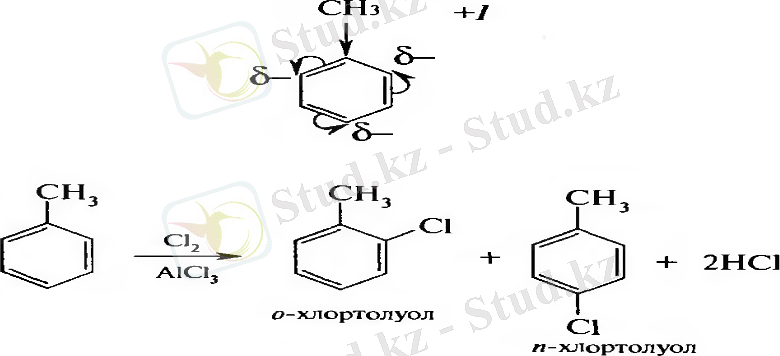
ІІ текті орынбасарлар - мета-ориентанттар. Оларға жатады:
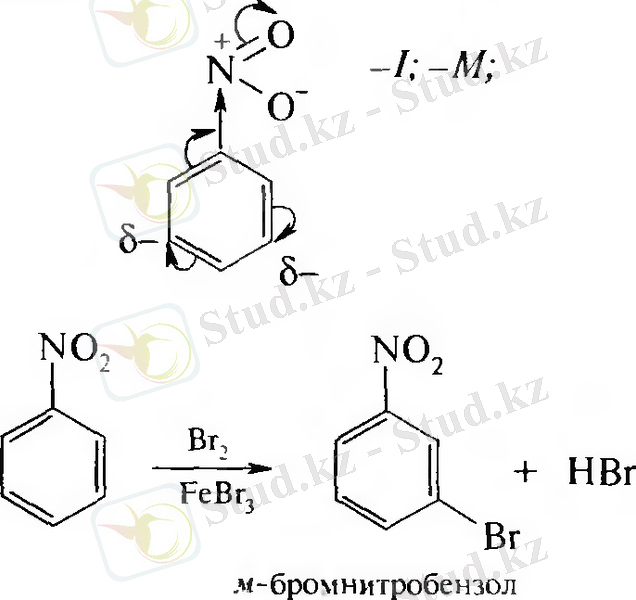
Дәріс материалдарын игергеннен кейін білуге қажетті негізгі түсініктер: бензол және оның гомологтарының изомерия, номенклатурасы, физикалық және химиялық қасиеттері, І және ІІ текті орынбасарлар
Өзін өзі бақылауға арналған сұрақтар:
- Бензолдың алу жолдары?
- Электрофильді орын басу реакцияларының механизмі?
- І текті орынбасарлардың бағыттаушы әсері неде?
Ұсынылған әдебиеттер:
1. Бруис, П. Ю. Органикалық химия негіздері. 1-бөлім: оқулық /П. Ю. Бруис; [қазақ тіліне ауд. Бажықова К. Б. ] - Алматы: Полиграфкомбинат, 2013. 293-330 б.
2. В. Л. Белобородов, С. Э. Зурабян, А. П. Лузин, Н. А. Тюкавкина. Органическая химия. - М. : Дрофа, 2008. -Кн. 1, С. 249-298
3. В. Ф. Травень. Органическая химия. - М. : Академкнига, 2008. Т. 1., С. 380-384, 411-457
Дәріс 9, 10 - Ароматты қосылыстардың галоген туындылары
Дәріс жоспары
- Номенклатура. Изомерия
- Синтез әдістері
- Химиялық қасиеттері
Көмірсутек молекуласындағы бір немесе бірнеше сутек атомдарын галогендермен алмастырғанда алынатын туындыларды галоген туындылар деп атайды. Галоген байланысқан радикалдың сипатына қарай галоген туындыларды қаныққын және қанықпаған галоген туындылар деп екіге бөледі. Сонымен бірге молекула құрамында галоген атомының санына қарай әр топтың өз ішінде моно-, ди және полигалоген туындылар болады.
Көмірсутектердің галогентуындылары - көмірсутек молекуласындағы бір немесе бірнеше сутек атомдарының орнын галоген атомдарына алмастырғанда түзілетін қосылыстар. Екі топқа бөлінеді:
1. Галогенарендер - галоген атомы бензол сақинасымен тікелей байланысқан қосылыстар
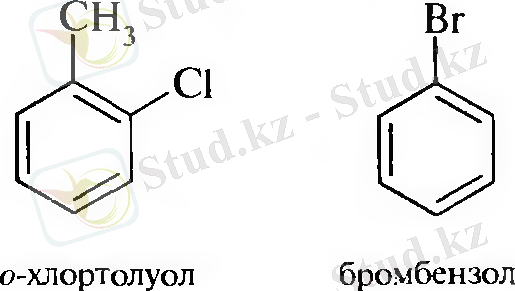
2. Арилалкилгалогенидтер - галон атомдары бұйыр тізбекте орналасқан ароматты қосылыстар
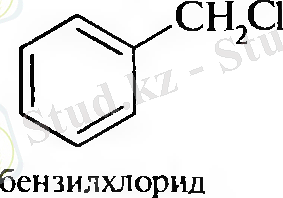
Алу жолдары .
1. Арендерді галогендеу
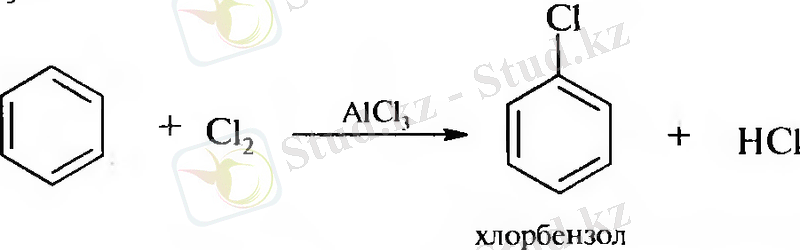
2. Арилдиазоний тұздарының мыс галогенидтерімен әрекеттесу:
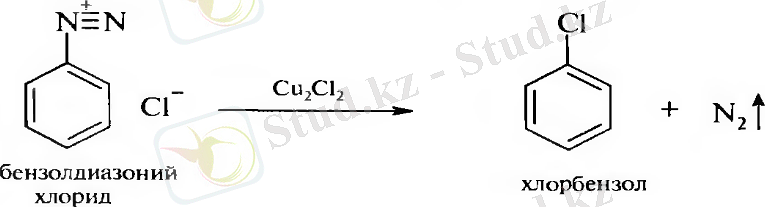
Химиялық қасиеттері.
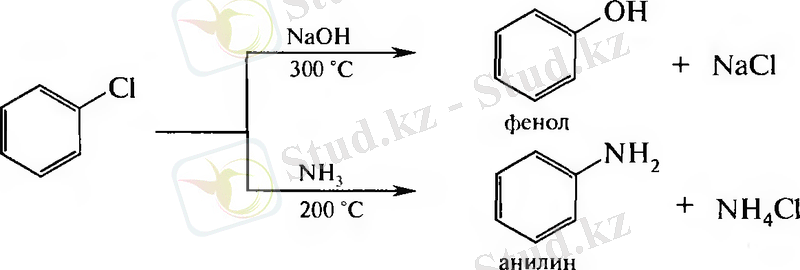
Нуклеофильді орын басу реакциялары қатан жағдайда жүреді:
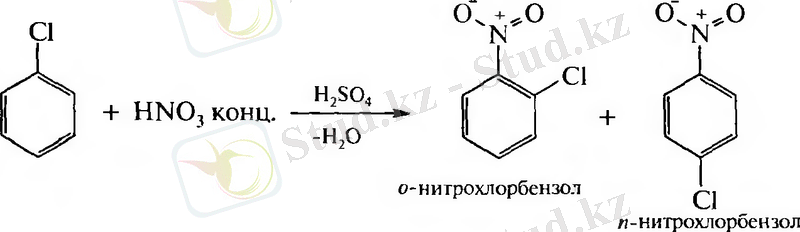
Электрофильді орын басу реакциялары:
Дәріс материалдарын игергеннен кейін білуге қажетті негізгі түсініктер: ароматты галоген туындыларының номенклатурасы мен изомерия, физикалық және химиялық қасиеттері
Өзін өзі бақылауға арналған сұрақтар:
- Галоген туындыларының химиялық қасиеттері
- Галоген туындылардың алу жолдары?
- Қандай химиялық реакциялар галоген туындыларға тән?
Ұсынылған әдебиеттер:
1. В. Л. Белобородов, С. Э. Зурабян, А. П. Лузин, Н. А. Тюкавкина. Органическая химия. - М. : Дрофа, 2008. -Кн. 1, С. 298-340
2. В. Ф. Травень. Органическая химия. - М. : Академкнига, 2008. Т. 1., С. 636-653
Дәріс 11, 12-Ароматты сульфоқышқылдар
Дәріс жоспары:
- Метилцеллюлоза. Алынуы, қасиеттері, қолданылуы
- Натрий-
Молекуласында сульфатобы бар ароматты көмірсутектердің туындыларын ароматты сульфоқышқылдар дейді.
Алу жолдары. Ароматты сульфоқышқылдарды бензолды және оның гомологтарын сульфирлеу арқылы алады. Сульфирлеу реакциясы әдеттегі электрофильді орынбасу механизмімен жүреді. Төмендегі схемамен түзілетін гидросульфон ионы реагент болады.
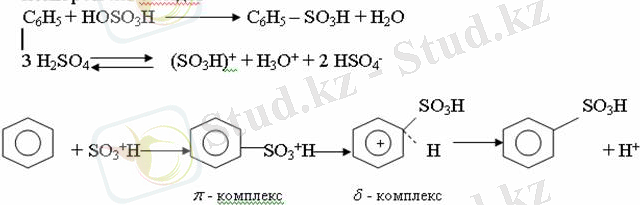
Химиялық қасиеті.
Сульфоқышқылдардағы бензол сақинасы электрофильді орынбасу яғни галогендеу, нитрлеу және сульфурлеу реакцияларына түседі. Электроноакцепторлы сульфотоп бензол сақинасындағы пи электрондарды өзіне қарай тартып, сақинаның электрондық тығыздығын кемітеді. Электрондық тығыздық орто- және пара- жағдайларда көбірек кемиді, келесі орынбасушы м-жағдайға орналасады.
І. Сульфотоптың реакциялары:
1. тұздардың түзілуі
C 6 H 5 SO 3 H + NaOH → C 6 H 5 SO 3 Na + H 2 O
2. хлоронгидридтердің түзілуі
C 6 H 5 SO 3 H + PCl 5 → C 6 H 5 SO 2 Cl + H 2 O
C 6 H 5 SO 2 Сl + 2 NH 3 →C 6 H 5 SO 2 NH 2 + NH 4 Cl
ІІ. Электрофильді орынбасу реакциялары
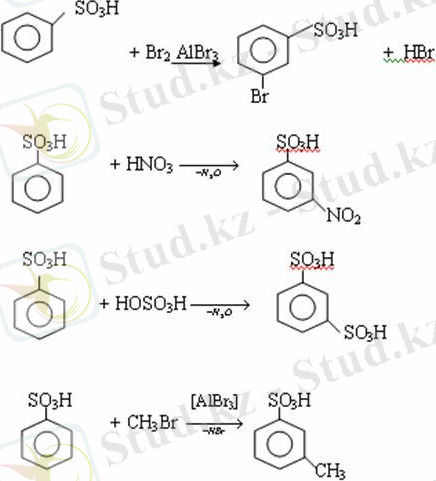
Дәріс материалдарын игергеннен кейін білуге қажетті негізгі түсініктер: ароматты сулфоқышқылдардың электрондық құрылысы, номенклатура, изомерия, химиялық қасиеттері, қолданылуы
Өзін өзі бақылауға арналған сұрақтар:
- Ароматты сульфоқышқылдарға қандай реакциялар тән?
- Ароматты сульфоқышқылдар қандай электрондық эффектілерді көрсетеді?
- Ароматты сульфоқышқылдарды қандай жолмен алады?
Ұсынылған әдебиеттер:
1. В. Л. Белобородов, С. Э. Зурабян, А. П. Лузин, Н. А. Тюкавкина. Органическая химия. - М. : Дрофа, 2008. -Кн. 1, С. 298-340
2. В. Ф. Травень. Органическая химия. - М. : Академкнига, 2008. Т. 1., С. 332-343
Дәріс 13, 14-Ароматты нитроқосылыстар
Дәріс жоспары:
- Нитроқосылыстардың құрылысы
- Номенклатура, изомерия
- Алу жолдары
- Химиялық қасиеттері
Молекуласында тікелей бензол сақинасымен байланысқан немесе бүйір тізбекте орналасқан бір немесе бірнеше нитротопшалары бар қосылыстарды ароматты нитроқосылыстар деп атайды.
Ароматты нитроқосылыстар екі топқа бөлінеді: 1. Нитротобы бензол сақинасымен тікелей байланысты, 2. Нитротобы бүйыр тізбекте орналасқан орналасқан қосылыстар
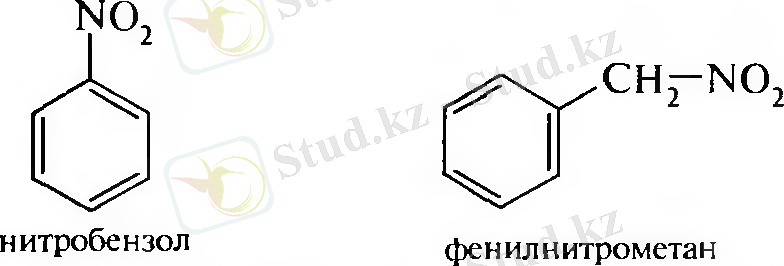
Алу жолдары. 1. Арендерді нитрлеу
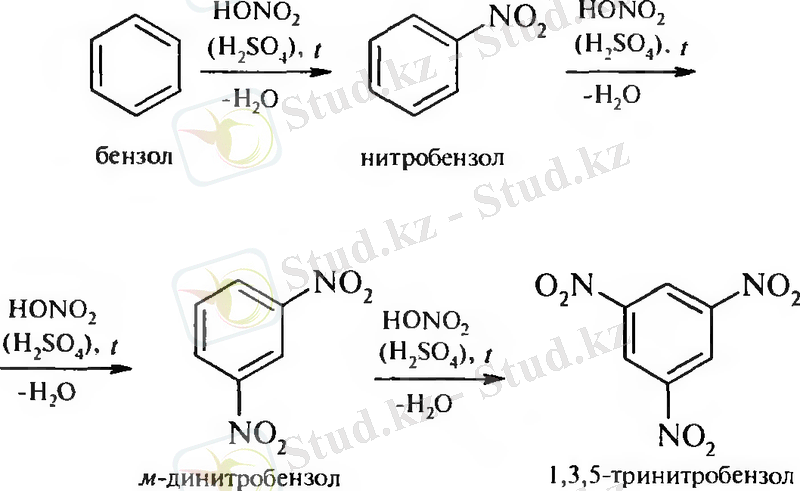
Химиялық қасиеттері. І. Нитротоп бойынша
1. Зинин реакциясы (қышқыл ортада)
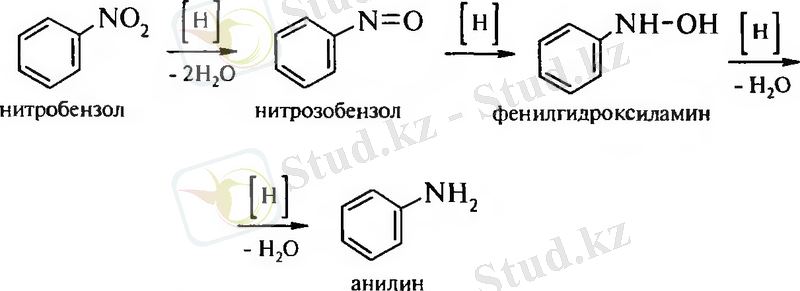
ІІ. Ароматты сақина бойынша реакциялар
1. Электрофильді орын басу реакциялары
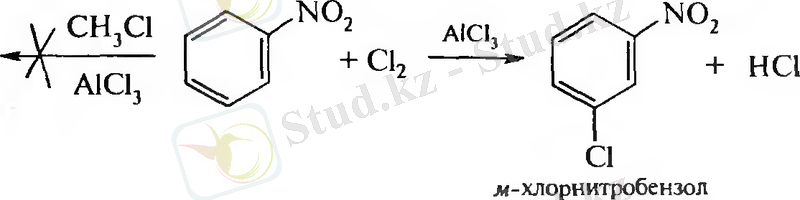
2. Нуклеофильді орынбасу реакциялары
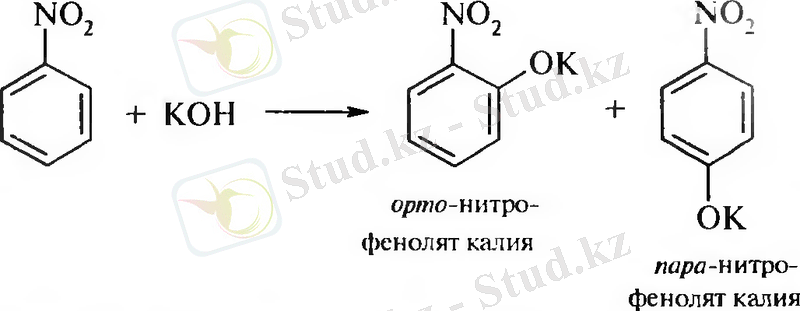
Дәріс материалдарын игергеннен кейін білуге қажетті негізгі түсініктер: ароматты нитроқосылыстардың электрондық құрылысы, алу жолдары, номенклатура, изомерия, химиялық қасиеттері.
Өзін өзі бақылауға арналған сұрақтар:
- Нитротоптың құрылысын сипаттаңыз?
- Ароматты нитроқосылыстарға қандай реакциялар тән?
- Ароматты нитроқосылстарды қандай жолмен алады?
Ұсынылған әдебиеттер:
1. В. Л. Белобородов, С. Э. Зурабян, А. П. Лузин, Н. А. Тюкавкина. Органическая химия. - М. : Дрофа, 2008. -Кн. 1, С. 531-541
2. В. Ф. Травень. Органическая химия. - М. : Академкнига, 2008. Т. 1., С. 348-356
Дәріс 15, 16-Ароматты аминдер
Дәріс жоспары:
- Ароматты аминдердің номенклатурасы, изомериясы, классификациясы
- Алу жолдары
- Химиялық қасиеттері
Молекуласында бензол сақинасымен байланысқан амин тобы (-NH 2 ) бар қосылыстарды ароматты аминдер деп атайды.
Ароматты аминдері алифатты аминдер секілді амиактың туындылары ретінде қарауға болады. Қарапайым өкілі - анилин. Соған сәйкес, ароматты аминдер де біріншілік (I), екіншілік (II) және үшіншілік (III) болып бөлінеді:
Ar - NH 2 (Ar) 2 NH (Ar) 3 N
I II III
Молекуласында екі амин топшасы бар қосылыстарды диаминдер дейді. Әдетте, ароматты аминдерді тарихи номенклатура бойынша атайды. Халықаралық номенклатура бойынша радикалдың атына амин деген сөзді қосып атайды:
Қосылыстар: Т. Н. Х. Н.
C 6 H 5 - NH 2 анилин фениламин
C 6 H 5 - NH - CH 3 N - метиланилин метилфениламин
CH 3 - C 6 H 4 - NH 2 толуидин толуиламин
Алу жолдары. 1. Нитроқосыларды тотықсыздандыру (Зинин реакциясы)
2. Галогентуындылардың аммиак пен аминдер мен әрекеттесу
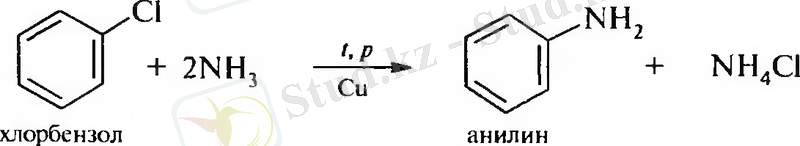
3. Біріншілік аминдерді алкилдеу
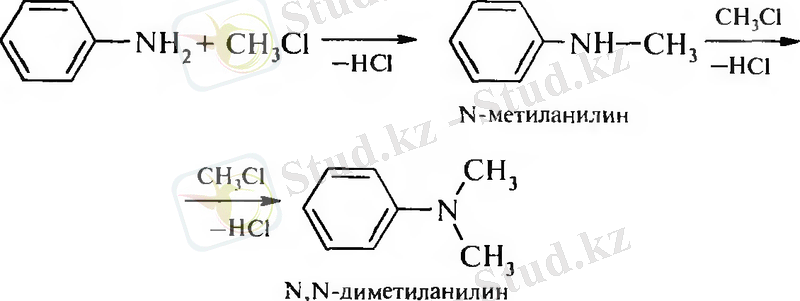
Химиялық қасиеттері.
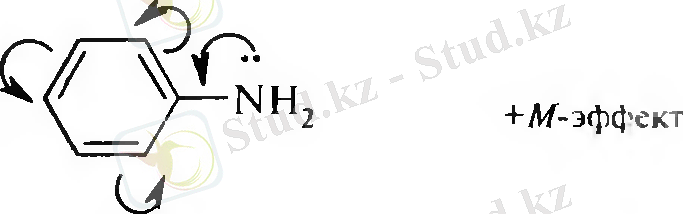
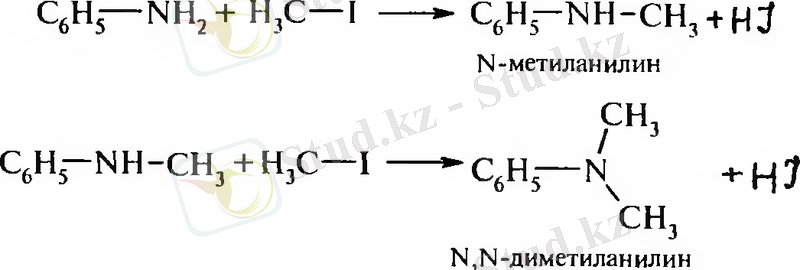
1. Алкилдеу реакциясы
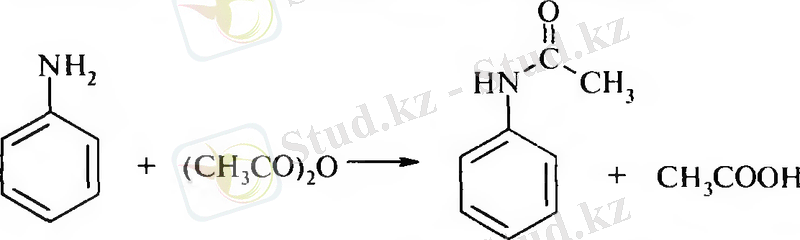
2. Ацилдеу реакциясы
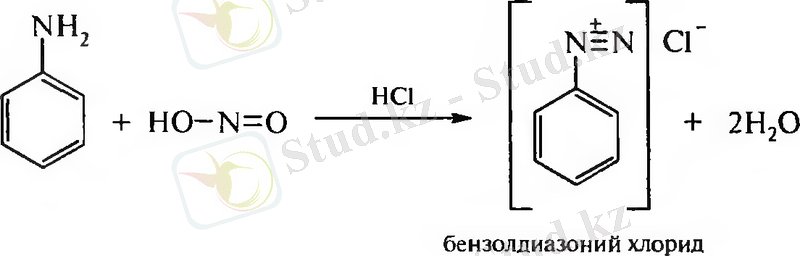
3. Азотты қышқылымен әрекеттесу
Біріншілік аминдер:
Екіншілік аминдер:
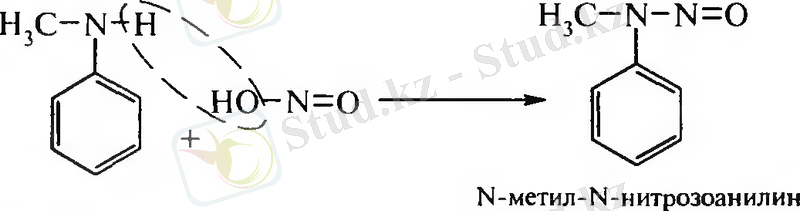
Үшіншілік аминдер:
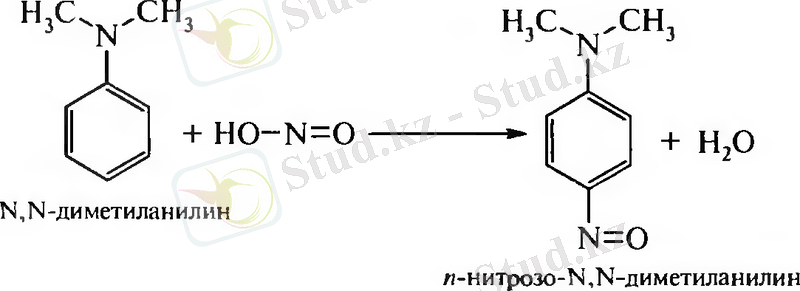
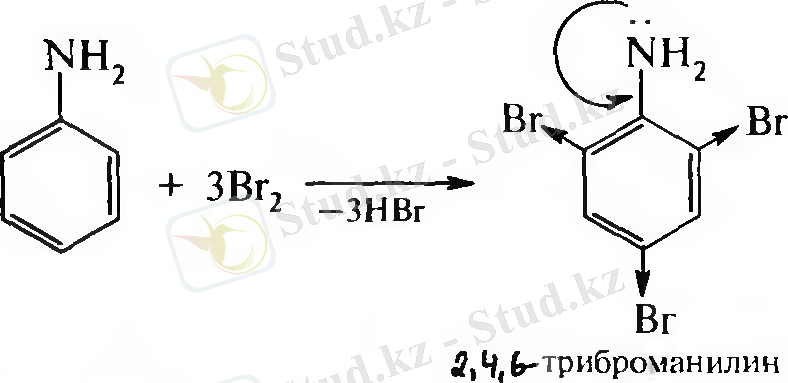
4. Электрофильді орынбасу реакциясы
Дәріс материалдарын игергеннен кейін білуге қажетті негізгі түсініктер: ароматты аминдердің классификациясы, номенклатурасы және изомериясы, алу жолдары, химиялық қасиеттері
Өзін өзі бақылауға арналған сұрақтар:
- Ароматты аминдер азотты қышқылмен қалай әрекеттеседі?
- Триброманилинді алу жағдайы ?
- пара-нитротолуолға сутегімен ( катализатор қатысында ) әсер етсе, түзілетін заттың аты мен формуласын жазыңыз.
Ұсынылған әдебиеттер:
1. В. Л. Белобородов, С. Э. Зурабян, А. П. Лузин, Н. А. Тюкавкина. Органическая химия. - М. : Дрофа, 2008. -Кн. 1, С. 514-541
2. В. Ф. Травень. Органическая химия. - М. : Академкнига, 2008. Т. 1., С. 361-405
Дәріс 17, 18-Диазо- және азоқосылыстар
Дәріс жоспары:
- Құрылысы. Алу тәсілдері
- Химиялық қасиеттері
- Азоқосылыстар
Ароматтық диазоқосылыстар деп құрылымы әртүрлі, бірақ бір-біріне оңай айналатын қосылыстарды айтады.
Құрылысы. Алу тәсілдері
Диазоний тұздарының құрылымы мынадай:
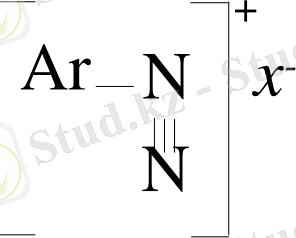 мысалы
мысалы
 немесе
немесе
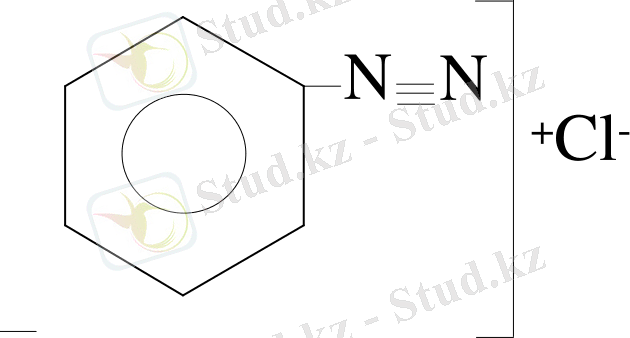
хлорлы бензол диазоний тұзы
Өзінің сипаты бойынша олар аммоний тұздарына ұқсас.
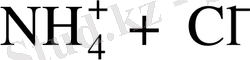
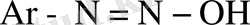 қосылыстар диазогидраттар деп аталады. Оларға амфотерлік қасиеттер тән және сілтілердің әрекет етумен диазотаттар
қосылыстар диазогидраттар деп аталады. Оларға амфотерлік қасиеттер тән және сілтілердің әрекет етумен диазотаттар
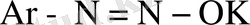 , ал қышқылдардың әсерінен диазоний тұздарын түзеді.
, ал қышқылдардың әсерінен диазоний тұздарын түзеді.
Диазоний тұздары ең маңызды қосылыстар болып табылады.
Аминдерден диазоқосылыстардың түзілу реакциясын диазоттау деп атайды. Диазоттау амин тұдарының тұздағы ерітіндісіне, артығымен алынған минералдық қышқылдың қатысуымен, өз тұздарынан алынатына азотты қышқылмеи әрекет ету арқылы өткізіледі. Реакция былайжүреді:
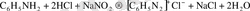
Қышқылдың артық мөлшері диазоний тұздарын тұрақтандыру үшін қажет. Ол жоқ болса қосалқы реакциялар орын алады.
Осындай жолмен диазоний тұздарының судағы ерітінділерін алады. Әдетте бұл тұздар суда жақсы ериді, электр тогын жақсы өткізеді.
Аминдерден диазоқосылыстардың түзілуін келесі жолмен көрсетуге болады. Қышқылды ортада азотты қышқыл бірнеше диазотоптағыш агенттерді
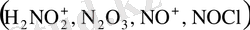 береді.
береді.
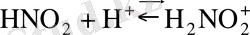
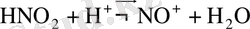
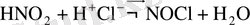
Олардың әрқайсысының реакциядағы ролі қышқылдың концентрациясына және аминнің негізділігіне тәуелді. Олардың барлығы да аминдермен әрекеттесіп нитрозоаминдерді түзеді, бірақ нитрозоаминдер қышқылдық ортада қайтадан диазовий тұздарына айналады.

нитрозоамин
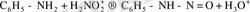

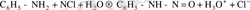

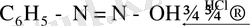
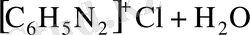
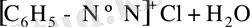
Диазоний тұздарының ерітінділерін сілтілегенде диазогидраттар түзіледі. Бірақ олар бос күйінде бөлініп алынбайды. Себебі, олар амфотерлік қосылыстар есебінде сілтілермен бірден реакцияға түсіп, диазотаттар түзеді.
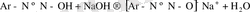
натрий диазотаттары
Диазоний тұздарының сілтілермен реакциясын жалпы мына схемамен қорытындылай белгілеуге болады.
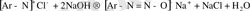
Химиялық қасиеттері. Диазоний тұздары реакцияға қабілетті органикалық қосылыстар болып табылады. Олар мұнай - химиялық синтездің аралық өнімдері болып есептеленеді.
Диазоқосылыстарға тән реакцияларды екі түрге бөліп қарастырады:
диазоқосылыстардың азотты бөле жүретін химиялық реакциялары;
диазоқосылыстардың азотты бөлмей жүретін химиялық реакциялары.
І. Азотты бөле жүретін химиялық реакциялары
1. Диазоний тұздарының қышқыл ерітінділерін қайнатқанда азот бөлініп шығады және фенолдар алынады.

2. Диазоний тұздарымен йодты калийды қыздырғанда амин тобы йодқа алмасады:
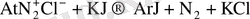
3. Диазотоптың басқа атомдарға немесе топтарға алмасуы катализатор ретінде тиісті мыс тұздарын қолдануды қажет етеді:
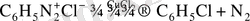
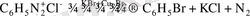
4. Әйгілі орыс ғалымы Несмьянов, диазоний тұздарына металл ұнтақтарымен әрекет ету арқылы көптеген металдардың, металорганикалық қосылыстарын алу әдісін жүзеге асырды, мысалы:

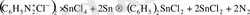
5. Формальдегидтіңәсері:

6. көмігімен де жүзеге асырылады

ІІ. Азотты бөлмей жүретін химиялық реакциялары
1. Диазоқосылыстарды тотықсыздандыру.
2. Диазоқосылыстарды тотықтыру.
Диазотоптарды сутегінің асқын тотығымен тотықтырғанда нитроаминдер және алынады.
3. Азобірігу реакциясы.
Бұл реакция сілтілік ерітіндіде фенолдарды және әлсіз қышқылдық ерітіндіде ароматты аминдерді диазоний тұздарымен әрекеттестіру арқылы жүреді:
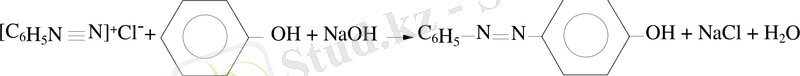
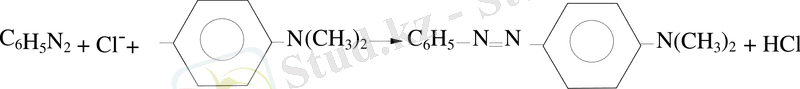
Азоқосылыстар.
Азоқосылыстар түрлі бояғыш заттар, себебі құрамында хромофорлы
 тобы бар, ол спектрдің көрінетін аймағында сәуле сіңіруге пайдалы әсерін тигізеді. Окси - және аминоазоқосылыстар да бояғыштар болып саналады.
тобы бар, ол спектрдің көрінетін аймағында сәуле сіңіруге пайдалы әсерін тигізеді. Окси - және аминоазоқосылыстар да бояғыштар болып саналады.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz