Мектептік электролиз аппаратын құрастыру және электротехника қалдықтарынан бағалы металдарды бөліп алу


Қазақстан Республикасы Алматы облысы
Еңбекшіқазақ аудандық білім бөлімінің
«Рахат ауылдық округі №1 орта мектеп»
коммуналдық мемлекеттік мекемесі
Ғылыми жоба:
«Мектеп бағдарламасына сәйкес электролиз аппаратын құрастыру және электротехника қалдықтарынан бағалы металдарды бөліп алу»
Дайындаған: 10«А» сынып оқушысы
Исқақбай Бексұлтан,
9«Б» сынып оқушысы
Бақатай Жанель
Жетекшісі: Химия ғылымдарының
магистірі, химия пәнінің мұғалімі
Нұртай Ерназар
2018-2019 оқу жылы
Мазмұны:
Кіріспе . . . 1
I. Әдеби шолу . . . 1-3
ІІ. Тәжірибелік бөлім . . . 4-16
2. 1 Электролиз құрылғысын құрастыру, мыс купросынан мыс алуды зерттеу.
2. 2 Катод массасының конентрацияға тәуелді өзгерісі
2. 3 Мыс сульфаты ерітіндісінің сілтілік гидролизі
ІІІ. Қорытынды . . . 17
Ұсыныстар . . . 18
Пайдаланған әдебиеттер . . . 19
Аннотация
Бұл ғылыми жұмыста, оқушы өз қолымен электролиз жүргізуге арналған аппаратты құрастырады әрі сол құрылғының көмегімен, электролиз процесстерін бақылауды үйреніп, көне электротехниканың құрамындағы бағалы металдарды бөліп алады. Оқушыны осы арқылы теориялық білімді практикамен ұштастыра отырып, ғылымға деген қызығушылығын арттырады, ғылымға жол бастайды.
Аннотация
В этой статье ученик строит свой собственный электролизный аппарат с помощью этого устройства, изучает контроль процессов электролиза и распределяет драгоценные металлы в электротехнике. Теоретические знания в сочетании с практикой повышают интерес к науке и ведут к науке.
Annotation
In this investigation work student builds his own electrolytic device, and with this devise will study the process of electrolysis and obtaining gold metal from E-WASTE. Theoretical concepts where they are used and will go to start on scienes.
Зерттеу мақсаты:
- Электролиз жүргізуге арналған, қарапайым әрі қолайлы құрлғы құрастыру, Оны практикада пайдаланып, мыс купросынан мысты алу процессі кезіндегі РН мәні мен концентрацияның өзгерісін зерттеу . Осы арқылы келесі жұмыстарда, бағалы металдарды ескі электротехникалық құрлғылардың қалдығынан бөліп әдістеріне тәжірибе жинақтау.
- Міндеттері:
- Электролиз аппаратын құрастыру.
- Мыс ертіндісінен мысты бөліп алу процессін зерттеу.
- Ескі электротехникадан бағалы металдарды бөліп алу.
Зерттеу орны : Мектеп лабораторясы (№1 Рахат орта мектебі, Сатпаев орта мектебі)
Ғылыми болжамы: Мектеп бағдарламасында қолдануға қолайлы, қолжетімді аппарат құрастырамыз; Мыс купросынан судағы ертіндісінің РН мәні бірқалыпты азайады, ертіндідегі мыс иондарының концентрациясының артқан сайын шығым уақытқа байлансты бір қалыпты өзгереді.
Зерттеу кезеңдері:
- І. Кіріспе. Электролиз жүргізу құрылғысы туралы мәліметтер жинау, мыс купросын алу жағдайларын талдау, бағалы металдарды бөліу әдісін қарастыру.
- ІІ. Тәжірибелік бөлімде. Эксперементтер жасау, алынған нәтижелерді тіркеу, электролиз процессін қадағалау.
- ІII. Алынған нәтіижелерге талдау жасау. Тәжірибе нәтижесінде алынған мәліметтерді, талдау, анализ жасау.
Зерттеу тәсілдері: Болжам жасау, Ақпарат жинап, мақсат қою, танысу, жоспарлау, эксперимент жасау, талдау, салыстыру, іздену, зерттеу, қортынды шығару.
Зерттеу жаңашылдығы: Оқушы қолымен жассалған электролиз аппаратын, мектептерде пайдалануға болады, арзан, әрі қол жетімді. Электролиз арқылы мысты бөліп алғанда, ортаның РН пен концентрацияны мәнін бақылап отыру.
Кірспе
Электролиз тақырыбы мектеп бағдарламасы бойынша тоғызыншы және оныншы сыныптарды қайталанып келетін маңызды тақырыптардың бірі әрі күрделі тақырып. Қазіргі кезде электролиз әдісімен өндірісте көптеген таза металдар алынады. Шаруашылықтың барлық салаларында және өндірісте электролиз барлық жақты қолданылады. Электролиздің түсті металлургияда қолданылуы: металдардың рафинирлеуі, рудалардан металды бөліп алу үшін. Балқыланған орталардан электролиз арқылы алынған металдар қатарына аллюминий, магний, цирконий, титан, уран, берилий және басқа металдардың қатары. Сулы ерітінділерден бөлініп ала алмайтын металдарды жоғары теріс потенциал нәтижесінде түсті металлургияда балқыған орталадың электролизі нәтижесінде алады. Бұл балқыған орталар болып әртүрлі қоспалардың қосындысынан тұратын тұздар болады. Олар балқыманың балқу температурасын төмендету, электрөткізгіштікті мақсатында жоғарылату үшін қолданылады. Химиялық өндірісте электролиз арқылы хлорат және перхлорат, персульфат, калий перманганаты, хлор және сілтілер, органикалық қосылыстар, химиялық таза сутегі, оттегі фтор және басқа да маңызды өнімдерді алуға болады. Машина жасау, радиотехника, полиграфты қндіріс салаларында электролизді металдар немесе бұйымдар бетіне жұқа жабылғы салу үшін қолданады.
Соған қарамастан мектепте практикалық және зертханалық жұмыстардың орындалмауынан, кей мектептерде ешқандай зертханалық жұмыс жүргізетін жағдайдың болмауынан, практикалық жұмыстар жүргізілмейді. Сол себепті біз ағайдың көрсеткен қарапайым электролиз жасайтыын құрлғысын негізге ала отырып, сабақтан кейін осы құрлғыны жетілдіріп, барлық мұғалімдерге қолжетімді әрі қарапайым құрлғы жинауды қолға алғанбыз. Нәтижесінде ойымыз сәтті жүзеге асып, төмендегідей(1-сурет) құрлғыны әдебиеттермен, интернеттен қарап құрастырып ағайға көрсеткен соң, ағай бұл құрлғыы арқылы тәжірбе жассап зерттеу жұмыстарын жүргізуді айтты.
Әдебиеттерден, электролит деп, ерітіндісі арқылы өтетін токтың нәтижесінде жүретін химиялық процесті айтамыз. Электр тогының өткізгіштеріне мыналар жатады: тұздардың, қышқылдардың, негіздердің сулы ерітінділері. Электр тогын өткізетін заттар мен ерітінділер электролит деген атқа ие болды. Сонымен қышқылдар, негіздер және тұздар электролит болып табылады.
Электролиз нәтижесінде катодта жаңа өнімдердің пайда болуымен электролит молекулалары мен иондарының тотығуы жүреді. Катиондар электрондарды қабылдап, тотықсызданудың төмен дәрежелі иондарға немесе атомдарға айналады. Электролиз нәтижесінде анодта анод материалына жататын немесе электролитте болатын иондар немесе молекулалардың тотықсыздануы жүреді (анод ыдырайды немесе тотықсызданады) . Сол әдіспен, электролиздердің бастапқы өнімдері қышқылдар, негіздер және тұздардың алмасу реакциясы кезіндегі бөлшектері болып табылады, олар өзгермейді, бір заттан екіншісіне ауысады. Бірінші жақты өткізгіштер белгілі, оларда электр электрондар арқылы тасымалданады, ал екінші жақты өткізгіштерде электр иондар арқылы тасымалданады.
Егер металды суға салатын болсақ, оның катиондары сұйықтыққа өте бастайды. Катион бетінде электр зарядының болуына байланысты метал бетінде өлшемі бойынша тең, таңбасы бойынша қарама қарсы болатын заряд артық электрондар түрінде жүреді, яғни металл беті теріс зарядталған болады. Ол өзіне металдың ерітіндіге өткен оң зарядты иондарын біртіндеп тарта бастайды, сол арқылы ктиондар ерітінді көлеміне еркін өте алмайды. Сондықтан, металл мен ерітінді шекарасында теріс жағы металл беті, ал оң жағы еріген иондардың жанасу қабаты болып келетін жазық конденсатор тәрізді жұп электрлік қабат түзіледі. Иондардың аз мөлшері ерігеннен кейіннен ақ жұп қабаттың заряды соншалықты өседі, металдың балқуы тоқталады. Егер металл суға емес, өзінің иондарының ерітіндісне салынған болса, (мвсалы, Сu ті CuSO4 ке салғанда), онда бұл процесс біршама өзгеше болады. Егер ерітінді концентрациясы аз болса, онда жұп электрлік қабаттың түзілуі металдың судағы ерітіндісіндегідей өтеді. Егер ерітіндіде иондар концентрациясы жоғары болса, онда алдымен металл бетіндегі оң зарядталған катиондардың тұнбаға түсуі байқалады. Енді металл беті өзіне теріс иондарды тарта бастайды және жұп электрлік қабат түзіледі. Катиондар металдың бір таңбалы заттарының және оның иондарының ары қарай тұнбаға түсуі тоқталатынға дейін катиондар тұнбаға түседі. Екі теріс таңбалы зарядталған денелер болғанда олардың арасында потенциалдар айырмасының болатыны белгілі. Бұндай потенциалдар айырмасы мұнда да, жұп электрлі қабатта, металл-ерітінді шекарасында байқалады. Иондардың металдан ерітіндіге және қайта өтуі олардың арасында потенциалдар айырмасын тудырады.
Осы процесстерді зерттеу барысында, Электролиздің түсті металлургияда қолданылуы: металдардың рафинирлеуі, рудалардан металды бөліп алу үшін қолданлады екен, сонымен бірге кейбір электротехникада, нақтырақ айтсақ телевизор, процессор сияқты заттарда электр тоғын жақсы өткізу үшін аз мөлшерде бағалі металдар қолданылады. олар бұзылғанда немесе жұмыс істеу мерзімі жеткенде қайта өңдеуге жіберіледі. Сол техниканың құрамындағы, әсіресе, ескі техникада көп мөлшерде алтын, платина кездесетіні әдебиеттерден белгәлі.
Сол бағалы металдарды бөліп алуға электролиз әдісін пайдалану және жетілдіру жұмыстары жұргізілді.
II . Тәжірибелік бөлім
- Бөлім 1- Тәжірибе Электролиз құрылғысын құрастыру мыс купросынан мыс алуды зерттеу.
Ең алдымен электролиз жүргізуге арналған құрлғыны құрастырдық.
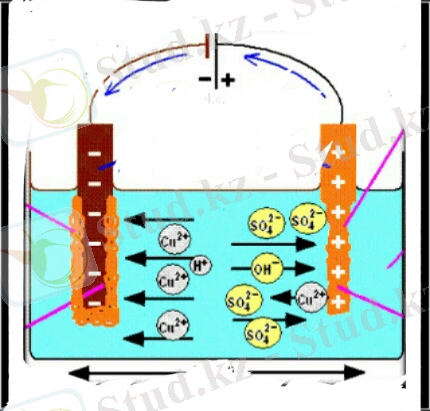

№1 - сурет. Электролиз құрлғысы және жүріу механизімі
2. 1 Электролитты дайындау
Мыс купросының; 1) 0, 1м 2) 0, 2м 3) 0, 3м 4) 0, 4м ертінділерін дайындау үшін СuSO 4 . 5H 2 O, C M = n / V формуласы бойынша 500мл белгісі бар колбаға:
0, 1 малярлы ертінді дайындау үшін 12, 5 г мыс купросын;
0, 2 малярлы ертінді дайындау үшін 25 г мыс купросын;
0, 3 малярлы ертінді дайындау үшін 37, 5г мыс купросын;
0, 4 малярлы ертінді дайындау үшін 50 г мыс купросын салып суда еріттік.
Дайын болған ертінділермен жеке-жеке электролиз жүргіздік.
Электролизді төмендегі берілген схема негізінде жабдықтап, оған өз өзгерістерімізді енгізе отырып, катод ретәнде графитті, ал анод ретінде мысты орналастырып, бөлінген газдың көлемін өлшеуге, электролиттен сынама алып электролиз барысында бақылауға қолайлы болатындай етіп орналастырдық, әрі уақыттың өтіуімен РН мәнінің өзгеруін бақыладық. Ал концентрацияның өзгерісін электролиз басында және соңында сілті иондарының көмегімен анықтадық, келесі жұмыстарды титірлеу арқылы сандық анализ жасаймыз.
2. 2 Катод массасының концентрацияға тәуелді өзгерісі
Электролиз алдында және электролизден кейін катотпен анод массаларын өлшедік.
№1 - кесте 30 минут аралығында әртүрлі концентрацияда катодпен анод массаларының өзгерісі
Теңдеу бойынша катодта бөлінген теориялық шығымды есептедік:
- 0. 1M ертіндіден электролиз нәтіижесінде:
2CuSO
4
+ 2H
2
O
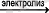 2Cu + O
2
+ 2H
2
SO
4
2Cu + O
2
+ 2H
2
SO
4
320гр, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, 124гр
8гр (0, 1М), ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, , х
Х = 8*124/320 = 3, 1гр(Сu)
- 0. 2M ертіндіден электролиз нәтіижесінде:
2CuSO
4
+ 2H
2
O
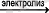 2Cu + O
2
+ 2H
2
SO
4
2Cu + O
2
+ 2H
2
SO
4
320гр, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, 124гр
16гр (0, 2М), ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, , х
Х = 16*124/320 = 6, 2гр(Сu)
- 0. 3M ертіндіден электролиз нәтіижесінде:
2CuSO
4
+ 2H
2
O
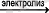 2Cu + O
2
+ 2H
2
SO
4
2Cu + O
2
+ 2H
2
SO
4
320гр, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, 124гр
24гр (0, 3М), ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, , х
Х = 24*124/320 = 9, 3гр(Сu)
- 0. 4M ертіндіден электролиз нәтіижесінде:
2CuSO
4
+ 2H
2
O
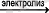 2Cu + O
2
+ 2H
2
SO
4
2Cu + O
2
+ 2H
2
SO
4
320гр, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, 124гр
32гр (0, 4М), ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, ,, , х
Х = 32*124/320 = 12, 4гр(Сu)
№2 - кесте Әртүрлі уақыт аралығында концентрацияның өнімнің шығымы
6А ток күші электролит ерітіндісі арқылы 30 минут, 60 мин, 90мин және 120мин бойы өткен кезде ерітіндіден бөлінген металлды теңдеу бойынша және тоқ бойынша шығымдарын салыстырдық.
Металдың эквиваленттік массасын таптық шығымы Фарадей заңы бойынша шешеміз.
Q=I*t
I- тоқ күші, А
t- уақыт (сек) ,
Электродта бөлінген мыстың массасы
m
=M*Q/ (96500*Z)
M- молекулалық масса, г/моль,
Q- электр қуаты Кл
Z-химиялық эквивалент (мыс -2)
96500- фарадий саны кл/моль
№3 - кесте
тоқ бойынша шығым
Q=6*1800=10800Кл
m=63, 5 *10800/(96500*2) =3, 55г
n =(2, 1/3, 55) *100%=59%
Q=6*3600=21600Кл
m=63, 5 *21600/(96500*2) =7, 1г
n =(6, 2/7, 1) *100%=87, 32%
Q=6*4800= 28800Кл
m=63, 5 *28800/(96500*2) =9, 47г
n =(6, 05/9, 47) *100%=63, 36%
Q=6*7200=43200Кл
m=63, 5 *43200/(96500*2) =14, 21г
n =(8, 1/14, 2) *100%=57%
№2 - диаграмма Өнімнің шығымыныі концентрацияға тәуелділігі
Катодта концентрацияның өзгерісіне байланысты мыстың массасы алдымен артты, содан кемиді, сомен бірге теориялық шығымның мәні кішірейді. тоқ бойынша шығым, теңдеу бойынша шығымға сайкес келмейді. Бұл дегеніміз ертіндіде мыс иондары толық мысқа айналған жоқ. Сондықтан мыс сульфатының электролизы кезінде ең тиімді концентрация 0, 2М концентрацияда 87% шығым бергендіктен осы концентрацияны талдадық .
№4 - кесте 0, 2М СuSO 4 электролиттың РН мәнінің уақытқа тәуелді өзгерісін зерттеу
№4 - диаграмма 0, 2М СuSO 4 электролиттың РН мәнінің уақытқа тәуелді өзгерісін зерттеу
Сулы ертіндіде CuSO
4
төмендегідей диссоцияланады:
CuSO
4
↔︎ Cu(2+) + SO4(2-)
катотқа қарай мыстың катиондары жылжып, 2е
-
қабылдап аладыда мысқа тотықсызданады. Анодқа қарай аниондар жылжыиды сульфат-анион және судың ОН
-
ионы жылжып, он
-
ионы оттекті береді де, ертіндіде H
+
, SO
4
2-
иондары қалып қышқылдық ортаны тудырады, және бұл электролиз барысында артады.
катодта төмендегідей процесс орын алады:
катод (-) анод (+)
Cu(2+) + 2ē → Cu(0) 2H2O - 4ē → 4H(+) + O2 ↑
ертіндіде : H
+
, SO
4
2-
а ) Графит анод
А(+) : 2 H
2
O - 4e ---> 4 H
+
+ O
2
1 - тотығу
К(-) : Сu
2+
+ 2e ---> Cu
0
2 - тотықсыздану
2CuSO
4
+ 2H
2
O = 2Cu + O
2
↑ + 2H
2
SO
4
Егер анод ретінде мысты алсақ реакция нәтіижесінде катодта тек мыс түзіледі де, анод ериді.
б ) Мыс анод болатын жағдайда
А(+) /Сu: Cu
0
- 2e ---> Сu
2+
1 - тотығу
К(-) : Сu
2+
+ 2e ---> Cu
0
1 - тотықсыздану
CuSО
4
= Сu(2+) + SO
4
(2-)
анод (+) : Сu(0) - 2e = Cu(2+),
катод (-) : Cu(2+) + 2e = Сu(0) .
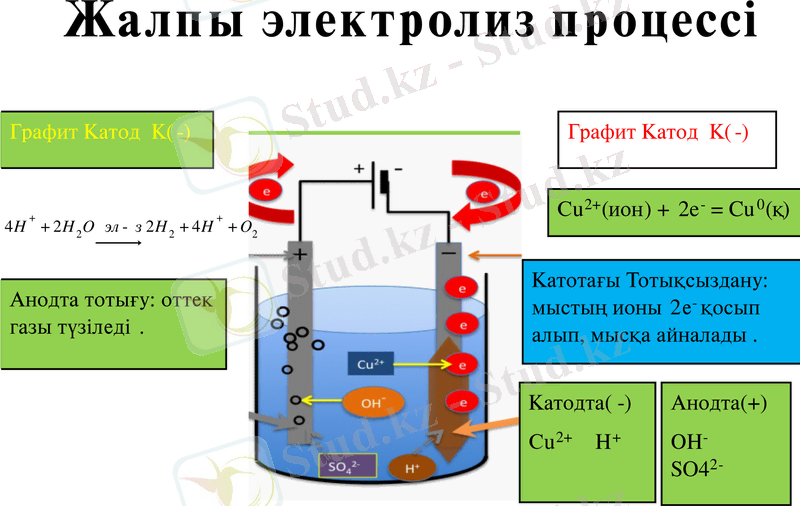
2 - сурет. Мыс купросын электролиздеу процессінің схемасы
2. 2бөлім 2-тәжірибе
1-бөлімде:
Бағалы металы бар делінген компютерді негізі 4 бөлекке жіктедік:
- Пластмассалар
- Сталды қорғаныш бөлшектері
- Көзге көрінетін белгілі мыс бөлектері
- Платалар, разьемдар, микросхемалар, контактлер

1-сурет компютердің бөлшектері
2-бөлімде:
Алдын ала дайындалған патыша сұйықтығана платаларды бөлшектеп салып бір суткаға қалдырдық. Ертесінде платаларды сумен шаймалап ертіндіден бөліп алдық. Бетіндегі металдар толығымен ертіндіге өткен, тек текстильді керамикалық қалдықтарғана қалған.




2-сурет Патыша сұйықтығында еріткенге дейін және одан кейін
3-бөлімде:
Алынған ертіндіден платаларды сумен шаймалап бөліп алдықта ертіндіні азот қышқылының конценртациясын азайту мақсатында құм төселген пеште қыздырдық.

3-сурет патыша сұйықтығын еріген метал концентратын қыздыру працесі
4-басқышта:
Алынған ертіндіні тұндырып, сүзгіден өткізіп филтірлеген соң электролиз арқылы металдарды бөліп алдық. Анод ретінде графит, ал катод ретінде сталь пластинкасын қолдандық. Нәтіижесінде катодтың бетінде алтынмен бірге металдың қоспасы түзілді.

4-сурет Ертіндіні электролиздеу процессі көрцетілген
Ертіндінің екінші бір бөлегін сүзіп тазартқан соң темірсульфаты мен тұнбаға түсіріп тұнбаны ертіндіден бөліп алдық.

5-сурет Ертіндіні FeSO 4 ертіндісімен тұнбаға түсіру
2. 3 Тәжірбелік бөлімге анализ және талдау
... жалғасы- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz