Химическое строение белков: аминокислоты, пептидные связи и уровни структурной организации


Министерство образования и науки Республики Казахстан
Алматинский технологический университет

СРСП
Тема: Современное представление о химическом строении белков
Группа:Тх 19-14
Проверила:
Выполнил:Султанкул М. Б
2020 года
Белки - сложные биополимеры, состоящие из аминокислот.
Все белки представляют собой полимеры, цепи которых собраны из фрагментов аминокислот. Аминокислоты - это органические соединения, содержащие в своем составе (в соответствии с названием) аминогруппу NH 2 и органическую кислотную, т. е. карбоксильную, группу СООН. Из всего многообразия существующих аминокислот (теоретически количество возможных аминокислот неограниченно) в образовании белков участвуют только такие, у которых между аминогруппой и карбоксильной группой - всего один углеродный атом . В общем виде аминокислоты, участвующие в образовании белков, могут быть представлены формулой: H 2 N-CH(R) -COOH.
Общая химическая формула аминокислот (АК), являющихся структурным элементом белковой молекулы, может быть представлена следующим образом:



 R CH COOH
R CH COOH
NH 2
В треугольнике выделена одинаковая для всех
 -аминокислот часть, а R-радикал или боковая цепь, специфична для каждой аминокислоты.
-аминокислот часть, а R-радикал или боковая цепь, специфична для каждой аминокислоты.
Группа R, присоединенная к атому углерода (тому, который находится между амино- и карбоксильной группой), определяет различие между аминокислотами, образующими белки. Эта группа может состоять только из атомов углерода и водорода, но чаще содержит помимо С и Н различные функциональные (способные к дальнейшим превращениям) группы, например, HO-, H 2 N- и др. Существует также вариант, когда R = Н.
В организмах живых существ содержится более 100 различных аминокислот, однако, в строительстве белков используются не все, а только 20, так называемых «фундаментальных».
Студентам следует повторить номенклатуру и основные свойства аминокислот из курса “Органическая химия”.
Свойства аминокислот разнообразны и они во многом определяют свойства белков.
По теории Э. Фишера аминокислоты присоединены друг к другу ковалентной амидной связью, которая возникает при взаимодействии α-карбоксильной группы одной аминокислоты с α-аминогруппой другой
амино
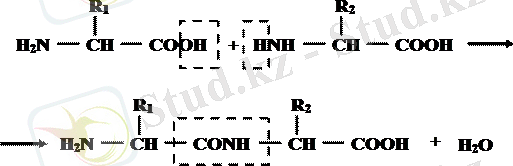
кислоты. При этом выделяется вода.
 Продукты такой реакции называют пептидами, а сама связь между аминокислотами - пептидной.
Продукты такой реакции называют пептидами, а сама связь между аминокислотами - пептидной.
Пептидная связь является повторяющимся фрагментом полипептидной цепи, она имеет ряд особенностей, которые влияют не только на форму первичной структуры белка, но и на высшие формы организации его структуры.
У пептидов на одном конце - свободная аминогруппа, а на другом - карбоксильная. К этим группам могут присоединятся новые аминокислоты, благодаря чему происходит наращивание полипептидной цепи.
Свойства пептидной связи определяют во многом структуру и свойства самих белков. Знать свойства пептидной связи полезно для понимания причин многоуровневой организации белковой молекулы.
Свойства пептидной связи :
1. Пептидная связь копланарна - все атомы, входящие в состав пептидной единицы, находятся в одной плоскости.
2. Вращение вокруг связи C-N отсутствует.
3. C
 -атомы каждой пептидной связи находятся в транс-конформации.
-атомы каждой пептидной связи находятся в транс-конформации.
4. Пептидные группировки обеспечивают максимально возможное число водородных связей (каждая группа -СО-NH- способна образовать две водородные связи с соседними пептидными группами) . Исключение пролин и оксипролин, которые образуют 1 водородную связь), что сказывается на формировании вторичной структуры белка, пептидная цепь на этом участке легко изгибается и молекуле образуются петли (шпильки) .
Структурная организация белковой молекулы имеет определенную иерархию структурных уровней, берущую начало от первичной структуры и заканчивающуюся четвертичной.
Первичная структура Каждый вид белка обладает строгой спецификой аминокислотного состава. уникальностью числа аминокислот и их последовательности в полипептидной цепи, что определяется понятием первичная структурабелка. Первичная структура белка предопределена генетическим кодом клетки. Она определяет пространственную структуру - конформацию белковой молекулы.
Вторичная структура
- это специфическая упорядоченная ориентация полипептидной цепи в пространстве, обусловленная свободным вращением вокруг ее связей, соединяющих
 -углеродные атомы. (упорядоченное пространственное расположение отдельных участков полипептидной цепи) Если торсионные углы равны 45-60
о
, то вторичная структура белка представлена в виде
-углеродные атомы. (упорядоченное пространственное расположение отдельных участков полипептидной цепи) Если торсионные углы равны 45-60
о
, то вторичная структура белка представлена в виде
 -спирали, если углы равны 120-135
о
, то образуется
-спирали, если углы равны 120-135
о
, то образуется
 -структура.
-структура.
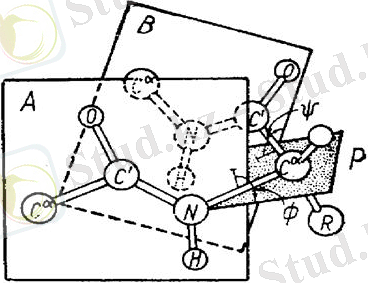 А и В - плоскости двух связанных пептидных единиц; Р - плоскость, содержащая связи С
А и В - плоскости двух связанных пептидных единиц; Р - плоскость, содержащая связи С
 - N и С
- N и С
 - С’, вокруг которых происходит вращение Ф и
- С’, вокруг которых происходит вращение Ф и
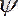 соответственно
соответственно
ПРОСТРАНСТВЕННОЕ РАСПОЛОЖЕНИЕ ТОРСИОННЫХ УГЛОВ В ПОЛИПЕПТИДНОЙ ЦЕПИ
А и В - плоскости двух связанных пептидных единиц; Р - плоскость, содержащая связи С
 - N и С
- N и С
 - С’, вокруг которых происходит вращение Ф и
- С’, вокруг которых происходит вращение Ф и
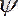 соответственно
соответственно
Отдельные витки спирали удерживаются многочисленными водородными связями с участием водорода аминогруппы и атома кислорода группы СО. При образовании спиралей радикалы, карбоксильные группы и аминогруппы остаются снаружи, что обуславливает возможность образования третичной структуры белка.

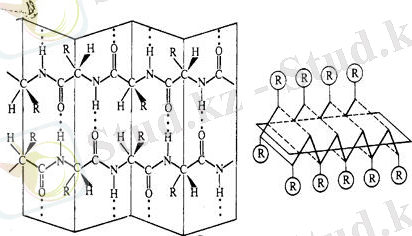

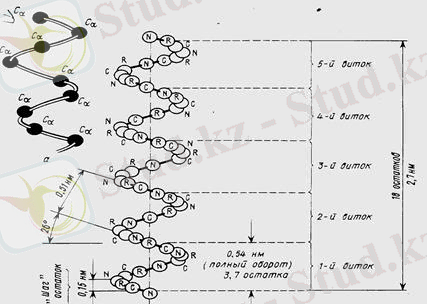
В пространстве аминокислотные остатки, составляющие белковую полипептидную цепь, плотно упакованы за счет примыкания друг к другу их боковых цепей за счет так называемого стэкинг-взаимодействия (англ. stack-стопка, кипа) .
Третичная структура Полипептидная цепь складывается в пространстве в уникальную для каждого белка трехмерную конфигурацию, которая называется третичной структурой или конформацией белковой молекулы. Третичная структура определяет вид молекулы под микроскопом и поведение ее в различных средах.
Глобулярные белки по третичной структуре можно разделить на пять групп:
1. α-белки - белки с большим количеством спиральных структур
2. β-белки - белки, глобулы кот-х состоят из двух и более β-складчатых слоёв.
3. α / β-белки - представляют полипептидную цепь, состоящую из чередующихся α-спиралей и вытянутых β-участков цепи, сгруппированных в один β-слой.
4. (α + β) - белки, представляющие собой полипептидную цепь, разделенную на участки, целиком состоящие из спиралей, и на участки, имеющие форму β-складчатого слоя.
5. белки без α, β - это белки, в структуре которых практически нет спиральных и складчатых участков. Молекулярные глобулы состоят из ясно различимых долей - доменов.
Основные связи, стабилизирующие третичную структуру молекулы белка:
водородные связи между боковыми цепями аминокислотных остатков;
водородные связи между пептидными единицами;
ионные связи;
ван-дер-ваальсовы силы;
гидрофобные взаимодействия
Типы химических связей в белковой молекуле
В биомолекулах химические связи можно разделить на ковалентные и нековалентные. К ковалентным относятся пептидная и дисульфидная связи. Важную роль в поддержании пространственной структуры биологических молекул играют более слабые, чем ковалентные, химические связи (водородные и ионные связи, ван-дер-ваальсовы силы, гидрофобные взаимодействия) .
Водородные связи. Этот тип появляется при электростатическом взаимодействии атома водорода с частично положительным зарядом и ковалентно связанного атома кислорода (азота) с отрицательным зарядом. Способность к образованию водородных связей ярко выражена у соединений, содержащих группы -СО, -NH, -ОН, -СОО-, -СОН.
В белковой молекуле водородная связь может образовываться между группировками пептидных цепей и боковыми цепями аминокислот. Водородные связи бывают внутримолекулярными и межмолекулярными. Единичная водородная связь довольно слабая и непрочная, однако образование даже нескольких таких связей, действующих кооперативно, представляет собой стабилизирующий фактор. Важное биологическое значение водородных связей определяется их участием в строении живой материи.
Гидрофобные взаимодействия. Соединения, несущие заряды, а также способные к образованию водородных связей, являются полярными, или гидрофильными. Вследствие того, что электроотрицательный заряд углерода близок к водороду, углерод не способен к образованию водородных связей. Связи С-Н непо-лярны, поэтому углеводородные цепи гидрофобны. Молекулы воды, стремясь образовать между собой водородные связи, выталкивают гидрофобные группы и молекулы, заставляя их преобразовываться в ассоциаты. Этот процесс идет самопроизвольно. Гидрофобные ассоциаты имеют первостепенное значение для «архитектуры» биомембран, нуклеиновых кислот и белков. В белках гидрофобные взаимодействия возникают вследствие стремления неполярных гидрофобных боковых цепей ряда аминокислот (Вал, Ала, Лей, Иле, Фен, Тир, Три) избегать контакта с водой. Полипептидная цепь при этом сворачивается как бы в клубок, внутри которого сближаются гидрофобные группировки, а на поверхности располагаются полярные группы, взаимодействующие с водой.
... продолжение- Информатика
- Банковское дело
- Оценка бизнеса
- Бухгалтерское дело
- Валеология
- География
- Геология, Геофизика, Геодезия
- Религия
- Общая история
- Журналистика
- Таможенное дело
- История Казахстана
- Финансы
- Законодательство и Право, Криминалистика
- Маркетинг
- Культурология
- Медицина
- Менеджмент
- Нефть, Газ
- Искуство, музыка
- Педагогика
- Психология
- Страхование
- Налоги
- Политология
- Сертификация, стандартизация
- Социология, Демография
- Статистика
- Туризм
- Физика
- Философия
- Химия
- Делопроизводсто
- Экология, Охрана природы, Природопользование
- Экономика
- Литература
- Биология
- Мясо, молочно, вино-водочные продукты
- Земельный кадастр, Недвижимость
- Математика, Геометрия
- Государственное управление
- Архивное дело
- Полиграфия
- Горное дело
- Языковедение, Филология
- Исторические личности
- Автоматизация, Техника
- Экономическая география
- Международные отношения
- ОБЖ (Основы безопасности жизнедеятельности), Защита труда


