Программа по химии для абитуриентов: атомно-молекулярная теория, неорганическая и органическая химия, основы практической и промышленной химии


Программа по химии для абитуриентов
- Предмет химии. Явления химические и физические.
- Атомно-молекулярное учение. Атомы. Молекулы. Молекулярное и немолекулярное строение вещества. Относительная атомная и молекулярная масса. Закон сохранения массы, его значение в химии. Моль - единица количества вещества. Молярная масса. Закон Авогадро и молярный объем газа. Относительная плотность вещества.
- Химический элемент. Простые и сложные вещества. Химические формулы.
- Валентность. Составление химических формул по валентности.
- Строение атома. Состав атомных ядер. Физический смысл порядкового номера химического элемента. Изотопы. Явление радиоактивности. Электронное строение атома. Понятие об электронном облаке. Атомная электронная орбиталь. Энергетический уровень и подуровень. S-, p-, d-орбитали в атоме. Строение электронных оболочек атомов на примере элементов 1-го, 2-го, 3-го периодов периодической системы.
- Периодический закон и периодическая система химических элементов Д. И. Менделеева на основе учения о строении атомов. Структура периодической системы. Изменение свойств химических элементов и их соединений по группах и периодах периодической системы.
- Природа и типы химической связи. Образование ковалентной связи на примере молекул водорода, хлороводорода и аммиака. Полярная и неполярная ковалентные связи. Донорно-акцепторный механизм образования ковалентной связи на примере иона аммония. Ионная связь. Водородная связь. Примеры химических соединений с разными видами связи.
- Классификация химических реакций по различным оценкам. Типы химических реакций: соединения, разложения, замещения, обмена. Тепловой эффект химической реакции. Термохимические уравнения.
- Окислительно-восстановительные процессы. Степень окисления элемента. Окисление и восстановление как процессы присоединения и отдачи электронов. Практическое использование окислительно-восстановительных процессов.
- Представление о скорости химических реакций. Зависимость скорости от природы и концентрации реагирующих веществ, температуры. Катализ и катализаторы.
- Обратимость химических реакций. Химическое равновесие и условия, которые влияют на смещение химического равновесия.
- Растворы. Растворимость веществ. Зависимость растворимости от их природы, температуры и давления. Массовая доля растворенного вещества в растворе.
- Электролиты и неэлектролиты. Электролитическая диссоциация. Сильные и слабые электролиты. Химические свойства кислот, оснований и солей в свете теории электролитической диссоциации. Реакции ионного обмена и условия их необратимости.
- Оксиды. Классификация оксидов. Способы получения и свойства оксидов. Понятие об амфотерности.
- Основания. Щелочи и нерастворимые основания. Способы получения и химические свойства.
- Кислоты. Классификация кислот. Способы получения и общие химические свойства.
- Соли. Состав солей и их названия. Получение и химические свойства солей. Гидролиз солей.
- Взаимосвязь между различными классами неорганических соединений.
- Металлы, их размещение в периодической системе. Физические и химические свойства. Основные способы промышленного получения металлов. Электрохимические способы получения металлов. Электрохимический ряд напряжений металлов. Понятие о коррозии на примере ржавления железа. Значение металлов в народном хозяйстве.
- Щелочные металлы, их характеристика на основе размещения в периодической системе и строении атомов. Соединения натрия и калия в природе, их использование. Калийные удобрения.
- Общая характеристика элементов главной подгруппы второй группы периодической системы. Кальций, его соединения в природе. Жесткость воды и способы ее устранения.
- Алюминий, характеристика элемента и его соединений на основе размещения в периодической системе и строения атома. Физические и химические свойства алюминия. Амфотерность оксида и гидроксида алюминия.
- Металлы побочных подгрупп (хром, железо, медь) . Физические и химические свойства. Оксиды и гидроксиды. Соли хрома, железа и меди. Роль железа и его сплавов в технике.
- Водород, его химические и физические свойства. Получение водорода в лаборатории, его использование.
- Галогены, их характеристика на основе размещения в периодической системе и строении атомов. Хлор. Физические и химические свойства. Хлороводород. Соляная кислота и ее соли. Качественная реакция на хлорид-ион.
- Общая характеристика элементов главной подгруппы шестой группы периодической системы. Сера, ее физические и химические свойства. Сероводород и сульфиды. Оксиды серы. Серная кислота, ее свойства и химические основы производства контактным способом. Соли серной кислоты. Качественная реакция на сульфат-ион. Сульфаты в природе, промышленности и быту.
- Кислород, его физические и химические свойства. Аллотропия. Получение кислорода в лаборатории и промышленности. Роль кислорода в природе и использование его в технике.
- Вода. Электронное и пространственное строение молекулы воды. Физические и химические свойства воды. Вода в промышленности, сельском хозяйстве, быту.
- Общая характеристика элементов главной подгруппы пятой группы периодической системы. Фосфор. Оксид фосфора, фосфорная кислота и ее соли. Фосфорные удобрения.
- Азот, его физические и химические свойства. Аммиак. Физические и химические свойства. Химические основы промышленного синтеза аммиака. Соли аммония. Азотная кислота. Химические особенности азотной кислоты. Соли азотной кислоты. Азотные удобрения.
- Общая характеристика элементов главной подгруппы четвертой группы периодической системы. Кремний, его физические и химические свойства. Оксид кремния и кремниевая кислота. Соединения кремния в природе.
- Углерод, его аллотропные формы. Химические свойства углерода. Оксиды углерода, их химические свойства. Угольная кислота, карбонаты и гидрокарбонаты, их свойства. Превращения карбонатов и гидрокарбонатов. Качественная реакция на карбонат-ион.
- Теория химического строения органических веществ. Зависимость свойств органических веществ от химического строения. Изомерия. Электронная природа химической связи в молекулах органических соединений, типы разрыва связи, понятие о свободных радикалах.
- Гомологический ряд предельных углеводородов (алканов), их электронное и пространственное строение, sp³-гибридизация. Номенклатура алканов. Физические и химические свойства алканов (реакции галогенирования и окисления) . Представления о механизме цепных реакций с участием свободных радикалов. Метан, его использование.
- Этиленовые углеводороды (алкены) ; σ- и π-связи, sp²-гибридизация. Пространственная (геометрическая) изомерия. Номенклатура этиленовых углеводородов. Химические свойства (реакции присоединения водорода, галогенов, галогеноводородов, воды; реакции окисления и полимеризации) . Правило Марковникова. Получение и использование этиленовых углеводородов.
- Общие понятия химии высокомолекулярных соединений (мономер, полимер, структурное звено, степень полимеризации) . Полиэтилен. Полихлорвинил. Отношение полимеров к нагреванию, действию растворов кислот и щелочей. Использование полимеров.
- Диеновые углеводороды, их строение, химические свойства и использование. Природный каучук, его строение и свойства. Синтетический каучук.
- Ацетилен. Строение тройной связи (sp-гибридизация) . Получение ацетилена карбидным способом и из метана. Химические свойства (реакции присоединения) . Использование ацетилена.
- Главные представители ароматических углеводородов. Бензол. Электронное строение бензола и его химические свойства (реакции замещения и присоединения) . Получение бензола в лаборатории и промышленности, его использование.
- Углеводороды в природе: нефть, природный и попутные газы. Переработка нефти: перегонка и крекинг. Использование нефтепродуктов в химической промышленности для получения различных веществ.
- Предельные одноатомные спирты. Строение и номенклатура. Химические свойства одноатомных спиртов (реакции замещения, дегидратации и окисления) . Промышленные и лабораторные способы синтеза этанола, его использование.
- Многоатомные спирты: этиленгликоль и глицерин, их использование.
- Фенол, его строение. Сравнение химических свойств фенола со свойствами предельных одноатомных спиртов. Кислотные свойства фенола. Влияние гидроксильной группы на реакции замещения в ароматическом ядре. Получение и применения фенола.
- Альдегиды, их строение, номенклатура, химические свойства (реакции окисления и восстановления) . Получение и использование муравьиного и уксусного альдегидов. Фенолформальдегидные смолы.
- Карбоновые кислоты. Строение карбоксильной группы. Химические свойства карбоновых кислот. Муравьиная кислота, ее восстановительные способности. Уксусная и стеариновая кислоты, их применение. Олеиновая кислота как представитель непредельных карбоновых кислот. Мыла как соли высших карбоновых кислот.
- Сложные эфиры, их номенклатура. Получение сложных эфиров и их гидролиз. Применения сложных эфиров. Синтетические волокна на основе сложных эфиров.
- Жиры как представители сложных эфиров, их роль в природе и свойства. Химическая переработка жиров.
- Углеводы, их классификация. Моносахариды. Глюкоза, ее строение, химические свойства (реакция окисления и восстановления) . Роль в природе. Сахароза, ее гидролиз.
- Полисахариды как природные полимеры. Крахмал и целлюлоза, их строение, химические свойства. Углеводы как источник сырья для химической промышленности. Искусственные волокна на основе целлюлозы.
- Амины, их строение и номенклатура. Амины как органические основания, взаимодейст-вие с кислотами. Анилин. Сравнение свойств алкил- и арилзамещенных аминов. Получение анилина из нитробензола (реакция Зинина) .
- Аминокислоты, их строение и кислотно-основные свойства. Синтетические полиамидные волокна.
- Понятие о строении белковых молекул. α-аминокислоты как структурные единицы белков. Свойства и биологическая роль белков.
- Взаимосвязь между классами органических соединений.
Предмет химии. Явления химические и физические.
Химия - это наука о веществах и их превращениях. Она изучает состав и строение веществ, зависимость их свойств от строения, условия и способы превращения одних веществ в другие.
Химия имеет большое практическое значение. Много тысячелетий тому назад человек использовал химические явления при выплавке металлов из руд, получении сплавов, варке стекла и т. д. Ещё в 1751г. М. В. Ломоносов в своём знаменитом «Слове о пользе химии» писал: «Широко распростирает химия руки свои в дела человеческие. Куда ни посмотрим, куда не оглянёмся - везде обращаются перед очами нашими успехи её применения. »
В наше время роль химии в жизни общества неизмерима. Химические знания сейчас достигли такого уровня развития, что на их основе коренным образом меняются представления о природе и механизме ряда важнейших естественных и технологических процессов. Химия помогла нам открыть и использовать не только ранее неизвестные свойства веществ и материалов, но и создать новые, не существующие в природе вещества и материалы.
Вещество - это вид материи, обладающей при определённых условиях постоянными физическими свойствами. Однако с изменением условий свойства вещества изменяются.
Всякие изменения, происходящие с веществом, называются явлениями. Явления бывают как физические, так и химические.
Физическими называются такие явления, которые приводят к изменению формы, агрегатного состояния, температуры вещества, не изменяя его состава. Химический состав вещества в результате физического явления не изменяется. Например, воду можно превратить в лёд, в пар, но её химический состав при этом остаётся прежним.
Химическими называются такие явления, при которых происходит коренное изменение состава и свойств веществ. В результате химических явлений происходит превращение одних веществ в другие, т. е. изменяется состав молекул, образуются молекулы другого вещества. Однако атомы при химических реакциях остаются неизменными. Примером может служить разложение известняка:
CaCO3 → CaO + CO2
Химические явления иначе называют химическими реакциями. Характерные признаки химических явлений (реакций) : выделение тепла, газа, выпадение осадка, изменение цвета, появление запаха. При физических явлениях этого наблюдать нельзя.
Атомно-молекулярное учение. Атомы. Молекулы. Молекулярное и немолекулярное строение вещества. Относительная атомная и молекулярная масса. Закон сохранения массы, его значение в химии. Моль - единица количества вещества. Молярная масса. Закон Авогадро и молярный объем газа. Относительная плотность вещества.
Теоретическую основу современной химии составляет атомно-молекулярное учение.
Атомы - мельчайшие химические частицы, являющиеся пределом химического разложения любого вещества.
Химический элемент представляет собой вид атомов с одинаковым положительным зарядом ядра.
Следовательно, атом - это наименьшая частица химического элемента, сохраняющая все его химические свойства. В настоящее время известно 110 элементов, из которых 92 встречаются в природе.
В зависимости от природы частиц, из которых построено вещество, различают вещества с молекулярной и немолекулярной структурой. Практически все органические вещества (т. е. подавляющее большинство известных веществ) состоят из молекул. Среди неорганических соединений молекулярное строение имеют примерно 5%. Таким образом, наиболее типичной формой существования вещества является молекула.
Молекула - наименьшая частица вещества, способная существовать самостоятельно и сохраняющая его основные химические свойства.
При обычных условиях вещества с молекулярной структурой могут находиться в твердом, жидком или газообразном состоянии. Вещества с немолекулярной структурой находятся только в твердом состоянии, преимущественно в кристаллической форме. Носителями химических свойств таких веществ являются не молекулы, а комбинации атомов или ионов которые образуют данное вещество.
Символическая запись простейшего численного соотношения, в котором атомы различных элементов образуют химическое соединение, называется формулой. Следовательно, формула выражает определенный (качественный и количественный) состав соединения. Так, SO2, N2, CO - формулы веществ, имеющих молекулярное строение. Их состав всегда строго постоянен. NaCl, AlF3, ZnS- формулы веществ, не имеющих молекулярное строение при обычных условиях. Состав таких веществ не всегда постоянен и часто зависит от условия их получения. Отклонение от целочисленного соотношения могут быть выражены при записи формулы: Fe0, 9S, TiO0, 7, ZrN0, 69. Вещества с постоянным составом называются дальтонидами, вещества с переменным составом - бертоллидами.
Массы атомов химических элементов чрезвычайно малы. В химии пользуются не их абсолютными значениями, а относительными.
Относительной атомной массой химического Ar элемента называется величина, равная отношению средней массы атомов данного элемента (с учетом процентного содержания его изотопов в природе ) к 1\12 массы изотопов углерода - 12. 1\12 массы атома изотопа углерода 12 принята за атомную единицу массы (а. е. м. ), международное обозначение - u.
Относительная атомная масса является величиной безразмерной.
Относительной молекулярной массой Mr вещества называется отношение массы его молекулы к 1\12 массы атома изотопа углерода 12.
Поскольку большинство неорганических веществ при обычных условиях не имеют молекулярного строения, в данном случае можно говорить о формульной массе F, понимая под ней сумму атомных масс всех элементов, входящих в соединение, с учетом числа атомов каждого элемента в формуле.
Единицей измерения количества вещества n (ν) в Международной системе единиц является моль .
Моль - количество вещества, содержащее столько структурных элементарных единиц (атомов, ионов, молекул, электронов, эквивалентов и т. д. ), сколько содержится атомов в 0, 012 кг изотопа углерода 12.
Число атомов NA в 0, 012 кг углерода (т. е. в 1моль) легко определить, зная массу атома углерода. Точное значение этой величины - 6, 02·10²³ . Эта величина называется постоянной Авогадро и является одной из важнейших универсальных постоянных. Она равна числу структурных единиц в 1 моль любого вещества.
Масса 1 моль вещества Х называется молярной массой М(Х) и представляет собой отношение массы m этого вещества к его количеству n.
Закон сохранения массы: «Масса веществ, вступивших в химическую реакцию, равна массе веществ, образовавшихся в результате реакции, с учетом массы, соответствующей тепловому эффекту реакции». Он был сформулирован великим русским ученым М. В. Ломоносовым в 1748г. и подтвержден экспериментально им самим в 1756г. и независимо от него французским химиком А. Л. Лавуазье в 1789г.
Закон постоянства состава вещества: «Любое сложное вещество молекулярного строения независимо от способа получения имеет постоянный количественный состав».
Закон Авогадро: «В равных объемах различных газов при одинаковых условиях содержится одно и то же количество молекул».
Следствия: 1. Если число молекул некоторых газов равно, то при н. у. они занимают равные объемы. Если же число молекул равно 6, 02·10²³, то объем газа равен 22, 4 л. Этот объем называется молярным объемом.
- Абсолютная плотность газа равна отношению его молекулярной массы к молярному объему
- Относительная плотность газа (Х) по другому газу (Y) равна отношению молярной массы газа (Х) к молярной массе газа (Y) .
Уравнение Клаперона:
 Уравнение Менделеева-Клаперона:
Уравнение Менделеева-Клаперона:
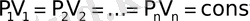 Уравнение Бойля-Мариотта:
Уравнение Бойля-Мариотта:
Уравнение Шарля-Гей-Люсака:
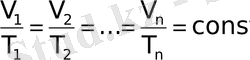
Химический элемент. Простые и сложные вещества. Химические формулы.
Вид атомов с одинаковыми химическими свойствами называется элементом. Атомы одного и того же элемента могут отличаться только массой. Химические свойства у них одинаковы. Существуют разновидности атомов одного и того же элемента, называемые изотопами .
Понятие «химический элемент» в равной мере относится к атомам данного элемента как находящимся в свободном виде, так и входящим в состав соединений.
Молекулы образуются из атомов. В зависимости от того, состоит ли молекула из атомов и того же элемента или из атомов различных элементов, все вещества делятся на простые и сложные.
Простыми веществами называются такие, молекулы которых состоят из атомов одного элемента. Молекулы простых веществ могут состоять из одного, двух и большего числа атомов одного элемента. В настоящее время является неоспоримым факт существования одного и того же элемента в свободном состоянии в виде ряда различных форм, т. е. в виде нескольких простых веществ.
Существование элемента в виде нескольких простых веществ называется аллотропией. Простые вещества, образованные одним и тем же элементом, называются аллотропическими видоизменениями этого элемента. Эти видоизменения отличаются как числом, так и расположением одних и тех же атомов в молекуле.
Сложными веществами или химическими соединениями называются такие, молекулы которых состоят из атомов двух или более элементов. Атомы, вступившие в химическое соединение, не остаются неизменными. Они оказывают друг на друга взаимное влияние. В различных молекулах атомы находятся в различных состояниях.
Химическая формула - это изображение состава вещества посредством химических знаков. Химические формулы обозначают молекулу вещества, ее качественный и количественный состав.
Валентность. Составление химических формул по валентности.
Важным понятием химии является валентность . Валентность - способность атома соединяться с другими атомами определенным числом химических связей. Числовое значение валентности определяется общим числом атомных орбиталей, участвующих в образовании химической связи:
СО: С≡О С: 1s 2 2s 2 2p 2 валентность:3
O: 1s 2 2s 2 2p 4
Все сказанное относится к соединениям с ковалентной связью. Если элемент образует ионные связи, то его валентность называется стехиометрической. Она ничего не говорит о числе связей. Высшая валентность равна номеру группы, в которой находится элемент, однако N, O и F имеют высшую валентность - 4. Это объясняется тем, что атомы этих элементов не могут переходить в возбужденное состояние из-за отсутствия вакантных орбиталей на ВЭУ.
Строение атома. Состав атомных ядер. Физический смысл порядкового номера химического элемента. Изотопы. Явление радиоактивности. Электронное строение атома. Понятие об электронном облаке. Атомная электронная орбиталь. Энергетический уровень и подуровень. S -, p -, d -орбитали в атоме. Строение электронных оболочек атомов на примере элементов 1-го, 2-го, 3-го периодов периодической системы.
... продолжение- Информатика
- Банковское дело
- Оценка бизнеса
- Бухгалтерское дело
- Валеология
- География
- Геология, Геофизика, Геодезия
- Религия
- Общая история
- Журналистика
- Таможенное дело
- История Казахстана
- Финансы
- Законодательство и Право, Криминалистика
- Маркетинг
- Культурология
- Медицина
- Менеджмент
- Нефть, Газ
- Искуство, музыка
- Педагогика
- Психология
- Страхование
- Налоги
- Политология
- Сертификация, стандартизация
- Социология, Демография
- Статистика
- Туризм
- Физика
- Философия
- Химия
- Делопроизводсто
- Экология, Охрана природы, Природопользование
- Экономика
- Литература
- Биология
- Мясо, молочно, вино-водочные продукты
- Земельный кадастр, Недвижимость
- Математика, Геометрия
- Государственное управление
- Архивное дело
- Полиграфия
- Горное дело
- Языковедение, Филология
- Исторические личности
- Автоматизация, Техника
- Экономическая география
- Международные отношения
- ОБЖ (Основы безопасности жизнедеятельности), Защита труда


