Битабарова Х.И. құрастырған стехиометрия және органикалық химия есептері мен шешімдері


 Онтүстік Қазақстан облысы.
Онтүстік Қазақстан облысы.
Мақтарал ауданы.
«Көктөбе» ауылы.
№ 19 М. Мақатаев атындағы жапы орта мектебі коммуналдық мемлекеттік мекемесінің
химия пәнінің мұғалімі
Битабарова Хадиша Исабековна.
1. 0, 5 моль метаннан трихлорметан түзілу үшін қажет хлордың көлемі ( қ. ж., лиртмен)
А) 33, 4
В) 33, 2
С) 33, 3
D) 33, 5.
Е) 33, 6
Шешуі: СН 4 + 3СІ 2 → CНСІ 3 + 3НСІ
V m = 22, 4 л/моль
V (СІ 2 ) = ν · V m = 3 моль · 22, 4 л/моль = 67, 2 л
0, 5 моль CН 4 х л СІ 2
1 моль CН 4 67, 2 л СІ 2
{дұрыс жауабы} = Е
2. Құрамында 80% көміртек, 20% сутек бар органикалық заттың сутек бойынша тығыздығы 15. Осы заттың формуласы.
А) СН 4
В) С 2 Н 6
С) С 3 Н 8
D) С 4 Н 10
Е) С 5 Н 10
Шешуі: М (C) = 12 г/моль
m (C) = ν · М (C) = 1 моль · 12 г/моль = 12 г
М (Н) = 1 г/моль
m (Н) = ν · М (Н) = 1 моль · 1 г/моль = 1 г
Mr (C x H у ) = Mr (H 2 ) ∙ D(H₂) = 2 · 15 = 30
M (C 2 H 6 ) = 12 ∙ 2 + 1∙ 6 = 30 г/моль
{дұрыс жауабы} = В
3. Ауамен салыстырғандағы тығыздығы 2-ге тең құрамындағы көміртектің массалық үлесі 82, 8%, сутектікі -17, 2% болатын көмірсутектің молекулалық формуласы
А) С 4 Н 8
В) С 3 Н 8
С) С 5 Н 10
D) С 3 Н 6
Е) С 4 Н 10
Шешуі: М (C) = 12 г/моль
m (C) = ν · М (C) = 1 моль · 12 г/моль = 12 г
М (Н) = 1 г/моль
m (Н) = ν · М (Н) = 1 моль · 1 г/моль = 1 г
Mr (C x H у ) = Mr (ауа) ∙ D(ауа) = 2 · 29 = 58 г/моль
M (C 4 H 10 ) = 12∙ 4 + 1∙10 = 58 г/моль
{дұрыс жауабы} = Е
4. 5 литр метан мен 11 литр оттек қоспасы қопарылғанда түзілетін көміртек диоксидінің
көлемі (қ. ж. )
А) 5 л
В) 5, 5 л
С) 5, 8 л
D) 5, 6 л
Е) 5, 4 л
Шешуі: CН 4 + 2О 2 → СО 2 + 2Н 2 О
V m = 22, 4 л/моль
V (CН 4 ) = ν · V m = 1 моль · 22, 4 л/моль
V (СО 2 ) = ν · V m = 1 моль · 22, 4 л/моль
V (О 2 ) = ν · V m = 2 моль · 44, 8 л/моль
ν (CН 4 ) < ν (СО 2 )
V (СО 2 ) = ν · V m = 1 моль · 22, 4 л/моль
х л СО 2 5 л CН 4
22, 4 л СО 2 22, 4 л CН 4
{дұрыс жауабы} = А
5. 120 мл этил спирті (p =0, 8 г/см 3 ) түзілу үшін қажет этиленнің массасы (г)
А) 29, 5
В) 34, 2
С) 45, 3
D) 58, 4
Е) 65, 8
Шешуі: C 2 Н 4 + Н 2 О → C 2 Н 5 ОН
М (C 2 Н 5 ОН) = 46г/моль
m (C 2 Н 5 ОН) = ν · М (C 2 Н 5 ОН) = 1 моль · 56 г/моль = 56 г
М(C 2 Н 4 ) = 28г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
m (C 2 Н 5 ОН) = 0, 8г/см 3 ∙ 120мл= 96г
хг C 2 Н 4 96г C 2 Н 5 ОН
28г C 2 Н 4 46гC 2 Н 5 ОН
{дұрыс жауабы} = D
6. Этанның жану реакциясының термохимиялық теңдеуі 2С 2 Н 6 + 7О 2 → 4СО 2 + 6Н 2 О+ 3080кДж . Реакция нәтижесінде 770кДж жылу бөлінсе, жұмсалған (қ. ж. ) оттегінің көлемі (л)
А) 39, 6
В) 39, 2
С) 44, 8
D) 22, 4
Е) 33, 6
Шешуі: 2С 2 Н 6 + 7О 2 → 4СО 2 + 6Н 2 О+ 3080кДж
7V(О 2 ) = 156, 8л/моль
V (Н 2 ) = ν · V m = 1 моль · 22, 4 л/моль
3080кДж 156, 8л О 2
770 кДж хл О 2
{дұрыс жауабы} = В
7. Массасы 30, 8 грамм пропан жанғанда түзілетін судың массасы (грамм)
А) 45, 4
В) 46, 4
С) 47, 4
D) 48, 4
Е) 50, 4
Шешуі: 2С 3 Н 8 + 10О 2 → 6СО 2 + 8Н 2 О
2М (С 3 Н 8 ) = 88г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
8М(H 2 O) = 144г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
хг H 2 O 30, 8г С 3 Н 8
144г H 2 O 88г С 3 Н 8
{дұрыс жауабы} = Е
8. Массасы 9, 9г дихлорэтан алу үшін хлорсутекпен әрекеттесетін ацетиленнің (қ. ж. ) көлемі
А) 5, 60л
В) 4, 48л
С) 1, 12л
D) 22, 40л
Е) 2, 24л
Шешуі: С 2 Н 2 + НСІ → С 2 Н 3 СI
С 2 Н 3 СI + НСІ → С 2 Н 4 СI 2
V(С 2 Н 2 ) = 22, 4л/моль
V (Н 2 ) = ν · V m = 1 моль · 22, 4 л/моль
М(С 2 Н 4 СI 2 ) = 99г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
9, 9г С 2 Н 4 СI 2 хл С 2 Н 2
99г С 2 Н 4 СI 2 22, 4л С 2 Н 2
{дұрыс жауабы} = Е
9. Егер жағуға 89, 6л оттек жұмсалған болса (қ. ж. ) жанған ацетиленнің көлемі (л)
А) 11, 8
В) 12, 5
С) 13, 2
D) 28, 3
Е) 35, 8
Шешуі: 2C 2 Н 2 + 5О 2 → 4СО 2 + 2Н 2 О
V(C 2 Н 2 ) = 44, 8л/моль
V (Н 2 ) = ν · V m = 1 моль · 22, 4 л/моль
V(О 2 ) = 112л/моль
V (Н 2 ) = ν · V m = 1 моль · 22, 4 л/моль
89, 6л О 2 хл C 2 Н 2
112л О 2 44, 8лC 2 Н 2
{дұрыс жауабы} = Е
10. 48м 3 метаннан алынатын ацетиленнің көлемі (л)
А) 12
В) 18
С) 24
D) 36
Е) 42
Шешуі: 2CН 4 → С 2 Н 2 + 2Н 2
V(C 2 Н 2 ) = 22, 4л/моль
V (Н 2 ) = ν · V m = 1 моль · 22, 4 л/моль
2V(CН 4 ) = 44, 8л/моль
V (Н 2 ) = ν · V m = 1 моль · 22, 4 л/моль
48м 3 = 4800л
4800л CН 4 хл C 2 Н 2
44, 8л CН 4 22, 4лC 2 Н 2
{дұрыс жауабы} = С
11. 140г пропинді (қ. ж. ) толық гидрлеу үшін сутектің көлемі қажет (л)
А) 156, 8
В) 165, 8
С) 171, 5
D) 187, 1
Е) 192, 4
Шешуі: С 3 Н 4 + 2Н 2 → С 3 Н 8
V(Н 2 ) = 44, 8л/моль
V (Н 2 ) = ν · V m = 1 моль · 22, 4 л/моль
М(С 3 Н 4 ) = 40г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
140г С 3 Н 4 хл Н 2
40г С 3 Н 4 44, 8л Н 2
{дұрыс жауабы} = А
12. Егер жағуға 78, 4 л оттек жұмсалған болса (қ. ж. ), жанған пентадиеннің массасы (г)
А) 34, 0
В) 33, 0
С) 44, 0
D) 67, 0
Е) 89, 0
Шешуі: C 5 Н 8 + 7О 2 → 5СО 2 + 4Н 2 О
М(C 5 Н 8 ) = 68г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
V(О 2 ) = 156, 8л/моль
V (Н 2 ) = ν · V m = 1 моль · 22, 4 л/моль
78, 4л О 2 хг C 5 Н 8
156, 8л О 2 68гC 5 Н 8
{дұрыс жауабы} = А
13. 336г циклогександы дегидрлеу нәтижесінде алынған бензолдың массасы (г)
А) 154
В) 225
С) 312
D) 416
Е) 523
Шешуі: C 6 H 12 → C 6 H 6 + 3Н 2
М (C 6 H 6 ) =78г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
М(C 6 H 12 ) = 84г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
хг C 6 H 6 336г C 6 H 12
78г C 6 H 6 84г C 6 H 12
{дұрыс жауабы} = С
14. 156 г бензол алу үшін қажет ацетиленнің көлемі (л)
А) 105, 3
В) 119, 2
С) 122, 5
D) 134, 4
Е) 153, 7
Шешуі: 3C 2 H 2 → C 6 H 6
М (C 6 H 6 ) =78г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
V(C 2 H 2 ) = 67, 2л/моль
V (Н 2 ) = ν · V m = 1 моль · 22, 4 л/моль
156г C 6 H 6 хл C 2 H 2
78г C 6 H 6 67, 2л C 2 H 2
{дұрыс жауабы} = D
15. 138 г толуол азот қышқылымен әрекеттескенде түзілетін 2, 4, 6- тринитротолуолдың массасы (г)
А) 340, 5
В) 353, 2
С) 374, 3
D) 452, 7
Е) 462, 8
Шешуі:
C
6
H
5
-CH
3
+ 3HNO
3
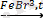 → C
6
H
2
(NO
2
)
3
-CH
3
+ 3H
2
O
→ C
6
H
2
(NO
2
)
3
-CH
3
+ 3H
2
O
М(C 6 H 5 -CH 3 ) = 92г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
М(C 6 H 2 (NO 2 ) 3 -CH 3 ) = 227г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
хгC 6 H 2 (NO 2 ) 3 -CH 3 138г C 6 H 5 -CH 3
227г C 6 H 2 (NO 2 ) 3 -CH 3 92г C 6 H 5 -CH 3
{дұрыс жауабы} = А
16. 3, 9 г көмірсутек жанған кезде 13, 2 г көміртегі (ІV) оксиді және 2, 7 г су буы түзіледі. Осы заттың сутек бойынша тығыздығы 39-ға тең болса, белгісіз заттың формуласы
А) С 2 Н 2
В) С 6 Н 6
С) С 8 Н 10
D) С 7 Н 8
Е) С 9 Н 12
Шешуі: C х Н у + О 2 → СО 2 + Н 2 О
М(CО 2 ) = 44г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
М(H 2 О) = 18г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
СО 2 → С
44г СО 2 12г С
13, 2г СО 2 х г С
Н 2 О → Н 2
18г Н 2 О 2г Н 2
2, 7г Н 2 О у г Н 2
m(СH) =m(C) + m(C) = 3, 6 г + 0, 3 г = 3, 9г
Mr(C x H у ) = Mr(H 2 ) ∙ D(H₂) = 2 · 39 = 78
M(C 6 H 6 ) = 12∙ 26+ 1∙6 = 78г/моль
{дұрыс жауабы} = В
17. 31, 2 г бензол 32 л хлормен (қ. ж. ) әрекеттескенде түзілген массасы (г)
А) 116, 4
В) 124, 1
С) 132, 5
D) 147, 3
Е) 153, 2
Шешуі: C 6 H 6 + 3СІ 2 →C 6 H 6 СІ 6
М(C 6 H 6 ) = 78г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
М(C 6 H 6 СІ 6 ) = 291 г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
V(СІ 2 ) = 67, 2л/моль
V (Н 2 ) = ν · V m = 1 моль · 22, 4 л/моль
хг C 6 H 6 СІ 6 31, 2г C 6 H 6
291г C 6 H 6 СІ 6 78гC 6 H 6
{дұрыс жауабы} = А
18. 11, 2 л ацетиленен (қ. ж. ) 10 мл бензол (p = 0, 88г/мл) алында. Түзілген бензолдың теориялық шығыммен салыстырғандағы шығымы (%)
А) 35, 7
В) 46, 7
С) 67, 7
D) 64, 7
Е) 72, 7
Шешуі: 3C 2 H 2 → C 6 H 6
М(C 6 H 6 ) = 78г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
V(C 2 H 2 ) = 22, 4л/моль
V (Н 2 ) = ν · V m = 1 моль · 22, 4 л/моль
M(C 6 H 6 ) = 0, 88 ∙ 10 = 8, 8г
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
х моль C 6 H 6 0, 5 моль C 2 H 2
1 моль C 6 H 6 3 мольC 2 H 2
m теор. = 0, 167 моль · 78 г = 13 г
m(C 6 H 6 ) = 0, 88 ∙ 10 = 8, 8г
{дұрыс жауабы} = С
19. 19, 5 г бензолды темір (ІІІ) хлоридінің қатысында бромдау нәтижесінде 31, 4 г бромбензол алынды. Түзілген бромбензолдың практикалық шығымы (%)
А) 80
В) 82
С) 85
D) 87
Е) 89
Шешуі: C 6 H 6 + Br 2 →C 6 H 5 Br + HBr
М(C 6 H 6 ) = 78г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
М(C 6 H 5 Br) = 157г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
19, 5г C 6 H 6 хг C 6 H 5 Br
78г C 6 H 6 157г C 6 H 5 Br
{дұрыс жауабы} = А
20. 52 г формальдегид 100 г суда ерітілді. Алынған формалинның массалық үлесі(%)
А) 31, 2
В) 32, 2
С) 33, 2
D) 34, 2
Е) 35, 2
Шешуі: m ерітінді = m(НСОН) + m(Н 2 О) = 52г + 100г = 152г
{дұрыс жауабы} = D
21. Массасы 8, 8 г ацетальдегидті сутекпен тотықсыздандырғанда түзілетін өнімнің мөлшері ( моль)
А) 0, 1
В) 0, 3
С) 0, 5
D) 0, 4
Е) 0, 2
Шешуі: CН 3 -СОН+ Н 2 → CН 3 - СН 2 ОН
М(CН 3 -СОН) = 44г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
v (CН 3 - СН 2 ОН) = 1моль
хмоль CН 3 - СН 2 ОН 8, 8г CН 3 -СОН
1 моль CН 3 - СН 2 ОН 44гCН 3 -СОН
{дұрыс жауабы} = Е
22. 29 г пропанальді күміс (І) оксидінің аммиактағы ерітіндісімен тотықтырғанда түзілетін күмістің массасы (г)
А) 108
В) 106
С) 107
D) 112
Е) 110
Шешуі: CН 3 - CН 2 СОН+ Аg 2 O CН 3 - CН 2 СООН + 2Ag↓
М(CН 3 - CН 2 СОН) = 58г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
2М(Ag) = 216г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
хг Ag 29г CН 3 - CН 2 СОН
216г Ag 58гCН 3 - CН 2 СОН
{дұрыс жауабы} = А
23. 2, 2 г сірке альдегиді күміс (І) оксидінің аммиактағы ерітіндісімен әрекеттескенде тұнбаға түскен күмістің массасы (г)
А) 8, 8
В) 9, 8
С) 12, 8
D) 11, 8
Е) 10, 8
Шешуі: CН 3 -СОН+ Аg 2 O CН 3 -СООН + 2Ag↓
М(CН 3 -СОН) = 44г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
2М(Ag) = 216г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
хг Ag 2, 2г CН 3 - CН 2 СОН
216г Ag 44гCН 3 - CН 2 СОН
{дұрыс жауабы} = Е
24. Реакция өнімінің шығымы 70 % болса, 330 г ацетальдегидтен алынатын сірке қышқылының массасы (г)
А) 450
В) 405
С) 360
D) 315
Е) 270
Шешуі: CН 3 -СОН+ Аg 2 O CН 3 - СООН + 2Ag↓
М(CН 3 -СОН) = 44г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
М(CН 3 -СООН) = 60г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
хг CН 3 -СООН 330г CН 3 -СОН
60г CН 3 -СООН 44гCН 3 -СОН
100% 450г
70% хг
{дұрыс жауабы} = D
25. Термохимиялық теңдеуі бойынша С 2 Н 4 + 3О 2 → 2СО 2 + 2Н 2 О+ 1400кДж
нәтижесінде 9100кДж жылу бөлінсе, жанған этиленнің массасы (г) :
А) 56
В) 112
С) 118
D) 182
Е) 195
Шешуі: С 2 Н 4 + 3О 2 → 2СО 2 + 2Н 2 О+ 1400кДж
М(С 2 Н 4 ) = 28г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
9100кДж хг С 2 Н 4
1400кДж 28г С 2 Н 4
{дұрыс жауабы} = D
26. 150 г ерітіндіде 33, 75 г құмырсқа қышқылының метил эфирі бар. Ерітіндідегі күрделі эфирдің массалық үлесі (%)
А) 22, 5
В) 22, 9
С) 23, 1
D) 22, 1
Е) 22, 3
Шешуі:
{дұрыс жауабы} = А
27. 240г суда 60гқұмырсқа қышқылының этил эфирін ерітті. Алынған ерітіндідегі күрделі эфирдің массалық үлесі (%)
А) 20
В) 25
С) 15
D) 30
Е) 23
Шешуі: m ерітінді = m( ) + m(Н 2 О) = 60г + 240г = 300г
{дұрыс жауабы} = А
28. Құрамында массалық үлесі 85 % тристеараты бар 1, 6 т майға натрий гидроксидімен әсер еткенде алынатын сабынның массасы (т)
А) 1, 5
В) 1, 7
С) 1, 9
D) 1, 6
Е) 1, 4
Шешуі: С 3 Н 5 (ОСОС 17 Н 35 ) 3 + 3NaОН → 3C 17 H 35 СООNa + С 3 Н 8 О 3
М(С 3 Н 5 (ОСОС 17 Н 35 ) 3 ) = 890т/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
3М(C 17 H 35 СООNa) = 918т/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
хт C 17 H 35 СООNa 1, 6т С 3 Н 5 (ОСОС 17 Н 35 ) 3
918тC 17 H 35 СООNa 890т С 3 Н 5 (ОСОС 17 Н 35 ) 3
100% 1, 65т
85% хт
{дұрыс жауабы} = Е
29. Егер глюкоза спирттік ашығанда 448 л (қ. ж. ) көмірқышқыл газы бөлінген болса, түзілген спирттің массасы (г)
А) 920
В) 925
С) 930
D) 935
Е) 940
Шешуі: C 6 Н 12 О 6 →2C 2 Н 5 ОН + 2СО 2
2М(C 2 Н 5 ОН) = 92г/моль
m (Ғе) = ν · М (Ғе) = 1 моль · 56 г/моль = 56 г
V(CО 2 ) = 44, 8л/моль
V (Н 2 ) = ν · V m = 1 моль · 22, 4 л/моль
хгC 2 Н 5 ОН 448лCО 2
92г C 2 Н 5 ОН 44, 8г CО 2
{дұрыс жауабы} = А
30. 0, 3 моль глюкоза спирттік ашығанда түзілетін этанолдың массасы (г)
А) 26, 6
В) 29, 6
С) 27, 6
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz