Молекулалардың өлшемдері мен массасы, молекула саны, зат мөлшері және молярлық масса


Сабақ жоспары
Сабақтың тақырыбы: Молекулалардың өлшемі мен массасы. Молекулалар саны. Зат мөлшері. Молярлық масса.
Сабақтың мақсаты:
1. Білімділік : Оқушыларға молекулалардың өлшемі мен массасы, зат мөлшері, молярлық масса, молекулалар саны туралы түсіндіру .
2. Дамытушылық : МКТ негіздерін оқып - үйренуде оқушылардың логикалық ойлау жүйесін дамыту, жүйелі түрде ойлауға, ізденуге бағыттау.
3. Тәрбиелік : Өмірдің барлық ағымы физикалық заңдылыққа қатысты екендігін көрсету. Оқушыларды еңбектене, іздене білуге тәрбиелеу.
Сабақтың түрі : аралас
Сабақтың әдісі: Түсіндірмелі баяндау, сұрақ-жауап.
Сабақтың көрнекілігі: интерактивті тақта, проектор, слайд
Пәнаралық, пәнішілік байланыс: физика 9 сынып
Сабақ барысы.
І. Ұйымдастыру кезеңі
ІІ. Үй тапсырмасын тексеру
ІІІ. Жаңа сабақты түсіндіру
IV. Жаңа сабақты бекіту
V. Үйге тапсырма беру
VI. Қорытындылау, бағалау
І Ұйымдастыру кезеңі .
а) оқушыларды түгендеу
ІІ. Үй тапсырмасын сұрау:
- Зат құрылысы туралы қандай түсініктер болды?
- Табиғаттағы барлық заттардың алуан түрлілігін ежелгі грек философтары қалай түсіндірді?
- МКТ негізгі қағидалары қалай айтылады?
- Молекула дегеніміз не?
- Атом деп нені атайды?
Семантикалық картаны толтыру
Молекула кинетикалық теорияның негіздеріне үлес қосқан ғалымдар:
Жаңа сабақ түсіндіру.
Молекулалардың негізгі сипаттамаларының бірі олардың өлшемі мен массасы болып табылады.
Молекулалар мен атомдардың өлшемдері өте кіші болғандыөтан оларды тек салыстыру жолымен ғана көрсетуге болады.
Молекулалар өлшемін бағалау үшін неміс физигі В Рентген мен ағылшын физигі Д Релей тәжірибе жүргізді.
Молекулалардың өлшемі өте кіші болғандықтан, олардың саны кез келген денеде өте көп болады.
Мысалы 1см
3
ауада қалыпты атмосфералық қысым мен 0
0
С температура кезінде 2, 7 *10
19
молекулалар болады. Массасы 1г су тамшысындағы молекулалардың жуық саны - 3, 7*10
22
.
сонда судың бір молекуласының массасы:
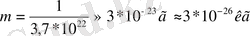 .
.
Макраскопиялық денелердегі молекулалар саны сияқты үлкен сандарды немесе молекула массасы сияқты өте аз сандарды тәжірибеде пайдалану ыңғайсыз. Сондықтан қолайлы болу үшін атомдардың саны мен массаларын көрсеткенде олардың салыстырмалы мәнін пайдадану қабылданған.
Халықаралық келісімге сай барлық молекулалардың массаларын көміртек атомы массасының 1/12 бөлігімен салыстырады.
Заттардың М r салыстырмалы массасы деп берілген заттың молекуласының m 0 массасының көміртек атомының m 0 C массасының 1/12 бөлігіне қатынасын айтады.
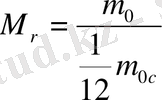
Барлық химиялық элементтердің атомдарының салыстырмалы массалары Д. И Менделеевтің периодтық кестесінде көрсетілген.
Егер зат атомдардан есем молекулалардан тұрса онда оның салыстырмалы молекулалық массасы молекуланы түзуші элементтердің салыстырмалы атомдық массаларының қосындысына тең. Мысалы, Н 2 О судың салыстырмалы молекулалық массасы мынаған тең: (1*2+16=18) .
Кейбір есептерді шешу үшін берілген денедегі барлық молекулалар мен атомдардың санын білу маңызды. Берілген денедегі барлық атомдар мен молекулалардың салыстырмалы саны зат мөлшері деп ататын физикалық шамамен сипатталады.
Заттың ν мөлшері деп берілген денедегі N молекулалар санының 12г көміртектегі N A атомдар санына қатынасын айтады:
ν=
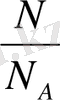
N A - Авагадро тұрақтысы. Оны 1811 жылы итальян физигі әрі химигі А. Авагадро анықтаған соның құрметіне осылай аталған.
N A = 6, 02*10 23 моль -1
Зат мөлшерінің бірлігіне 1 моль алынған.
Моль - 12г көміртекте қанша атом болса, сонша бөлшектері бар заттың мөлшері.
Салыстырмалы молекулалық массамен қатар физика мен химияда М молярлық масса ұғымы кеңінен пайдаданылады.
Молярлық масса деп 1 моль мөлшерінде алынған заттардың массасын айтады. Өлшем бірлігі 1 кг/моль.
M=m 0 N A
Заттардың молярлық массасы мен оның салыстырмалы молекулалық массасы өзара байланысты. Заттардың молярлық массасының граммен өрнектелген сандық мәні осы заттардың салыстырмалы молекулалық массасына тең.
Молекуланың массасын табу үшін
m
0
=
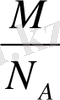
Зат мөлшері, зат массасы және молярлық масса арасында мынадай байланыс бар:
m=m 0 N= m 0 ν N A =νM
денедегі молекула санын зат массасы мен молярлық масса арқылы табуға болады:
N=N
A
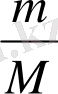
Жаңа сабақты бекіту
Физикалық диктант
- деп берілген заттың молекуласының m0массасының көміртек атомының m0 Cмассасының 1/12 бөлігіне қатынасын айтады.
- Берілген денедегі N молекулалар санының 12г көміртектегі NAатомдар санына қатынасын айтады.
- деп 1 моль мөлшерінде алынған заттардың массасын айтады.
- Авагадро тұрақтысы мынаған тең:
- Зат мөлшері, зат массасы және молярлық масса арасындағы байланыс
- 1 моль өлшем бірлігі.
Үйге тапсырма: §21 Молекулалардың өлшемі мен массасы. Молекулалар саны. Зат мөлшері. Молярлық масса. тақырыбы
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz