Химиялық байланыстардың негізгі түрлері: иондық, ковалентті (полюсті және полюссіз) және олардың теориялық негіздері


Тақырыбы Химиялық байланыстың негізгі түрлері
Мақсаты Саяхат сабағы арқылы, химиялық байланыс
түрлері тақырыбын терең ұғындыру
Міндеті 1. Өткен тақырыпты жаңа тақырыппен
байланыстыра ұғына білу
2 . саяхат кезінде алған жаңалықтарын пайдалана білу
Түрі саяхат сабағы
Әдісі түсіндіру, сұрақ-жауап
Барысы
Біз саяхатымызды ауа шарымен шығамыз, шарға ір айлақ өткен сайын алған жағалықтарды жапсырып отыру.
І айлақ «Күн»
Үй тапсырмасын тексеру «сұрақ-жауап» арқылы тексеру
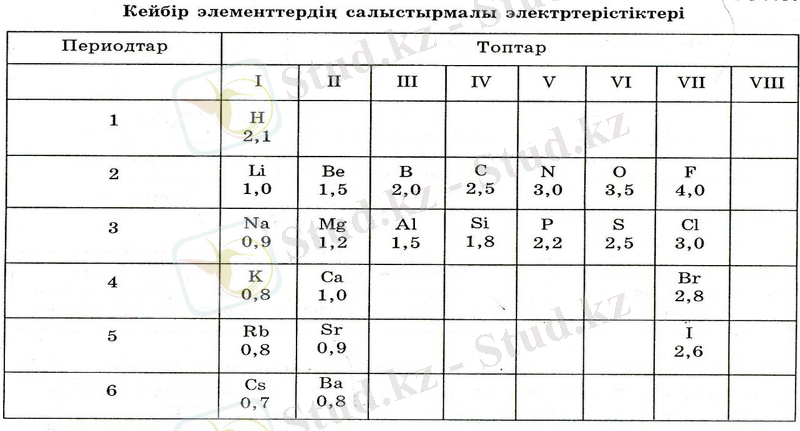
- Электіртерістілік дегеніміз не?
- Электіртерістілік топ, период бойынша қалай өзгереді?
- Электіртерістілік ең жоғарғы элемент, ең төменгі элемент?
Период бойынша элементтің атом ядроларыының зарядтары өскен сайын олардың сыртқы электрондық қабаттарын толтыру аяқтала бастайды. Осыған сай элементтердің бейметалдық қасиеттері күшейіп, олардың электртерістіліктері арта түседі. Бұдан электіртерістік элементтердің металдық және бейметалдық қасиеттерін көрсететін шама екенін байқаймыз. Элементтердің электіртерістігі туралы мәліметтер олар түзетін химиялық байланысты түзуге көмегін тигізеді.
Бүгінгі тақырыбымыз химиялық байланыстың негізгі түрлері. Осы тақырып бойынша табиғаттың негізгі құраушылары ауаға, табиғи су қорларына, өндіріске ауа шарымен саяхатқа шығамыз.
ІІ аялдамамыз - «Ауа кеңістігінен » бастаймыз, ол үшін ауаның құрамына тоқталамыз. Ауаның құрамындағы сутек, оттек, азот молекулалары өзара бірдей екі атомнан тұратын жай затттар H 2 O 2 N 2 ковалентті полюссіз байланыс түзеді.
 Электіртерістіктері бірдей сутектің 2 атомының әрекеттесіп молекулаға айналуын қарастырсақ. Сутек атомы оң зарядты ядродан және оны қоршаған шар пішінді электрон бұлтынан тұратындығы белгілі. Осындай екі атом әрекеттескенде, олардың электрон бұлыттары жақындасып бірімен-бірі араласады.
Электіртерістіктері бірдей сутектің 2 атомының әрекеттесіп молекулаға айналуын қарастырсақ. Сутек атомы оң зарядты ядродан және оны қоршаған шар пішінді электрон бұлтынан тұратындығы белгілі. Осындай екі атом әрекеттескенде, олардың электрон бұлыттары жақындасып бірімен-бірі араласады.
·H + · H → H ∙∙H
атом атом молекула бұдан шығатыны
- Қай заттың болсын молекуласындағы атомдар белгілі -бір ретпен орналасады.
- Молекуланың құрамындағы атомдар өзара тікелей не болмаса басқа атом арқылы қосылысса да біріне-бірі әсер етеді.
- Заттың қасиеті молекуладағы атомдардың қосылу ретіне және олардың біріне-бірінің әсеріне, яғни химиялық құрылысна тәуелді.
- Заттың химиялық қасиеттеріне сүйіне отырып, оның молекуласынығ құрылысын анықтауға болады.
Сонда жұптаспаған электрондар жұптасу үшін атомдар арсында химялық байланыс түзіледі. Сыртқы валентілік электрондарын 8 ге толтыру үшін электіртерістілігі төмен элементтер беріп жіберсе, электіртерістігі жоғары элементтер қосып алуға бейім. Сондықтан арасында байланыс түзіледі.
Химиялық байланыстың 1916 жылы американ ғалымы ЛЬЮИС теориясын ұсынды.
Теорияда- 1. Атомдар молекула құрып біріккенде ортақ электрон қосағын түзу арқылы өздерінің сыртқы қабаттарын инертті газдардікіндей етуге тырысады.
2. Химиялық байланыс әсерлесуші атомдардың екеуіне де ортақ электрон жұбы арқылы жасалады. Бір электрон жұбын түзу үшін әратом бір-бір электроннан жұмсайды.
Бір не болмаса бірнешеэлектрон жұптары арқылы түзілетін химиялық байланыс
к о в а л е н т т і к байланыс деп атайды.
ІІ аялдама «Табиғи су қорларына» саяхат. Баріміз білеміз теңіз суларындатұз коп кездесетінін. Сол тұздардың арасындағы байланыс и о н д ы қ байланыс түзеді . Атомдарэлектрондарын беріп жіберу немесе қосыпалу арқылы оң нетеріс зарядталады. Мұндайзарядталған атомдар иондар деп аталады. Демек. қарама-қарсы зарядталған иондарарсындағы байланысты иондық байланыс деп атайды. 1916 жылы неміс ғалымы Коссель ұсынды. Өзінің сыртқы валенттік электрондарына сай электрон бұлтын берген атомдар оң зарядты катиондарға , ал осы электрондарға сай бұлтты қосып алған атомдар терісзарядты анионындарға айналады. Түзілген иондар біріне-бірі Кулон заңы бойынша тартылысып. иондық байланыс түзіледі.
Мысалы
Na 0 + F 0 → Na + F -
Na 0 + Cl 2 0 → Na + Cl -
K 0 + Cl 2 0 → K + Cl -
Zn 0 + S 0 → Zn + S -
ІІІ аялдама «Өндіріске» саяхат. Біз білеміз өндірісте әртүрлі заттар өндіреді соның ішінде қышқыл өндіретін зауытқа саяхатқа атанамыз. Жалпыалғанда әрекеттесуші атомдардың азғантай болса да айырмашылықтарына байланысты, көбіне молекулалар ковалентті поюсті байланыс түзеді. Коваленттік полюстібайланыс көбіне қышқылдарға тән .
Мысалы ∙∙ ∙∙
∙H + ∙Cl ∙∙ → H ∙∙Cl∙∙
∙∙ ∙∙
кестемен жұмыс жасаймыз.
Полюсті молекуладағы электрондар ығысқан кезде атомдар қосымша зарядқа ие бола бастайды. Молекуланың бір жағы оң, бір жағы теріс зарядталады. Мұндай молекулалар полюсті деп аталады.
ІҮ аялдама «Гүлдер»
Кесте толтыру
Полюссіз
Ковалентті
Полюсті
ковалентті
Жоғарыда берілген кестенің сәйкес бағанына мына заттарды толтырыңыз
NaI, ZnF2, N2, H2SO4, PH3, O2, HNO3, H2S, I2, KNO3, Br2,
Тест тапсырмалары
- Электртерістік дегеніміз не?
А) атомның электрон беру қабілеті
Б) қосылыстағы атомнығ электронды өзіне тарту қабілеті.
С) атомның қосылыстағы белгілі валенттік көрсететін қасиеті.
- Элементтердің электртерістілігі период бойынша қалай өзгереді?
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz