Алюминий және оның қосылыстары: қасиеттері, құрылымы және қолданылуы


Сабақтың тақырыбы: Алюминий және оның қосылыстары
Сабақтың мақсаты:
Екідайлы элементтер жайлы білімді сатылай кешенді талдай отырып дамыту. Алюминиийді мысалға ала отырып жай зат ретіндегі қасиеттерін, қосылыстары олардың қолданылуы туралы мәлімет алу.
Сабақтың міндеті: 1. Екідайлы элементтер табиғатын оқып-үйрену
2. Алюминиий оның қосылыстарымен танысу
3. Тірек-сызбаны есеп шығаруда қолдана білу
Сабақтың әдісі: жаңа сабақ
Сабақтың әдісі: Сатылай кешенді талдау технологиясы
Көрнекілігі: Периодтық кесте, қымбат, бағалы тастар (жинақ), тау жыныстары(жинақ),
Al сымды қыздыру(44 сурет) . Алюминий (жинақ), Al қолдану (45 сурет)
Сабақтың жүру барысы:
Болмаса да айтарлықтай салмағым
Көп металдан ардақтымын алдамын
Ұшақ болып аспанға ұшып, қалықтап,
Жердің жүзін, көк аспанды шарладым.
Дюралюмин дейтін менің қоспамды,
Әспеттейді химияның достары
Тұрмыста үстел, ыдыс-аяқ кереует,
Бағандардың бұйдаларын қостым мен
Қағаз да мен кәмпит, шайды сәндеген
Токқа балқып келіп тұрған ән де мен
- Өлең жолдарына талдау жасап, мысалдар келтіру арқылы шешуін табу.
Периодтық жүйедегі орны
1. Химиялық таңбасы- Al
2. Реттік нөмірі- 13
3. Ar(Al) - 27
4. Период нөмірі- ІІІ (кіші)
5. Топ нөмірі-ІІІ (негізгі)
Атом құрылысы:
1. Ядро заряды- +13
2. Электрон саны- 13
3. Протон саны- 13
4. Нейтрон саны -14
5. Энергетикалық деңгей саны -3
6. Валенттілік электрондары- 3
7. Электрондық конфигурациясы 1s 2 /2s 2 2P 6 /3s 2 3p 1
Табиғатта кездесуі:
1. Өзгемен салыстарғанда алатын орны- І
2. Өзге элементтермен салыстарғанда алатын орны-ІІІ (O 2 , Si)
3. Алюмосиликаттар (Al, O 2 , Si, Сілті Me, Сілті. жер Me)
 4. Каолинит (H
2
O
3
· 2SiO
2
· 2H
2
O) саз балшық
4. Каолинит (H
2
O
3
· 2SiO
2
· 2H
2
O) саз балшық
5. Корунд (Al 2 O 3 ) өте қатты, рубин(қызыл), аметист(күлгін), сапфир (көк) 43 сурет
6. Боксит (Al 2 O 3 · nH 2 O)
7. Қазақстанда кездесетін кен орындары: Қостанай, Ақтөбе облыстарында
Физикалық
m- күмістей ақ, Me, p=2. 7 г/см 3
Электр жылу өткізгіш(Ag, Cu) ; T қайнау=650 0 С
Кристал торы-көлемді орталық куб.
Қасиеті
Химиялық
1. Белсенді Me (Me k акт. қатары) бірақ алюминий ыдыс +O 2 ; H 2
2. 4Al 0 +3
=
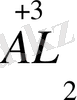
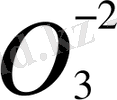
Al- тотықсыздандырғыш
Al 2 O 3 -қабықша қалыңдығы: 0, 1мм
Al 2 O 3 -күңгірт m, жемірілуге тұрақты
3.
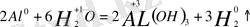
4.
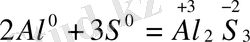
5.
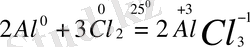
6.
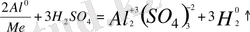
7.
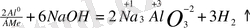
8. 2Al+Fe 2 O 3 =Al 2 O 3 +2Fe+3241кДж
Қосылыстары:
- Al2O3ф. қ. Т-ақ, Тб. = 20500С
Кристал торы-атомдық байланыс-ковалентті
(зат берік, қатты)
Al 2 O 3 - суда ерімейді, онымен әрекеттеспейді
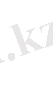
Х. қ. Al 2 O 3 +6HCl
2AlCl 3 +3H 2 O
Al 2 O 3 +6NaOH
2Na 3 AlO 3 +3H 2 O
Қолданылуы: Электролиз арқылы ме Al алу.
Жасанды кристалдар, лазер жасау үшін
Рубин, сапфир
2. Al(OH) 2 T-ақ, суда ерімейді
Алу: AlCl 3 +3NaOH=Al(OH) 3 ↓ +3NaCl
Ақ ірімшік
тәрізді
сапал. Реакция
Х. қ. 1. Al(OH) 3 ↓+3HNO 3 =Al(NO 3 ) 3 +3H 2 O
2. Al(OH) 3 ↓+NaOH= NaAlO 2 +2H 2 O
3. 2Al(OH) 3
Al 2 O 3 +3H 2 O
4. Al тұздары әлсіз негіз тұздары ретінде сатылап диссоциаланады. (қышқыл орта көрсетеді)
Алынуы:
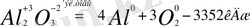
2007 ж. Павлодар электролиз зауыты
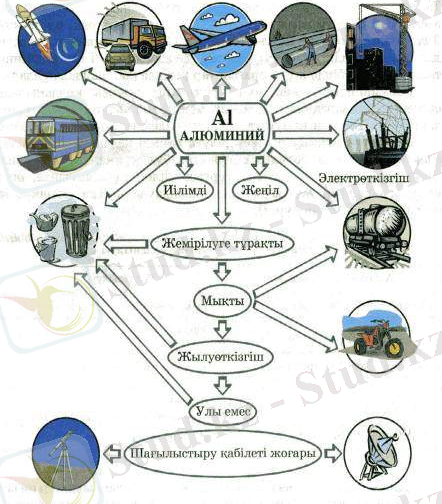
Қолданылуы:
Есептеу № 9
Мазмұны:
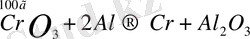
Белгілі: 15, 2г → 9г
Белгісіз: х %
Шешуі:
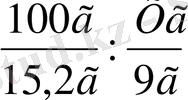
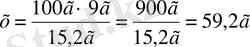
Жауабы: х=15, 2%
Тексеру: 59, 2г-100%
9г- х%
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz