9-сынып: ерітінділерге байланысты есептерді шешу әдістемесі, алгоритмдері мен практикалық тапсырмалар жауаптарымен


ЕРІТІНДІГЕ БАЙЛАНЫСТЫ ЕСЕПТЕР
9 сынып
Ерітінділерге байланысты типтік есептердің шығарылу әдістемесі қарастырылып, оларды шешудің алгоритмі берілген. Оқушылардың есеп шығару машықтарын берік етіп қалыптастыру мақсатында өз бетімен шығаруға болатын есептер ұсынылған. Сонымен қатар есептердің жауаптары бар. Ерітінді дайындауға арналған есептер:
Массалық үлесі 0, 06 немесе 6 % массасы 230 г калий нитратының ерітіндісін дайындауға қажетті су мен калий нитратының массаларын есептеңіздер.
Берілгені:
ω 1 (КNО 3 ) =0, 06
m (КNО 3 ) = 230 г
Т/к m (КNО 3 ) , m (Н 2 О)
Шешуі:
1) Массалық үлестері бойынша ерітіндідегі таза заттардың массаларын есептейміз:
m (ер. зат)
ω (ер. зат) =
m (ерітінді)
m (ер. зат) = ω (ер. зат) •m (ерітінді)
m (КNО 3 ) = 0, 06•230 = 13, 8 г
2) Ерітінді дайындау үшін қажетті судың массасы:
M (Н 2 О) = m (ер-ді) - m (КNО 3 ) = 230 -13, 8 = 216, 2 г
Жауабы: КNО 3 - 13, 8 г; Н 2 О - 216, 2 г.
Массасы 25 г мыс купоросын (СuSO 4 •5Н 2 О) көлемі 200 мл ( р = 1 г/см³) суда ерітті. Алынған ерітіндідегі сусыз мыс сульфатының массалық үлесін (%) есептеңіздер.
Берілгені:
m (СuSO 4 •5Н 2 О ) = 25 г
V(H 2 О) = 200 мл
р (H 2 О ) = 1 г/см³
Т/к ω (СuSO 4 )
Шешуі:
1) Мыс купоросы мен мыс сульфатының молярлық массаларын есептейміз:
М (СuSO 4 •5Н 2 О) = 63, 5 +32+16•4 +18•5= 249, 5 г/моль
М (СuSO 4 ) = 63, 5 + 32 + 16•4 = 159, 5 г/моль
2) Кристаллогидрат құрамындағы сусыз мыс сульфатының массасы:
249, 5 г СuSO 4 •5Н 2 О 159, 5 г СuSO 4
25 г СuSO 4 •5Н 2 О х г СuSO 4
159, 5•25
х = = 15, 98 г
249, 5
3) Еріткіштің массасын анықтаймыз:
M (Н 2 О) = V(Н 2 О) •p (Н 2 О) =200 •1 = 200 г
4) Түзілген ерітіндінің массасы:
m (ерітінді) = m (еріткіш) + m(тұз)
m (ерітінді) = 200 +25 = 225 г
5) Мыс сульфатының массалық үлесі:
m (ер. зат)
ω (ер. зат) = • 100 %
m (ерітінді)
15, 98 г •100 %
ω (СuSO 4 ) = = 7, 1 %
225
Жауабы: 7, 1 %.
Еріген заттың массалық үлесі 50 %, р = 1, 3 г/см³, көлемі 250 см³ азот қышқылының ерітіндісіне көлемі 1 л су қосылғанда түзілген ерітіндідегі азот қышқылының массалық үлесін (%) есептеңіздер.
Берілгені:
ω 1 (НNО 3 ) = 50 %
V(ер-ді) = 250 см³
р (ер-ді) = 1, 3 г/см³
V(H 2 О) =1 л
Т/к ω 2 (НNО 3 )
Шешуі:
1) Массалық үлесі 50 %-қ ерітіндідегі азот қышқылының массасын есептейміз:
100 г ерітіндіде 50 г НNО 3 болса, 250 - 1, 3 г ерітіндіде х г НNО 3 бар.
250 - 1, 3 • 50
х = = 162, 5 г
100 2) Массалық үлесі 50 %-қ ерітіндінің массасы:
m (ер-ді) = V(ер-ді) • р (ер-ді) = 250 см³•1, 3 г/см³ = 325 г
3) Қышқыл мен судан тұратын ерітіндінің массасы:
m (ер-ді) = 1000 +325 = 1325 г
4) Су қосылған ерітіндідегі азот қышқылының массалық үлесі:
m (ер. зат)
ω (ер. зат) = • 100 %
m (ерітінді)
162, 5г •100 %
ω 2 (НNО 3 ) = = 12, 26 %
1325 г
Жауабы: 12, 26 %
Массалық үлесі 20 %-қ массасы 500 г ерітінді дайындау үшін массалық үлестері 10 % және 30 % болатын бірдей тұз ерітінділерінің қандай массасы қажет? Берілгені: ω 1 = 10 % ω 2 = 30 % ω 3 = 20 % m 3 = 500 г Т/к m 1, m 2 Шешуі: Крест ережесін қолданамыз:
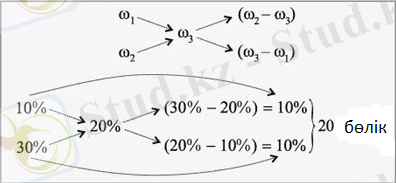
20 %-қ 500 г тұз ерітіндісін дайындау үшін бастапқыда алынған ерітінділердің концентрациясынан 10 бөліктен алу керек. 1 бөлік 500
:
(10 + 10) = 25 грамға тең, ал 10 бөлік 25•10 = 250 г бұдан, m
1
= 250 г; m
2
= 250 г
Есепті тексеру
10 %-қ 100 г ерітіндіде 10 г тұз болса, 10 %-қ 250 г ерітіндіде х г тұз болады.
250 •10
z = = 25 г
100 30 %-қ 100 г ерітіндіде 30 г тұз болса, 30 %-қ 250 г ерітіндіде у г тұз болады.
250 •30
у = = 75 г
100 m ( ерітінді) = 250+250 = 500 г m(тұз) = 25 + 75 = 100 г. Бұдан
 3
табамыз : 500 г ерітіндіде 100 г тұз болса, 100 г ерітіндіде
3
табамыз : 500 г ерітіндіде 100 г тұз болса, 100 г ерітіндіде
 3
г тұз болады.
3
г тұз болады.
100 •100
 3
= = 20 г немесе 20 %
3
= = 20 г немесе 20 %
500
Жауабы: m 1 = 250 г, m 2 = 250 г.
Массалық үлесі 0, 3 немесе 30 % -қ 150 г натрий хлоридінің ерітіндісі мен массалық үлесі 0, 1 немесе 10 % -қ 250 г натрий хлоридінің ерітіндісін араластырған. Алынған ерітіндідегі натрий хлоридінің массалық үлесі (%) қандай? Берілгені:
m 1 (NaCІ ) = 150 г
m 2 (NaCІ ) = 250 г
ω 1 (NaCІ ) = 30 %
ω 2 (NaCІ ) = 10 %
Т/к ω 3 (NaCІ ) Шешуі: 1- әдіс ( пропорция әдісі) 1) Ерітіндінің жалпы массасы:
m 3 = m 1 + m 2 = 150 + 250 = 400 г 2) Бірінші және екінші ерітіндідегі натрий хлоридінің масссасын анықтаймыз:
100 г ерітіндіде 30 г NaCІ болса, 150 г ерітіндіде х г NaCІ бар.
30 •150
х = = 45 г
100
100 г ерітіндіде 10 г NaCІ болса, 250 г ерітіндіде у г NaCІ бар.
10 •250
у = = 25 г
100
3) Түзілген ерітіндінің құрамындағы натрий хлоридінің массасы:
45 +25 =70 г 4) Түзілген ерітіндінің концентрациясы:
400 г ерітіндіде 70 г NaCІ болса, 100 г ерітіндіде z г NaCІ бар.
70 •100
z = = 17, 5 г немесе 17, 5 %
400
2- әдіс ( алгебралық әдіс)
m
1
•
 1
+ m
2
•
1
+ m
2
•
 2
=
2
=
 3
(m
1
+ m
2
) .
3
(m
1
+ m
2
) .
Бұдан
( m
1
•
 1
+ m
2
•
1
+ m
2
•
 2
)
2
)
 3
=
3
=
(m 1 +m 2 )
(150 •30+250•10)
 3
= = 17, 5 %
3
= = 17, 5 %
(150+250)
3- әдіс ( «крест» ережесі)
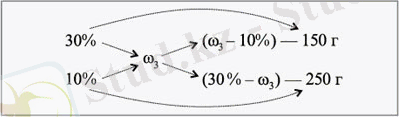
(
 3
- 10) 150
3
- 10) 150
= (30 -
 3
) 250
3
) 250
(30 -
 3
) •150 = (
3
) •150 = (
 3
- 10) •250 4500 -150•
3
- 10) •250 4500 -150•
 3
= 250•
3
= 250•
 3
- 2500 4500 +2500=250•
3
- 2500 4500 +2500=250•
 3
= 150•
3
= 150•
 3
7000 = 400•
3
7000 = 400•
 3
3
 3
= 7000/400 = 17, 5 %
3
= 7000/400 = 17, 5 %
Жауабы: 17, 5 %.
15 %-қ 540 г ерітінді дайындау үшін қажетті 10 % -қ натрий карбонаты ерітіндісінің массасы мен құрғақ кристаллогидраттың (Na 2 CO 3 •10H 2 O) массасын табыңыздар. Берілгені: ω 1 = 10 % ω 3 = 15 % m 3 = 540 г Т/к m 1, m 2 Шешуі: 1- әдіс (екі белгісіз арқылы теңдеулер жүйесін құру) 1) 15 % -қ 540 г ерітіндідегі натрий карбонатының массасы: 15 %-қ 100 г ерітіндіде 15 г тұз болса, 15 %-қ 540 г ерітіндіде z г т ұз болады.
540 •15
z = = 81 г
100
2) Na 2 CO 3 •10H 2 O-ң молярлық массасын есептейміз: М (Na 2 CO 3 •10H 2 O) =106 + 180 = 286 г/моль
3) Теңдеулер жүйесін құрамыз: х+ у = 81 m 1 +m 2 = 540 ( х г 10 %-қ ерітінді құрамындағы тұз, у г Na 2 CO 3 •10H 2 O құрамындағы тұз)
286•у
m 2 =
106
10 %-қ 100 г ерітіндіде 10 г тұз болса, m 1 г 10 %-қ ерітіндіде х г тұз бар.
100•х
m 1 = = 10 х
10
4) Теңдеулер жүйесінде m 1 , m 2 мәндерін орнына қойып, оны шешу арқылы құрғақ Na 2 CO 3 •10H 2 O масасын табамыз:
286 • у
10 х + = 540
106 х + у = 81
х = 81 - у
286 • у
10 (81-у) + = 540
106
810 - 10у +2, 7у = 540 -7, 3у = - 810 + 540 - 7, 3у = - 270
- 270
у = = 37 г
- 7, 3
286 • у
m 2 = = 2, 7 •37 = 100 г (қажетті құрғақ Na 2 CO 3 •10H 2 O масасы)
106
х = 81 - у = 81 - 37 = 44 г (10 %-қ ерітіндідегі тұздың массасы) 5) 10 %-қ ерітіндінің массасы: 10 %-қ 100 г ерітіндіде 10 г тұз болса, m 1 г 10 %-қ ерітіндіде 44 г тұз бар.
100 • 44
m 1 = = 440 г
10
2 әдіс ( крест ережесі) 1) Кристаллогидраттың құрамындағы тұздың массасы немесе массалық үлесі:
286 г Na 2 CO 3 •10H 2 O 106 г тұз болса, 100 г Na 2 CO 3 •10H 2 O х г тұз бар.
100 •106
х = = 37 г немесе 37 %
286 2) Крест ережесін қолданамыз:
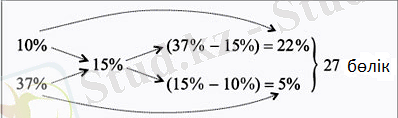
3) Бір бөліктің массасы мен зат массасын есептейміз: 540/27 = 20 г, 4) 10 %-қ ерітіндінің массасы : m 1 = 20•22 = 440 г, Na 2 CO 3 •10H 2 O массасы: m 2 = 20•5 = 100 г.
Жауабы: 10 %-қ ерітіндінің массасы 440 г
және 100 г Na 2 CO 3 •10H 2 O.
ЕСЕПТЕР
1) 25 %-қ 300 г ерітінді дайындау үшін тұздың массалық үлестері 60 % -қ және 10 %-қ екі ерітіндінің қандай массаларын араластыру қажет?
Жауабы: m 1 - 90 г, m 2 - 210 г.
2) 45 %-қ 250 г ерітіндіні су қосып сұйылтқанда массалық үлесі 10 % -қ ерітінді алынды. Судың массасын есептеңіздер.
Жауабы: m 2 - 875 г.
3 ) 10 %-қ 250 г ерітіндінің концентрациясын 45 %-ға жеткізу үшін қажетті құрғақ тұздың массасын табыңыздар.
Жауабы: m(құрғақ тұз) - 158 г.
4) Еріген заттың массалық үлесі 50 % массасы 200 г күкірт қышқылының ерітіндісін әзірлеу үшін 60 %-қ және 20 %-қ ерітінділерден қанша керек?
Жауабы: m 1 - 150 г, m 2 - 50 г.
- Іс жүргізу
- Автоматтандыру, Техника
- Алғашқы әскери дайындық
- Астрономия
- Ауыл шаруашылығы
- Банк ісі
- Бизнесті бағалау
- Биология
- Бухгалтерлік іс
- Валеология
- Ветеринария
- География
- Геология, Геофизика, Геодезия
- Дін
- Ет, сүт, шарап өнімдері
- Жалпы тарих
- Жер кадастрі, Жылжымайтын мүлік
- Журналистика
- Информатика
- Кеден ісі
- Маркетинг
- Математика, Геометрия
- Медицина
- Мемлекеттік басқару
- Менеджмент
- Мұнай, Газ
- Мұрағат ісі
- Мәдениеттану
- ОБЖ (Основы безопасности жизнедеятельности)
- Педагогика
- Полиграфия
- Психология
- Салық
- Саясаттану
- Сақтандыру
- Сертификаттау, стандарттау
- Социология, Демография
- Спорт
- Статистика
- Тілтану, Филология
- Тарихи тұлғалар
- Тау-кен ісі
- Транспорт
- Туризм
- Физика
- Философия
- Халықаралық қатынастар
- Химия
- Экология, Қоршаған ортаны қорғау
- Экономика
- Экономикалық география
- Электротехника
- Қазақстан тарихы
- Қаржы
- Құрылыс
- Құқық, Криминалистика
- Әдебиет
- Өнер, музыка
- Өнеркәсіп, Өндіріс
Қазақ тілінде жазылған рефераттар, курстық жұмыстар, дипломдық жұмыстар бойынша біздің қор #1 болып табылады.



Ақпарат
Қосымша
Email: info@stud.kz